Thionylchlorid
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Thionylchlorid (Trivialname) ist eine stark lichtbrechende farblose Flüssigkeit, das Dichlorid der Schwefligen Säure.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
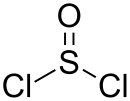 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Thionylchlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | SOCl2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose, stark lichtbrechende, erstickend riechende Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 118,97 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
76 °C[2] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,518 (20 °C)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 1 ml·m−3 bzw. 5 mg·m−3[5] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Geschichte
Thionylchlorid wurde erstmals im Jahre 1849 durch die Umsetzung von Schwefeldioxid mit Phosphorpentachlorid erhalten.[6][7][8] Nachdem seine Eignung als Chlorierungsreagenz erkannt worden war, wurde es etwa ab 1900 im industriellen Maßstab hergestellt und verwendet.[9]
Eigenschaften
Zusammenfassung
Kontext

Thionylchlorid ist eine farblose bis gelbliche, an der Luft rauchende Flüssigkeit, die sich in Wasser oder bei Erhitzung oder unter Lichteinwirkung zersetzt. Ihre Dämpfe wirken schon bei großer Verdünnung erstickend.[2] Die Verbindung reagiert heftig mit Wasser und Basen sowie mit einigen Alkoholen. Beim Erhitzen über 80 °C zerfällt es in Schwefeldioxid, Chlor und Dischwefeldichlorid,[10] gemäß der Gleichung:
Bei der Reaktion mit Wasser bilden sich Chlorwasserstoff und Schwefeldioxid:[2]
Herstellung
Zusammenfassung
Kontext
Thionylchlorid wird im Labor durch Einleiten von Schwefeltrioxid in Schwefeldichlorid oder durch Überleiten von Schwefeldioxid über Phosphorpentachlorid hergestellt:[11]
Verwendung
- In Lithium-Thionylchlorid-Batterien als Lösungsmittel und Elektrolyt
- Industriell wird Thionylchlorid zur Herstellung folgender Substanzen verwendet:
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.








