Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Lithiumperoxid, Li2O2 ist eine Sauerstoffverbindung des Alkalimetalls Lithium.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
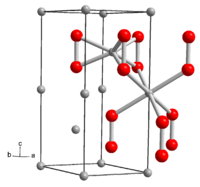 | ||||||||||||||||
| _ Li+ _ O− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Lithiumperoxid | |||||||||||||||
| Andere Namen |
Dilithiumperoxid | |||||||||||||||
| Verhältnisformel | Li2O2 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 45,88 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,36 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit |
exotherme Reaktion mit Wasser[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Die Darstellung erfolgt durch Umsetzung von Lithiumhydroxid mit Wasserstoffperoxid und anschließendem Erhitzen unter Abspaltung von Wasserstoffperoxid[4]
Lithiumperoxid ist ein in reinster Form farbloser, gewöhnlich gelblicher Feststoff. Mit Wasser erfolgt Bildung von Wasserstoffperoxid. Die Verbindung hat eine hexagonale Kristallstruktur mit der Raumgruppe P63/mmc (Raumgruppen-Nr. 194) und den Gitterparametern a = 3,183 Å und c = 7,726 Å.[5] Die Kristallstruktur enthält zwei kristallographisch verschiedene Li-Atome. Eines ist von den sechs Sauerstoffatomen dreier Perioxidionen koordiniert, das zweite in einem verzerrten Oktaeder von den Sauerstoffatomen sechs benachbarter Peroxidionen. Die Standardbildungsenthalpie von Lithiumperoxid beträgt ΔHf0 = −633 kJ/mol.[6]
Lithiumperoxid kann zur Herstellung hochreinen Lithiumoxids eingesetzt werden. Hierbei wird Lithiumperoxid bei 195 °C zersetzt, wobei sich Lithiumoxid und Sauerstoff bilden:[4]
Des Weiteren wird es in der Raumfahrt zur Regeneration der lebenserhaltenden Gasversorgungssysteme eingesetzt. Mit Kohlenstoffdioxid reagiert es zu Lithiumcarbonat und Sauerstoff. Hierdurch wird der Atemluft Kohlenstoffdioxid entzogen und Sauerstoff freigesetzt.[7]
Lithiumperoxid findet Verwendung als Härter für spezielle Polymere.[8] Es wird weiterhin für die sich in der Entwicklung befindenden Lithiumperoxid-Akkumulatoren verwendet bzw. beim Entladebetrieb in der Batterie gebildet.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.