chemická sloučenina From Wikipedia, the free encyclopedia
Hexakarbonyl vanadu, V(CO)6, je modrozelená těkavá pevná látka.[1] Tato sloučenina je z teoretického hlediska velmi zajímavá, protože jde o homoleptický karbonyl kovu, který je paramagnetický. Většina sloučenin se vzorcem Mx(CO)y dodržuje 18-elektronové pravidlo, ale V(CO)6 má 17 valenčních elektronů.
| Hexakarbonyl vanadu | |
|---|---|
 Strukturní vzorec | |
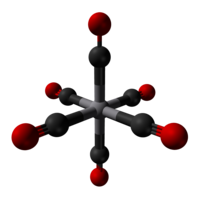 Krystalová struktura | |
| Obecné | |
| Systematický název | Hexakarbonyl vanadu |
| Anglický název | Vanadium hexacarbonyl |
| Německý název | Vanadiumhexacarbonyl |
| Sumární vzorec | V(CO)6 |
| Vzhled | modrozelené krystaly |
| Identifikace | |
| Registrační číslo CAS | 20644-87-5 |
| PubChem | 519800 |
| SMILES | O=C=[V](=C=O)(=C=O)(=C=O)(=C=O)=C=O |
| Vlastnosti | |
| Molární hmotnost | 219,00 g/mol |
| Teplota tání | rozklad |
| Hustota | 1,7 g/cm3 |
| Rozpustnost ve vodě | nerozpustný |
Některá data mohou pocházet z datové položky. | |
Hexakarbonyl vanadu se připravuje redukcí chloridu vanaditého sodíkem v přítomnosti oxidu uhelnatého (160 °C, 20 MPa). Tato reakce se provádí zpravidla v diglymu:[1][2]
Produkt je poté redukován krystalickou kyselinou fosforečnou:
Další možností je reduktivní karbonylace pomocí směsi zinku a hořčíku v nadbytku pyridinu při teplotě 120-140 °C.[3]
V(CO)6 má oktaedrickou geometrii, je izostrukturní s hexakarbonyl chromem a hexakarbonyl molybdenem. RTG strukturní analýza ukázala, že molekula je mírně deformována, axiální vazby V-C mají délku 1,993(2) Å, zatímco čtyři ekvatoriální vazby V-C jsou mírně delší, 2,005(2) Å.[4]
Hexakarbonyl vanadu je termicky nestabilní. Primární reakcí je redukce na anion V(CO) -
6 . Také lze provést substituci terciárními fosfiny, ta ale často vede k disproporcionaci.
Reakce se zdroji cyklopentadienylového aniontu vede ke vzniku oranžového komplexu (C5H5)V(CO)4. Ten se řadí do skupiny polosendvičových komplexů.[5]
Seamless Wikipedia browsing. On steroids.