From Wikipedia, the free encyclopedia
Retinoblastomski protein (pRb, Rb, RB ili RB1) je tumor-supresorski protein čija nefunkcionalnost uzrokuje nekoliko glavnih kancera.[5] Jedna od funkcija pRb je sprečavanje prekomjerne proliferacije ćelija, inhibiranjem progresije ćelijskog ciklusa sve dok ćelija nije spremna za diobu. Kad je ćelija spremna za podjelu, pRb se fosforilira, deaktivirajući je, i dopušta se ćelijskom ciklusu da napreduje. Također je regruter nekoliko enzima za remodeliranje hromatina, kao što su metilaze i acetilaze.[6]
pRb pripada porodici džepnih proteina, čiji članovi imaju džep za funkcionalno vezivanje drugih proteina.[7][8] Ako se onkogeni proteini, poput onih koje proizvode ćelije inficirane visokorizičnim tipovima ljudskog papiloma virusa, veže i inaktivira pRb, to može dovesti do raka. Gen RB je možda bio odgovoran za evoluciju višećelijskih oblika u nekoliko loza života, uključujući životinje.[9]
Kod ljudi, protein je kodiran genom RB1 koji se nalazi na hromozomu 13, tačnije, na sekvenci 13q14.1-q14.2. Ako oba alela ovog gena mutiraju u ranom životu, protein se inaktivira i rezultira razvojem retinoblastomakog raka, pa otuda i naziv pRb (p=protein). Ćelije mrežnjače se ne odmazuju i ne zamjenjuju, te su podvrgnute visokom nivou mutagenog UV-zračenja, pa se zato većina izlučivanja pRb-a javlja u njenom tkivu (ali je također dokumentirano kod određenih karcinoma kože kod pacijenata iz New Yorka i Novog Zrelanda gdje je količina UV zračenja znatno veća).
Uočena su dva oblika retinoblastoma: bilateralni, porodični i jednostrani, sporadični oblik. Pacijenti ovih bolesti imali su šest puta veću vjerojatnoću da će kasnije u životu razviti druge tipove raka.[10] Ovo je naglasilo činjenicu da se mutirani pRb mogao naslijediti i dati podršku za hipotezu o dva pogotka. Ovo navodi na zaključak da je samo jedan aktivni alel genski supresor tumora neophodan za njegovu funkciju (mutirani gen je recesivan), pa se prije pojave fenotipa raka dogosila takva mutacija. U porodičnom obliku, mutirani alel se nasljeđuje zajedno s normalnim. U ovom slučaju, ako bi ćelija održala samo jednu mutaciju u drugom "RB" genu, svi pRb u toj ćeliji bili bi nedjelotvorni u inhibiranju progresije ćelijskog ciklusa, dopuštajući ćelijama da se nekontrolirano dijele i na kraju postanu kancerogene. Nadalje, kako je jedan alel već mutiran u svim ostalim somatskim ćelijama, buduća učestalost karcinoma kod ovih osoba javlja se prema linearnoj kinetici.[11] Aktivni alel ne mora se podvrgnuti mutaciji per se, jer se u takvim tumorima često primjećuje gubitak heterozigotnosti (LOH) .
Međutim, u sporadičnom obliku, oba alela bi morala održati mutaciju prije nego što ćelija postane kancerogena. Ovo objašnjava zašto oboljeli od sporadičnog retinoblastoma nisu u povećanom riziku od raka kasnije u životu, jer su oba alela funkcionalna u svim drugim ćelijama. Buduća učestalost karcinoma u sporadičnim slučajevima pRb-a promatrana je polinomnom, kinetikom, ne baš kvadratnom, kako se očekivalo jer prva mutacija mora nastati normalnim mehanizmima, a zatim je LOH može duplicirati tumorskim progenitorima.
RB1 ortolozi [12] identificirani su i kod većine sisara, za koje su dostupni potpuni podaci o genomu.
RB/E2F-proteini porodice potiskuju transkripciju.[13]
pRb je multifunkcionalni protein s mnogim mjestima vezanja i fosforilacija. Iako se njegova zajednička funkcija smatra vezanjem i potiskivanjem ciljeva E2F, pRb je vjerovatno višenamjenski protein jer se veže na najmanje 100 drugih proteina.[14]
pRb ima tri glavne strukturne komponente: karboksi-kraj, "džepnu" podjedinicu i amino-kraj. Unutar svakog domena postoje različita mjesta vezivanja proteina, kao i ukupno 15 mogućih mjesta fosforilacije. Općenito, fosforilacija uzrokuje zaključavanje među domenima, što mijenja konformaciju pRb i sprječava vezanje za ciljne proteine. Različita mjesta mogu se fosforilirati u različito vrijeme, što dovodi do mnogih mogućih konformacija i vjerovatno mnogih funkcija/nivoa aktivnosti.[15]
Dužina polipeptidnog lanca je 928 aminokiselina, a molekulska težina 106.159 Da.[16].
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MPPKTPRKTA | ATAAAAAAEP | PAPPPPPPPE | EDPEQDSGPE | DLPLVRLEFE | ||||
| ETEEPDFTAL | CQKLKIPDHV | RERAWLTWEK | VSSVDGVLGG | YIQKKKELWG | ||||
| ICIFIAAVDL | DEMSFTFTEL | QKNIEISVHK | FFNLLKEIDT | STKVDNAMSR | ||||
| LLKKYDVLFA | LFSKLERTCE | LIYLTQPSSS | ISTEINSALV | LKVSWITFLL | ||||
| AKGEVLQMED | DLVISFQLML | CVLDYFIKLS | PPMLLKEPYK | TAVIPINGSP | ||||
| RTPRRGQNRS | ARIAKQLEND | TRIIEVLCKE | HECNIDEVKN | VYFKNFIPFM | ||||
| NSLGLVTSNG | LPEVENLSKR | YEEIYLKNKD | LDARLFLDHD | KTLQTDSIDS | ||||
| FETQRTPRKS | NLDEEVNVIP | PHTPVRTVMN | TIQQLMMILN | SASDQPSENL | ||||
| ISYFNNCTVN | PKESILKRVK | DIGYIFKEKF | AKAVGQGCVE | IGSQRYKLGV | ||||
| RLYYRVMESM | LKSEEERLSI | QNFSKLLNDN | IFHMSLLACA | LEVVMATYSR | ||||
| STSQNLDSGT | DLSFPWILNV | LNLKAFDFYK | VIESFIKAEG | NLTREMIKHL | ||||
| ERCEHRIMES | LAWLSDSPLF | DLIKQSKDRE | GPTDHLESAC | PLNLPLQNNH | ||||
| TAADMYLSPV | RSPKKKGSTT | RVNSTANAET | QATSAFQTQK | PLKSTSLSLF | ||||
| YKKVYRLAYL | RLNTLCERLL | SEHPELEHII | WTLFQHTLQN | EYELMRDRHL | ||||
| DQIMMCSMYG | ICKVKNIDLK | FKIIVTAYKD | LPHAVQETFK | RVLIKEEEYD | ||||
| SIIVFYNSVF | MQRLKTNILQ | YASTRPPTLS | PIPHIPRSPY | KFPSSPLRIP | ||||
| GGNIYISPLK | SPYKISEGLP | TPTKMTPRSR | ILVSIGESFG | TSEKFQKINQ | ||||
| MVCNSDRVLK | RSAEGSNPPK | PLKKLRFDIE | GSDEADGSKH | LPGESKFQQK | ||||
| LAEMTSTRTR | MQKQKMNDSM | DTSNKEEK |
pRb ograničava sposobnost ćelije da replicira DNK, sprečavanjem njenog napredovanja iz G1 u S (faza sinteze) .[17] pRb se veže i inhibira vezivajućeg partnera za dimerizaciju proteina (E2F-DP), koji su faktori transkripcije iz porodice E2F koji uvode ćeliju u S-fazu.[18][19][20][21][22][23] Održavajući E2F-DP inaktiviranim, RB1 održava ćeliju u G1 fazi, sprječavajući napredovanje kroz ćelijski ciklus i djelujući kao supresor rasta.[8] Kompleks pRb-E2F/DP također privlači protein zvani histon-deacetilaza (HDAC) u hromatin, smanjujući transkripciju faktora koji promoviraju S fazu, dodatno suzbijajući sintezu DNK.
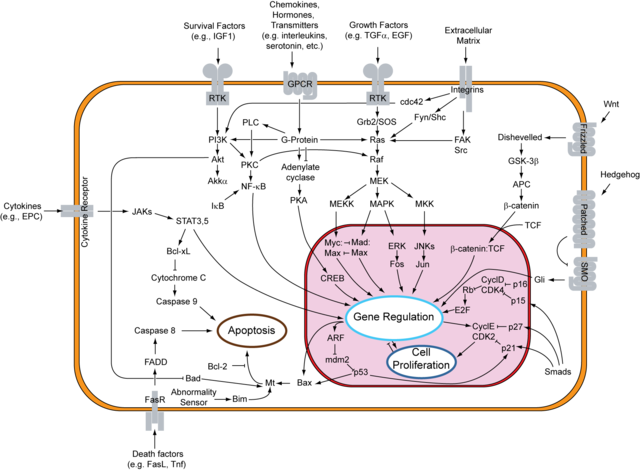
Kad dođe vrijeme za ćeliju da uđe u S fazu, kompleksi ciklin-ovisna kinaza (CDK) i ciklini fosforiliraju pRb, dopuštajući E2F-DP da se disocira od pRb i postane aktivan. Kad je E2F slobodan, aktivira faktore poput ciklina (npr. ciklin E i ciklin A), koji tjeraju ćeliju kroz ćelijski ciklus aktiviranjem kinaza ovisnih o ciklinu, i molekuli koja se naziva proliferirajući ćelijski jedarni antigen ili PCNA , koji ubrzava replikaciju DNK i nje popravak, pomažući pri vezivanju polimeraze za DNK.[24][25]
Od 1990-ih godina poznato je da je pRb inaktiviran fosforilacijom. Do tada je prevladavao model da ga je ciklin D-Cdk 4/6 progresivno fosforilirao iz nefosforiliranog u njegovo hiperfosforilirano stanje (14+ fosforilacija). Međutim, nedavno je pokazano da pRb postoji samo u tri stanja: nefosforiliran, monofosforiliran i hiperfosforiliran. Svaki ima jedinstvenu ćelijsku funkciju.[26]
Prije razvoja 2D IEF, samo se hiperfosforilirani pRb razlikovao od svih ostalih oblika, tj. nefosforilirani pRb nalikovao je monofosforiliranom pRb na imunoblotovima. Pošto je pRb bio ili u aktivnom „hipofosforiliranom“ stanju ili u neaktivnom „hiperfosforilisanom“ stanju. Međutim, s 2D IEF-om, sada je poznato da je pRb nefosforiliran u G0 i monofosforiliran u ranim G1 ćelijama, prije hiperfosforilacije, nakon restrikcijske tačke u kasnoj G1 fazi.
Tokom prijelaza M-u-G1, pRb se zatim progresivno defosforilira, pomoću PP1, vraćajući se u svoje hipofosforilirano stanje koje potiskuje rast.[8][27]
Proteini porodice pRb su komponente DREAM kompleksa, sastavljene od DP, E2F4/5, sličnih RB (p130/p107) i MuvB (Lin9: Lin37: Lin52: RbAbP4: Lin54). Kompleks DREAM sastavljen je u Go/G1 i održava mirovanje, sastavljanjem na promotorima > 800 gena ćelijskog ciklusa i posredovanjem transkripcijske represije. Sklapanje DREAM-a zahtijeva DYRK1A (Ser/Thr kinaza) zavisnu fosforilaciju jedarne komponente MuvB, Lin52 na serinu28. Ovaj mehanizam je ključan za regrutiranje p130/p107 u MuvB jedru, a time i sklopa DREAM.
Poznato je da pRb stupa u interakciju s više od 300 proteina, od kojih su neki navedeni u nastavku:
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.