五氟化鉭是一種無機化合物,化學式為TaF5,它是鉭的氟化物之一。
| 五氟化鉭 | |
|---|---|

| |
| 別名 | 氟化鉭(V) |
| 識別 | |
| CAS號 | 7783-71-3 |
| PubChem | 82218 |
| SMILES |
|
| InChI |
|
| EINECS | 232-022-3 |
| RTECS | WW5775000 |
| 性質 | |
| 化學式 | TaF5 |
| 莫耳質量 | 275.95 g/mol g·mol⁻¹ |
| 外觀 | 白色晶體[1] |
| 密度 | 4.74 g/cm3(固體) |
| 熔點 | 96.8 °C(369.9 K) |
| 沸點 | 229.2 °C(502.3 K)[2] |
| 溶解性(水) | 分解 |
| 磁化率 | +795.0·10−6 cm3/mol |
| 結構 | |
| 偶極矩 | 0 D |
| 危險性 | |
| 警示術語 | R:34 |
| 安全術語 | S:26-27-28-36/37/39-45 |
| 歐盟分類 | 未列出 |
| 主要危害 | 易生成HF |
| 閃點 | 不可燃 |
| 相關物質 | |
| 其他陰離子 | 五氯化鉭 |
| 其他陽離子 | 五氟化鈮 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
製備
五氟化鉭可由金屬鉭和氟氣在約250 °C反應得到:[3][1]
鉭和氟化氫在250~300 °C、105Pa下反應,也能得到五氟化鉭,但同時會生成三氟化鉭。[1]鉭和氟化亞錫反應,可以得到五氟化鉭:[4]
性質
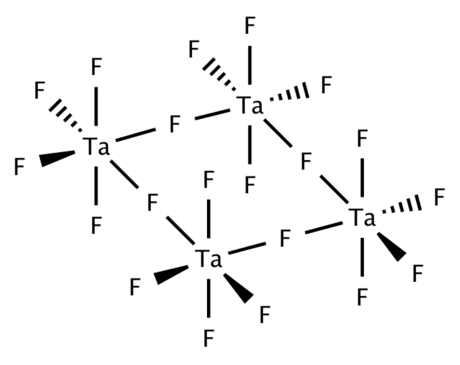
五氟化鉭在固態是四聚體,由四個TaF6中心經氟橋連接而成;氣態時為三聚體,具有D3h對稱性。[5][1]
五氟化鉭是強路易斯酸,在水中水解。[1]它可以和中性路易斯鹼(如膦、砷[6])形成加合物,它和吡啶(py)反應形成的加合物可以寫作[TaF4(py)4][TaF6][7]。它和乙醯丙酮氧鈦反應,經過[F4Ta(OTi(acac)2)2]TaF6加合物,得到二氟二乙醯丙酮鈦和三氟氧化鉭,完成鈦至鉭的氧遷移。[8]
五氟化鉭在HF水溶液中和有機陽離子共結晶,可以得到含有TaF72−、TaF83−等配陰離子的鹽。[9]它和SbF5不同,和HF形成的體系TaF5–HF在還原性環境中是穩定的。[10]
參考文獻
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.