热门问题
时间线
聊天
视角
肝素
来自维基百科,自由的百科全书
Remove ads
肝素(英文:heparin)又称普通肝素、未裂解肝素(unfractionated heparin,UFH),是一种天然且高度硫化的糖胺聚糖抗凝血剂[3][4],也是所有生物分子中阴电密度最高的分子[5],平均分子量约15,000道尔顿。肝素可用来治疗及预防深静脉血栓、肺栓塞、动脉栓塞,也可用于治疗心肌梗塞以及不稳定型心绞痛。通常以静脉注射方式给药,也可以应用在采血管以及血液透析机。[4][6]
肝素于1916年自狗的肝细胞分离而发现,故而得名[7]。使用肝素常见的副作用包括出血、注射部位疼痛以及血小板减少症,严重可导致肝素诱发的血小板减少症(HIT)。虽然肾功能不佳者在使用肝素时需要特别留意,但对于孕妇及授乳的妈妈来说肝素是相当安全的。[8]
低分子量肝素(low-molecular-weight heparin,LMWH)是平均分子量4500Da的肝素盐[9],由高分子肝素通过多种分提或解聚方法得到。
肝素已列入世界卫生组织基本药物标准清单中(能列入这个清单的,都是被认定为健康照护系统中最安全与最有效的药物)[10]。 在预防用途上,发展中国家的批发价大约是每个月9.63到 37.95 美金[11];在美国则是25到50美金[12]。另外也有低分子量的肝素[13]。
Remove ads
医疗用途

体内的嗜碱性球与肥大细胞都可以合成肝素[14] 。虽然它只能预防血栓形成,不能像组织纤溶酶原激活剂(tPA 或PLAT)一样把血栓溶解,但它可以防血栓扩大,接着体内的纤维蛋白溶解机制便可以将血栓溶解。适应症包括:
虽然肝素与低分子量肝素(包括依诺肝素、达肝素钠与锡扎肝素钠)对于预防深静脉血栓与肺栓塞都很有效[15][16],但目前的研究并未发现任何一种效果特别好[17]。
副作用
最严重的副作用是肝素诱发的血小板减少症(HIT)。肝素诱发的血小板减少症是一种免疫反应,造成血小板成为免疫反应攻击的目标,导致血小板分解、血小板减少。通常停用后症状会消失,而且可借由使用合成肝素来避免其发生。除此之外,一开始使用肝素时也会出现轻微的血小板减少症,不过不需要停用。
另外两个与出血无关的副作用是:有八成的患者在使用肝素后会出现血清转胺酶上升的现象,另外有百分之五到十的患者则会在使用肝素后出现高钾血症。使用肝素造成的血清转胺酶上升与肝功能无关,在停用后就会恢复正常;高钾血症则是因为肝素诱发了醛固酮分泌抑制所导致。长期使用肝素的患者有少数会出现脱发与骨质疏松。
对于有出血顾虑(尤其是血压控制困难、肝病、中风)的患者,严重肝病、高血压的患者不宜使用肝素[19]。
肝素的生理功能
肝素在体内的功能未知。肥大细胞合成肝素后会储存在分泌泡中,直到组织受伤时便会释出。因此,它被认为在体内可能与防御细菌与其他物质入侵有关[22]。肝素被怀疑在体内与抗凝血无关的另一个原因是,许多不具有与人类类似的凝血系统的无脊椎动物也会制造肝素。
除了可以由猪与牛的组织中萃取出制药级的肝素之外,在以下这些生物中也都曾萃取出肝素:
由于项目6-11的生物并不具有与人类类似的凝血系统,进一步支持了肝素可能与抗凝血无关的说法。
药理学
自然界的肝素是一群分子量多变的聚合物。普通肝素指的是没有将低分子量肝素分离出来的肝素,而低分子量肝素则是将低分子量部分分离出来,以使其疗效变得较为可预测。不论是普通肝素或低分子量肝素都可以在临床下使用,有些症状使用其中一种效果会比较好[36]。
肝素经由它的硫化五糖序列与酵素抑制剂抗凝血酶III结合,使其构形改变而活化[37]。 活化的抗凝血酶III接着抑制凝血酶与凝血因子Xa以及其他蛋白酶,抑制的效果可因为肝素的加入而上升一千倍[38]。硫化五糖序列如下:
GlcNAc/NS(6S)-GlcA-GlcNS(3S,6S)-IdoA(2S)-GlcNS(6S)
抗凝血酶III与肝素结合后导致的构形改变,造成它可抑制凝血因子Xa。至于凝血酶与抗凝血酶III之间的作用,除了酵素以外,还需要同时与肝素结合形成三元复合体才能达到抑制的效果;这部分肝素的高阴电性担任了重要的角色[5]。因此,至少要具有十八个糖的肝素才能与凝血酶及抗凝血酶III产生有效的作用;但是与凝血因子Xa的作用只需要硫化五糖序列就可以了[39]。 这就是为何会开发出低分子量肝素与磺达肝素(其化学结构几乎与肝素/硫酸肝素的硫化五糖序列相同)之因:低分子量肝素与磺达肝素可以只抑制凝血因子Xa而不抑制凝血酶,如此一来不仅可以微调凝血系统,达到更好的治疗效果;还能降低骨质疏松与肝素诱发的血小板减少症发生的风险。因为这两种药物只影响凝血因子Xa,在使用这两种药物时便不需进行活化性部分凝血酶时间测试(APTT)。
对于肝素诱发的血小板减少症患者,可以使用不含有肝素或肝素片段的Danaparoid:它是硫酸肝素、硫酸皮肤素与硫酸软骨素的混合物,因为不含有肝素或肝素片段,所以只有不到10%的患者出现抗体交叉反应[40]。
肝素的效果通常以活化性部分凝血激素时间测试来监测。活化性部分凝血激素时间测试是试验血浆凝固的时间,与凝血酶原时间测试不同。
Remove ads
因为肝素是个高阴电性的大分子,一般以静脉注射或皮下注射方式给药;不建议以肌肉注射方式给药,因为会造成血肿。由于普通肝素在生物体内的半衰期约为一到二小时,因此若能以点滴的方式给予效果会较佳[41]。低分子量肝素的半衰期较长,约为四到五小时;因此可以以每天一剂的方式给予[42]。在长期抗凝血剂的治疗上,肝素一般只使用到口服抗凝血剂(如:华法林)开始发挥作用即停止给药。
美国胸内科医师学会已针对肝素剂量出版临床指引[43]。
普通肝素的半衰期约为一到二小时,[41]低分子量肝素的半衰期约为四到五小时。巨噬细胞会吞噬并分解与它结合的肝素,内皮细胞则会借着与肝素的结合使其无法与抗凝血酶III发生连结。高剂量的肝素会使内皮细胞与其结合的位置出现饱和的现象;虽然肾脏也会清除肝素,但速度很慢[44],这也就是为何低剂量的肝素半衰期比高剂量短的原因。
化学

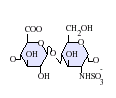
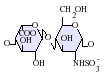
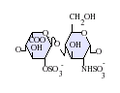
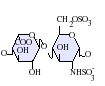
虽然大部分制药级的肝素的分子量介于 12 到 15 kDa之间,天然的肝素的分子量可以从 3 到 30 kDa[45]。肝素以及硫酸肝素都属于碳水化合物家族中的糖胺聚糖,由重复的硫化双糖单位组成[46]。在肝素中较常出现的双糖单元包括了以下这六种类型,最常见(牛肺中约占85%,猪肠黏膜则有75%)的是由 2-O-硫化艾杜糖醛酸与 6-O-硫化, N-硫化葡萄糖胺(IdoA(2S)-GlcNS(6S))所组成[47]。
极少出现的双糖单元是由含有 3-O-硫化葡萄糖胺(GlcNS(3S,6S)) 或含有胺基的葡萄糖(GlcNH3+)所组成的双糖单元。
在生理状况下,肝素的酯基与酰胺基会去质子化并吸引带正电的离子来形成盐类,制药级的肝素通常也是以盐类的方式给予。
一豪威尔单位的肝素大约等于 0.002 毫克的肝素。肝素的单位是以可以在摄氏零度下维持 1 毫升的猫血不凝固 24小时来制订的[48]。
-
GlcA-GlcNAc -
GlcA-GlcNS -
IdoA-GlcNS -
IdoA(2S)-GlcNS -
IdoA-GlcNS(6S) -
IdoA(2S)-GlcNS(6S)
- GlcA = β-D-葡萄糖醛酸
- IdoA = α-L-艾杜糖醛酸
- IdoA(2S) = 2-O-硫-α-L-艾杜糖醛酸
- GlcNAc = 2-去氧-2-乙酰氨基-α-D-吡喃葡萄糖基
- GlcNS = 2-去氧-2-乙酰氨基-α-D-吡喃葡萄糖基
- GlcNS(6S) = 2-去氧-2-乙酰氨基-α-D-吡喃葡萄糖基-6-O-硫酸盐
因为艾杜糖醛酸在寡糖内部可以以两种不同的构形存在,使肝素具有复杂的立体结构。除此之外,邻近的葡萄糖胺的硫化程度也会对构形产生影响[49]。 1993年,以核磁共振光谱仪与分子建模这两种技术,已将由六个2-去氧-2-乙酰氨基-α-D-吡喃葡萄糖基-6-O-硫酸盐-2-O-硫-α-L-艾杜糖醛酸组成的肝素立体结构解出[50] ,并得到两种模型。其一是所有的2-O-硫-α-L-艾杜糖醛酸都在 2S0 构形 (如下图 A 与 B), 第二个则是都在 1C4 构形 (如下图 C 与 D)。不过,目前没有任何证据支持单一肝素分子内所有的2-O-硫-α-L-艾杜糖醛酸都只会有一种构形。这些模型对应到蛋白质数据库代码 1HPN[51] 。
上图:
- A = 1HPN (所有的2-O-硫-α-L-艾杜糖醛酸都在 2S0 构形 )Jmol viewer
- B = A 的凡得瓦半径空间填充模型
- C = 1HPN (所有的2-O-硫-α-L-艾杜糖醛酸都在 1C4 构形 ) Jmol viewer
- D = C 的凡得瓦半径空间填充模型
在这些模型中,肝素呈现了螺旋状的构形;不论在螺旋轴任一侧,其旋转的角度都会让硫酸根以 17 埃(1.7 奈米)的间隔错开。
以化学及/或酵素将肝素解聚的技术,对于肝素或硫酸肝素的结构与功能的研究有重大的贡献。
分解肝素与硫酸肝素的酵素通常来自于土壤中的解肝磷脂土地杆菌[52]。解肝磷脂土地杆菌以肝素或硫酸肝素作为它的唯一碳源,为了分解肝素与硫酸肝素,解肝磷脂土地杆菌产生裂解酶,葡糖苷酸酶,磺基酯酶和磺酰胺酶[53] ,最常使用的是裂解酶。解肝磷脂土地杆菌共产生三种裂解酶:肝素酶 I (EC 4.2.2.7)、肝素酶 II (没有EC编号)、肝素酶 III (EC 4.2.2.8),这三个酵素的专一性详见下表: [54][55]
| 肝素酶 | 对受质的专一性(辨认的糖类序列) |
| 肝素酶 I | GlcNS(±6S)-IdoA(2S) |
| 肝素酶 II | GlcNS/Ac(±6S)-IdoA(±2S) GlcNS/Ac(±6S)-GlcA |
| 肝素酶 III | GlcNS/Ac(±6S)-GlcA/IdoA (with a preference for GlcA) |

肝素酶以β-氢消除反应机制来分解肝素与硫酸肝素,这个机制会在糖醛酸的四号碳与五号碳之间产生一个不稳定的双键[56][57]。由于这个具有不稳定双键的糖醛酸(称为 ΔUA 或 UA)会吸收232奈米紫外光,因此在实验室常用232奈米吸收的变化来监控肝素酶的反应。
在pH1.5或4之下,亚硝酸可用于肝素与硫酸肝素的化学解聚。 在这两种条件下,亚硝酸会使肝素糖链发生脱氨裂解[58]。脱氨裂解发生在GlcNS-GlcA以及GlcNS-IdoA之间,氧原子是否硫化并不受影响,不过在较高的pH值下进行反应时,速率会较慢。

在较低的pH条件下,脱氨裂解会释放出无机硫酸根与由2-去氧-2-乙酰氨基-α-D-吡喃葡萄糖基转化而成的无水甘露糖。由于组成硫化软骨素与硫化皮肤素的多糖其氮原子并未硫化,而亚硝酸无法在较低的pH条件下裂解氮未硫化的多糖,使此法可用来分辨肝素/硫酸肝素与硫化软骨素/硫化皮肤素。
临床上主要是以活化性部分凝血激素时间测试或抗凝血因子Xa活性测试等间接的方式来测试肝素是否发挥效用,而不是直接侦测肝素的存在。进行这些测试需要新鲜、未溶血以柠檬酸、氟化物或草酸盐作为抗凝血剂处理过的血浆[59][60]。
肝素的历史
肝素是在1916年威廉·亨利·豪威尔与他的学生杰·麦克莱恩在约翰·霍普金斯大学从狗的肝细胞中分离出来的,所以被命名为肝素(希腊文hepar是肝的意思,加上字尾-in)。虽然1916年就发现了肝素,不过一直到1935年才开始进行临床测试[61]。
麦克莱恩当时正在狗的肝脏组织中找寻可以促进凝血的物质,却发现了脂溶性磷脂抗凝血分子[62];豪威尔在1918年把它命名为肝素。到了1920年代初,豪威尔又分离出了一个水溶性的抗凝血分子,虽然这个分子与麦克莱恩分离出来的分子特性不同,但豪威尔还是给它同样的名字[63][64]。
到了1930年代,许多科学家都在研究肝素;其中卡罗琳学院的艾瑞克·杰普斯在1935年解出了肝素的结构[65],使瑞典的Vitrum AB药厂得以在1936年生产第一个静脉注射的肝素制剂。在1933年之前,肝素相当的昂贵且具有高毒性;在康诺特医学研究实验室(当时属于多伦多大学)以四年的时间(1933-1936)将生产肝素的制程优化后,肝素终于可以使用于生理食盐水中。肝素的第一个人体试验发生在1935年五月,到了1937年已经确定为安全、有效且容易取得的抗凝血剂了[66]。
肝素的其他功能
- 作为抗凝血剂,肝素不像乙二胺四乙酸(EDTA)会与大部分的离子结合,造成干扰;因此临床采血管与毛细管常使用锂肝素作为抗凝血剂。加入锂肝素作为抗凝血剂的采血管与毛细管以绿色贴纸与管盖标示。如需要测定锂离子浓度时,可以使用含有钠肝素的采血管(以蓝色盖子标示)。虽然肝素与EDTA相比,对血液离子浓度的测定干扰极小,但高量的肝素可能会影响到钙离子浓度[67];也曾发现肝素会干扰免疫测定。
- 使用体外循环机时会配合使用以肝素涂层的血液充氧器,借由提供接近血管内皮细胞的环境来提升整体的生物相容性与病人的生理平衡。
- 核糖核酸聚合酶的去氧核糖核酸结合位址可与肝素结合,造成它无法与基因上的启动子结合;这个特性在许多分子生物的试验上非常有用。
- 虽然使用肝素作为抗凝血剂所采取的血,可以由其中的白血球取得足够的DNA来进行聚合酶链反应;但研究者也发现即使是微量的肝素(每50 μL 0.002单位),还是会干扰聚合酶链反应的进行[68]。
关于肝素的社会与文化议题
相比于完全由化学合成的治疗药剂,由动物来源萃取纯化的肝素潜在的不纯物当然多得多了:包括病毒、细菌的内毒素、普利昂蛋白、脂肪、蛋白质与去氧核糖核酸都有可能出现在其中;而纯化过程中所使用的溶剂、重金属以及离子等也不无可能成为污染物。虽然这样说,但过去已经建立了许多方法来将不纯物/污染物含量尽可能的降低,这些方法也都详列于药典中。目前分析肝素的污染物最大的困难,首推如何鉴定如硫化皮肤素(DS,一名硫化软骨素B)这类结构与肝素类似的污染物。硫化皮肤素由N-乙酰-半乳糖胺(GalN)与糖醛酸以1→3连结所组成的双糖形成,双糖之间以1→4形式相连。糖醛酸部分可能为葡萄糖醛酸、艾杜糖醛酸、2-O-硫-α-L-艾杜糖醛酸,六碳糖的部分除了乙酰半乳糖胺以外,也有可能在四号碳及/或六号碳的位置硫化(Gal- NAc4S, GalNAc6S, 或 GalNAc4S6S)。艾杜糖醛酸的存在使硫化皮肤素与硫化软骨素A与C不同,但却使它与肝素较为相似,但比肝素的阴电密度要低。通常在肝素中大约有1-7%的硫化皮肤素,但它们不具有肝素的生物活性[69]。
2007年12月,美国食品药品监督管理局发现有一批肝素制剂遭到粘质沙雷氏菌污染而全面回收。粘质沙雷氏菌感染严重可致死[70]。
2008年三月,美国食品药物监督管理局发现由中国进口的一批肝素遭到硫化软骨素污染,并造成81人死亡,宣布全面回收[71][72]。这些硫化软骨素是一般硫化软骨素的“过度硫化”型态,原本适用于关节炎的治疗,但却被加到肝素里面企图蒙混过活性测试[73]。
2008年三月,药厂因为未知的污染宣布召回一批来自中国的肝素[74][75]。后来发现这些肝素遭到“过度硫化”的硫化软骨素污染[76],美国食品药物监督管理局宣布至少有十九个人因此死亡,另外还有785人因为使用了这些污染的肝素,造成呼吸困难、恶心、呕吐、大量流汗、血压急速下降甚至休克等症状。
一名任职于雪松-西奈医疗中心的护理师在2007年错误地注射了成人剂量(约为婴儿剂量的1000倍)的肝素到丹尼斯‧奎德12天大的双胞胎体内[78]。因为药厂(百特国际)提供的成人与婴儿包装的肝素外表相似,奎德家族虽然与医院以75万美金和解[79],但仍决定对百特国际提告[80][81]。在奎德家族的不幸事件发生之前,已经有六个在印第安纳波利斯的卫理公会医院的婴儿也被错误地注射了成人剂量,并造成三人死亡[82]。
2008年7月,在德州圣体市的 Christus Spohn 医院出生的双胞胎,因为医院药局出错被注射了过量的肝素而死[83],目前该案件仍在调查[84][85]。2010年3月,来自德州的一名两岁的器官移植病人在内布拉斯加大学医学中心因被注射了致死剂量的肝素而死,该案目前也仍在调查[86]。
制药级的肝素是从屠宰动物的黏膜(如猪肠或牛肺)纯化而来[87]。全合成肝素的技术正持续地研发[88],以化学酶法工艺从双糖合成低分子量肝素的方法已在2011年被研发出来[89]。
肝素除了作为抗凝血剂之外,将类似肝素的结构开发为药剂的潜力也不容忽视。肝素潜在的用途如下表所示[90][91]:
| 对肝素敏感的疾病!!目前肝素在实验模型上的效果 !! 临床状态 | ||
| 艾滋病 | 降低培养的T淋巴球对第一型与第二型人类免疫缺乏病毒的吸收[92]。 | - |
| 急性呼吸窘迫症候群 | 在动物模型中,肝素可以降低呼吸道中细胞的活化与聚集、中和对细胞有毒的细胞产物、提升肺部功能。 | 对照临床试验 |
| 过敏性脑脊髓炎 | 在动物模型中有疗效。 | - |
| 过敏性鼻炎 | 虽然对成人呼吸窘迫症候群有疗效,但在鼻炎中没有被测试过。 | 对照临床试验 |
| 关节炎 | 可抑制细胞聚集、胶原蛋白受损与血管增生。 | 轶事证据 |
| 哮喘 | 如成人呼吸窘迫症候群的发现,在实验动物中发现肝素对提升肺部功能有帮助。 | 对照临床试验 |
| 癌症 | 在动物模型中,肝素可以抑制癌的生长、远端转移、血管新生,从而提升存活时间。 | 一些轶事证据 |
| 第四型过敏反应 | 在动物模型中有疗效。 | - |
| 炎症性肠病 | 抑制发炎细胞运输。 | 对照临床试验 |
| 间质性膀胱炎 | 在人类的实验中可以抑制间质性膀胱炎。 | 已在临床使用 |
| 移植排斥 | 在动物模型中,肝素可以延长异体移植器官寿命。 | - |
- 表示没有资讯可参考。
由于研究发现肝素对许多疾病都可能会有疗效,目前已有一些在结构上与肝素类似的新药物正在开发中[90],如下表所示:
| 药物分子!!新药与肝素比较 !! 生物活性 | ||
| 肝素四糖 | 非抗凝血剂、不具抗原性、可口服 | 抗过敏剂 |
| 戊聚糖多硫酸盐 | 由植物分子衍生而来、微小抗凝血活性、抗发炎、可口服 | 抗发炎、抗黏着、抗远端转移 |
| 磷酸戊糖甘露糖硫酸盐 | 抑制肝素酶活性的有效抑制剂 | 抗远端转移、抗血管新生、抗发炎 |
| 化学选择性O-去硫肝素 | 不具抗凝血活性 | 抗发炎、抗过敏、抗黏着 |
参考文献
延伸阅读
外部链接
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads