| 薁 | |
|---|---|

| |

| |
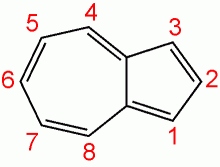
| IUPAC名 Azulene | |
| 系統名 bicyclo[5.3.0]decapentaene Azulene[1] 雙環[5.3.0]癸五烯 | |
| 別名 | 藍烴、甘菊環 |
| 識別 | |
| CAS號 | 275-51-4 |
| PubChem | 9231 |
| ChemSpider | 8876 |
| SMILES |
|
| InChI |
|
| InChIKey | CUFNKYGDVFVPHO-UHFFFAOYAT |
| EINECS | 205-993-6 |
| ChEBI | 31249 |
| RTECS | CO4570000 |
| KEGG | C13392 |
| 性質 | |
| 化學式 | C10H8 |
| 摩爾質量 | 128.17 g·mol⁻¹ |
| 外觀 | 青藍色片狀晶體[2] |
| 氣味 | 無[3] |
| 密度 | 1.037 g/cm3 |
| 熔點 | 99 °C(372 K)([2]) |
| 沸點 | 242 °C(515 K)([5]) |
| 溶解性(水) | 幾乎不溶[3] |
| 溶解性 | 可溶於有機溶劑[3] |
| 磁化率 | -98.5·10−6 cm3/mol[4] |
| 熱力學 | |
| ΔcHm⦵ | −1266.5 kcal/mol[6] |
| 危險性 | |
| 警示術語 | R:R51/53 |
| 安全術語 | S:S61 |
| 歐盟分類 | |
| 主要危害 | 有毒 |
| 閃點 | 76.66 °C |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
化學性質


薁是一種含有七元環與五元環的稠環芳烴。和萘相似,薁分子中含有10個π電子的共振結構,但是其共振穩定能只有萘的一半。薁可看做由環庚三烯正離子(䓬離子)和環戊二烯負離子構成,因此薁分子具有約1.08D的電偶極矩。[8]由於極性,薁的五元環一側容易發生親電取代反應,七元環一側容易發生親核取代反應。薁的芳香性略低於萘,更容易加氫生成環戊烷並環庚烷。
薁在基態的極性反映在它的深色上,這對於小的不飽和芳族化合物來說是不尋常的。[9]薁不符合卡莎規則,其許多衍生物也都不會在最低激發態發出熒光。[10]
合成
由於薁的特殊結構,科學家一直關注其合成方法。[11]1939年,科學家St. Pfau和Plattner用茚滿和重氮乙酸乙酯首次人工合成薁。[12]
有效的薁一鍋法涉及了環戊二烯與不飽和的C5合成子的環化。[13]環庚三烯前體的替代方法早已為人所知,下面顯示了一種說明性方法。[14][15]

步驟:
薁配合物
在有機金屬化學中,薁可作為低價金屬中心的配體,其配合物包括 (azulene)Mo2(CO)6和(azulene)Fe2(CO)5。[16]
相關化合物
1-羥基薁是不穩定的綠色油狀液體,沒有酮-烯醇互變異構。[17]穩定的2-羥基薁可以由2-甲氧基薁和氫溴酸反應而成,有酮-烯醇互變異構。[18]它的酸性比苯酚和萘酚強,在水中的pKa為8.71。6-羥基薁的酸性更強,在水中的 pKa為7.38。[18]
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.