Loading AI tools
化合物 来自维基百科,自由的百科全书
三硫化二砷是一種無機化合物,化學式為As2S3。三硫化二砷在自然界以雌黃礦物的形式存在。[1]
| 三硫化二砷 | |
|---|---|

| |
| |
| IUPAC名 Arsenic trisulfide | |
| 別名 | 硫化砷(III)、雌黃 |
| 識別 | |
| CAS號 | 1303-33-9 |
| PubChem | 4093503 |
| ChemSpider | 21241348 |
| SMILES |
|
| InChI |
|
| InChIKey | OUFDYFBZNDIAPD-UHFFFAOYAM |
| EINECS | 215-117-4 |
| RTECS | CG2638000 |
| 性質 | |
| 化學式 | As2S3 |
| 摩爾質量 | 246.04 g·mol−1 |
| 外觀 | 橙色晶體 |
| 密度 | 3.43 g cm−3 |
| 熔點 | 310 °C(583 K) |
| 沸點 | 707 °C(980 K) |
| 結構 | |
| 空間群 | P21/n (No. 11) |
| 晶格常數 | a = 1147.5(5) pm, b = 957.7(4) pm, c = 425.6(2) pm |
| 晶格常數 | α = 90°, β = 90.68(8)°, γ = 90° |
| 配位幾何 | As:角錐型 |
| 危險性 | |
| H-術語 | H300, H331, H400, H411 |
| NFPA 704 | |
| PEL | [1910.1018] TWA 0.010 mg/m3 |
| 相關物質 | |
| 其他陰離子 | 三氧化二砷 三硒化二砷 |
| 其他陽離子 | 三硫化二磷 硫化銻 硫化鉍 |
| 相關化學品 | 四硫化四砷 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
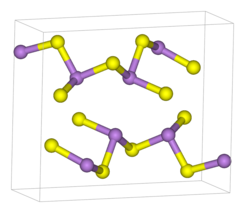
三硫化二砷存在晶體和無定形體。[2]單斜的As2S3是層狀結構,每個As和3個S成鍵,As-S為224pm,∠S-As-S 99°;而其蒸氣以二聚體As4S6的形式存在,結構與As4O6類似。[3]
三硫化二砷可由單質化合得到,或者從As(III)的溶液中由H2S沉澱。[5]
它可以被硫化鈉轉化為三硫代亞砷酸鈉,被多硫化鈉轉化為四硫代砷酸鈉:
而在和氫氧化鈉溶液的反應中,會同時產生亞砷酸鹽和硫代亞砷酸鹽:
此溶液在經過脫硫、還原等操作可以製得三氧化二砷。[6]當溶液中OH-不足時,則產生偏亞砷酸鹽和硫代偏亞砷酸鹽:[7]
和碳酸鈉溶液反應,得到同樣的砷化合物:
和氯化亞銅、氯化銀等金屬氯化物共熱,均會產生三氯化砷:[7]
As2S3不溶於水,因此毒性低。 老化的樣品中可能含有大量的砷氧化物,這些氧化物是可溶的,因此具有劇毒。
在火山環境中發現了雌黃,通常與其他硫化砷(主要是雄黃)一起被發現。 有時會在低溫熱液脈中發現它,以及一些其他硫化物和亞硫酸鹽礦物。
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.