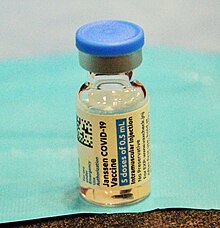
强生2019冠状病毒病疫苗(英语:Johnson & Johnson COVID-19 vaccine,简称强生疫苗)是由位于荷兰莱顿的杨森疫苗[12]及其比利时母公司同时也是美国强生公司子公司杨森制药(Janssen Pharmaceutica)[13]研发的2019冠状病毒病疫苗[14][15]。
它是一种基于人类腺病毒的病毒载体疫苗,人类腺病毒经过改造后会含有能产生严重急性呼吸系统综合征冠状病毒2刺突蛋白的基因[3]。人体的免疫系统会对这种刺突蛋白产生反应并产生抗体[16]。人类只需注射一剂该疫苗,且该疫苗仅需在摄氏2至8度冷藏,不用冷冻保存 [17][18]。
该疫苗的临床试验于2020年6月开始,三期试验涉及约4.3万人[10]。2021年1月29日,杨森公司宣布,在疫苗接种28天后,该疫苗预防2019冠状病毒病的有效率为66%,预防重症2019冠状病毒病的有效率为85%[19][20][21],预防2019冠状病毒病引起的住院或死亡的有效率为100%[1]。
该疫苗于2021年2月27日获得美国食品药品监督管理局的紧急使用授权,2021年3月11日获得欧洲药品管理局的有条件上市授权[22][23]。各国也在加紧疫苗接种。
疫苗简介
强生2019冠状病毒病疫苗采用与卫星V疫苗、阿斯利康疫苗相似的技术。疫苗采用人类腺病毒为载体,与卫星V疫苗更为相似,但根据一期临床试验,其效果可能较差[24]。疫苗由无复制能力的重组腺病毒26型(Ad26)载体组成,该载体包含严重急性呼吸系统综合症冠状病毒2的刺突(S)蛋白[25][4]。
美国国家过敏和传染病研究所疫苗研究中心和德州大学奥斯汀分校的研究人员开发了刺突蛋白的稳定版本,其中包括两个突变,其中普通氨基酸被脯氨酸取代[26][27][28]。该疫苗的非活性成分为:柠檬酸一水合物、柠檬酸三钠二水合物、乙醇、2-羟丙基-β-环糊精(HBCD)(羟丙基βdex)聚山梨酸酯80、氯化钠、氢氧化钠和盐酸[25][1]。
疫苗可在冰箱中冷藏保存数月时间[29][30][31]。与辉瑞疫苗、莫德纳疫苗不同的是,强生疫苗采用单针接种程序,且无需冷冻运输[32][17]。每瓶疫苗含五剂[18]。
不良反应
该疫苗主要的不良反应包括注射部位的疼痛、头痛、疲劳、肌肉酸痛和恶心[10][33]。这些不良反应大多数在接种疫苗后1至2天内发生,轻度至中度的不良反应则持续1至2天[33][34]。
根据8例六十岁以下接种者血栓与低血小板病例,欧洲药品管理局4月20日称强生疫苗与罕见血栓形成之间有“可能的联系”,但总体而言接种仍然利大于弊。[35]
2021年5月,美国有研究显示抗凝血药“比伐卢定”(Bivalirudin)可以有效治疗接种强生疫苗后出现罕见血栓的人士[36]。
研发历史

2019冠状病毒病疫情期间,强生公司与美国卫生及公共服务部应急管理办公室生物医学高级研究与发展局合作,以非盈利性原则研发疫苗[37][38]。强生公司表示,其疫苗项目将“处于非营利水平”,因为该公司将其视为“以最快最好的方式找到世界上所有合作,来实现这一目标”[39]。
杨森疫苗公司则与贝斯以色列女执事医疗中心合作,根据用于生产埃博拉疫苗的相同技术,负责开发候选疫苗[15][40][41]。
2020年6月,强生公司和美国国家过敏和传染病研究所确认,计划于2020年9月开始该疫苗的临床试验,并可能进行一、二a期人类临床试验。试验工作从7月下半月开始加速发展[43][44][45]。
一、二a期试验自2020年7月15日招募首位受试者开始,并在比利时和美国招募了研究参与者[46]。一、二a期试验的中期结果确定了疫苗的安全性、反应原性和免疫原性。根据报告,注射一剂疫苗后的29天内,可确保90%的参与者具有中和病毒所需的足够抗体。在57天后,所有参与者全部具有抗体[47][48]。
三期临床试验命名为“ENSEMBLE”,于2020年9月开始招募,并于2020年12月17日完成招募。此次临床试验是随机、双盲、安慰剂对照的试验,旨在与18岁及以上成年人的安慰剂相比,评估单剂量疫苗的安全性和有效性。研究参与者在第一天接受疫苗的单次肌肉注射,剂量为5×1010病毒颗粒[49]。但因一名志愿者出现不良反应,试验于10月12日暂停。试验在11天后恢复[50]。2021年1月29日,杨森从此次临床试验数据的中期分析中公布安全性和有效性数据。该数据表明,该疫苗在所有志愿者中预防接种后28天内,重度COVID-19疾病预防有效率为66%。中期分析则是基于阿根廷、巴西、智利、哥伦比亚、墨西哥、秘鲁、南非和美国的43783名成年志愿者中的468例COVID-19征候病例。在疫苗试验组中,没有与COVID-19相关的死亡个案,而在安慰剂组中,有5例与COVID-19相关的死亡个案。在试验期间,所有参与者未观察到过敏反应[51]。
第二次三期临床试验于2020年11月12日开始招募。第二次三期临床试验与第一次的不同之处在于,其研究参与者将分别接受两次肌内注射,分别在第1天和第57天[52]。
生产
2020年4月,强生公司与Catalent建立合作关系,以在Catalent位于印第安纳州布卢明顿的工厂大规模生产疫苗[54]。2020年7月,合作关系扩大到包括Catalent在意大利阿纳尼的工厂[55]。
2020年7月,强生承诺向美国提供多达3亿剂疫苗,其中1亿剂为前期供应,另外还包括2,000万剂作为后期选择。此次交易总价值超过10亿美元,由生物医学高级研究与开发局和美国国防部资助[56][57]。同年8月5日,双方确认交易[58]。
2020年9月,Grand River无菌制造公司与强生公司达成协议,将在密歇根州大急流城的工厂支持疫苗的制造,包括技术转让以及灌装和精加工制造[59]。
2020年12月,强生公司与西班牙Reig Jofre制药公司达成协议,将在Reig Jofre的巴塞罗那工厂生产疫苗[60]。一旦欧洲药品管理局在2021年3月之前批准该疫苗,强生公司可能会从2021年4月开始,向欧盟各成员国提供疫苗[61][62]。从2021年第二季度开始,该工厂将每年生产5000万剂疫苗[63]。
2020年8月,强生与美国联邦政府签署了一项价值10亿美元的合同,同意在疫苗获得美国食品和药物管理局的批准或紧急使用授权后,向美国提供1亿剂疫苗[57]。根据与美国政府达成的协议,强生的目标是到2021年2月底生产1200万剂,到2021年4月底生产超过6000万剂,到2021年6月底生产超过1亿剂。然而,强生公司在2021年1月承认,由于生产方面的延迟,可能会阻止其履行2月底之前交付给美国的1200万剂的合同[64]。2021年2月,强生公司高管在美国国会作证。但强生公司表示,该公司可以在3月底之前向美国政府交付2千万剂,在2021年上半年交付1亿剂[65]。
2021年2月,赛诺菲与强生公司达成一项协议,要求赛诺菲在法国Marcy-l'Étoile工厂提供支持和基础设施。一旦赛诺菲获得授权,赛诺菲每月可生产约1200万剂强生疫苗[66]。
2021年3月,默克公司和强生公司达成一项交易,要求默克公司在美国的两个工厂生产强生疫苗,以根据《国防生产法》的规定帮助扩大疫苗的生产能力[67]。同月,在巴尔的摩新兴生物科技公司运营的一家工厂发生人为失误,由于员工弄混药剂成分,导致多达1500万剂强生疫苗变质及报废[68]。强生公司3月31日向媒体证实,这家工厂生产的某批次强生疫苗“质量不达标”,涉事疫苗处于试生产阶段,该厂所产强生疫苗尚未获美国食品和药物管理局批准投用于美国市场[69]。
2021年6月,美国食品药品监督管理局表示,Emergent BioSolutions Inc在巴尔的摩工厂生产的强生疫苗发生操作错误,混淆了强生和阿斯利康的生产成分后,4月被FDA下令暂停生产,这导致多个批次的强生疫苗无法使用。该机构和厂家都未透露损失疫苗的具体数字。《纽约时报》援引知情人士透露,可能有6000万剂疫苗受到波及。欧盟表示,强生公司很可能不会在预定的6月底之前向欧盟运送5500万剂疫苗[70]。南非监管机构宣布,南非将不会分发使用该批次的疫苗,正与强生公司商量换货[71]。
获批与供应
2020年12月1日开始,该候选疫苗的临床试验已经由欧洲药品管理局人用药品委员会进行“滚动审查”,以加快对预期的有条件销售许可申请[61][72]。2021年2月16日,杨森向欧洲药品管理局申请该疫苗的有条件销售许可[3]。2021年3月11日,欧盟委员会批准疫苗上市[7][22]。该疫苗计划于4月下半月开始发货,杨森亦承诺到2021年将向欧盟运送至少2亿剂疫苗[73]。
2021年4月9日,欧洲药品管理局表示,在发现4起接种强生疫苗后出现与低血小板有关的严重罕见血栓案例,其中一人死亡。欧洲药品管理局表示当局正在审查接种强生疫苗后出现的血栓案例[74]。4月13日,强生宣布将延后在欧洲推出疫苗[75]。
2021年4月14日,瑞典卫生局宣布,将暂缓开始使用强生疫苗接种的打算。法国表示将继续为55岁以上的人接种强生疫苗[76]。
4月20日,强生公司宣布重启其在欧洲的接种活动,而欧洲药品管理局建议在其标签上加注安全警示标语[77]。欧洲药品管理局表示,该疫苗可能与罕见类型的血栓病例有关联,但是该疫苗的益处要大于风险[78]。
5月3日,丹麦国家卫生局宣布停止接种强生2019冠状病毒病疫苗,丹麦卫生局认为接种强生疫苗的益处未必大于风险[79]。
2021年2月4日,杨森生物技术公司向美国食品药品监督管理局申请紧急使用授权。美国食药监局宣布,疫苗和相关生物产品咨询委员会将于2月26日开会审议该申请[29][32][80][81]。强生公司宣布,计划在获得紧急使用授权后立即发货[51]。2月24日,在疫苗和相关生物产品咨询委员会召开会议之前,发布了杨森和美国食药监局的简报文件。美国食药监局文件建议授予疫苗的紧急使用授权,其结论是疫苗的临床试验结果和安全性数据与美国食药监局针对COVID-19疫苗的紧急使用授权指南一致[82][83][25][84]。2月26日,疫苗和相关生物产品咨询委员会成员就此进行投票,最终以22票(全票赞成)的结果,建议为该疫苗授予紧急使用授权[85]。翌日,美国食药监局授予疫苗的紧急使用授权[10][11][86]。2月28日,美国疾病控制与预防中心免疫实践咨询委员会(ACIP)建议为18岁以上的人群使用该疫苗[87][23],并于翌日起开始应用于美国2019冠状病毒病疫苗接种计划。
2021年4月初,美国国内多地发生了接种该款疫苗后出现头晕、呼吸急促等不良反应状况。其后佐治亚州、科罗拉多州以及北卡罗来纳州的部分地区已宣布暂停接种强生疫苗[88]。
2021年4月13日,美国疾病控制与预防中心和美国食品药品监督管理局宣布,他们将调查6例极其罕见的在注射疫苗后出现的脑静脉窦血栓形成病例,并建议暂停接种强生疫苗。6名病例中有一名妇女已经死亡,另有一名妇女紧急住院。[89][90][91]截至4月23日,美国有15人在接种强生新冠疫苗后出现严重血栓,其中3人死亡[92]。当天,美国疾控控制与预防中心免疫实践咨询委员会建议应当在美国恢复使用强生疫苗[93]。在暂停11天接种疫苗后的4月24日,美国疾控控制与预防中心与部分州属如印第安纳州、纽约州、弗吉尼亚州、密苏里州和密歇根州恢复使用强生疫苗[94]。
2021年2月11日,圣文森特和格林纳丁斯政府授予强生疫苗的紧急使用授权[95]。
2020年12月,强生与GAVI疫苗联盟原则上签署了一项协议,以支持COVAX计划。2021年2月19日,强生公司向世界卫生组织提交其“紧急使用清单”的正式请求和数据包;而参加COVAX的要求则是EUL。强生公司预计到2022年将为COVAX提供多达5亿剂的疫苗[96][30][97]。
2021年2月25日,巴林授权疫苗的紧急使用[98][99]。
2021年2月26日,韩国食品及药品安全处开始审查强生公司的疫苗批准申请[100]。
2020年11月下旬,强生公司向加拿大卫生部提交滚动审核申请,以批准其疫苗[101]。加拿大政府已与强生公司签订了供应1000万剂疫苗的订单,强生亦拥有再购买2800万剂疫苗的权利。2021年3月5日,该疫苗成为第四个获得加拿大卫生部批准使用的疫苗[102]。
2021年2月,该疫苗在南非获得紧急授权[103][104][105]。同年4月,南非暂停使用该疫苗[106]。南非在4月28日恢复为医护人员接种强生疫苗[107]。
2021年3月底,该疫苗在哥伦比亚获得紧急授权[108]。
2021年4月,澳大利亚政府表示,将不会购买强生疫苗,并强调“目前不打算再购买任何腺病毒疫苗”[109][110]。
2021年5月27日,台湾的宗教团体国际佛光会发函给中央流行疫情指挥中心,申请输入50万剂强生疫苗捐赠给政府供医护及神职人员接种,不过之后娇生公司表示仅会直接与政府洽谈疫苗采购,不透过第三方[111]。
2021年5月28日,英国政府向强生疫苗批出紧急使用许可,而该等疫苗将于英国2019冠状病毒病疫苗接种计划中应用[112]。
2021年6月13日,韩国大邱市一名38岁市民在接种强生疫苗三天后死亡,这是韩国报告的首例强生疫苗接种者死亡案例,卫生部门将着手调查死因[113]。
争议
美国天主教主教团表示,对强生疫苗表达“道德关切”。美国天主教主教会议和新奥尔良等多个教区先后发声明,指强生使用流产胎儿的细胞生产疫苗,已经受“道德污染”,注射疫苗等同在道德上妥协,呼吁信徒在有选择情况下,应尽量接种其他疫苗[114][115][116][117]。教宗方济各则认为这类疫苗“在道德上是可以接受的”[116][118][114]。另外美国康涅狄格州哈特福德大主教(Archbishop of Hartford)和其他当地神职人员在一份声明中宣布,所有居民“应该凭良心自由地接种目前可用的疫苗……为了自己的健康和公共利益”[114]。而强生公司其后发表声明,否认有关说法,指疫苗中没有流产胎儿组织细胞[115]。
参考资料
外部链接
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.