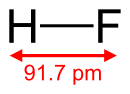
Hydro fluoride
From Wikipedia, the free encyclopedia
Hydro fluoride là một hợp chất hóa học với công thức hoá học HF. Loại khí hoặc chất lỏng không màu này là nguồn fluor công nghiệp chính, thường là dung dịch nước gọi là acid hydrofluoric. Đây là một nguyên liệu quan trọng trong việc chế biến nhiều hợp chất quan trọng bao gồm dược phẩm và polyme (ví dụ như Tefluorn). HF được sử dụng rộng rãi trong ngành công nghiệp hoá dầu như là một thành phần của các chất siêu acid. Hydro fluoride sôi ở nhiệt độ phòng, cao hơn nhiều so với các hydro halide khác. Không giống như các hydro halide khác, HF nhẹ hơn không khí.
| Hydro fluoride | |||
|---|---|---|---|
| |||
 | |||
| Tên khác | Fluoran | ||
| Nhận dạng | |||
| Số CAS | 7664-39-3 | ||
| PubChem | 16211014 | ||
| KEGG | C16487 | ||
| ChEBI | 29228 | ||
| Số RTECS | MW7875000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | RGL5YE86CZ | ||
| Thuộc tính | |||
| Công thức phân tử | HF | ||
| Khối lượng mol | 20,00634 g/mol | ||
| Bề ngoài | khí hoặc chất lỏng không màu (dưới 19.5°C) | ||
| Khối lượng riêng | 1,15 g/L, gas (25 °C) 0.99 g/mL, liquid (19.5 °C) | ||
| Điểm nóng chảy | −83,6 °C (189,6 K; −118,5 °F) | ||
| Điểm sôi | 19,5 °C (292,6 K; 67,1 °F) | ||
| Độ hòa tan trong nước | miscible | ||
| Áp suất hơi | 783 mmHg (20 °C) | ||
| Độ axit (pKa) | 3.17[1][2] | ||
| Chiết suất (nD) | 1,00001 | ||
| Cấu trúc | |||
| Hình dạng phân tử | Linear | ||
| Mômen lưỡng cực | 1.86 D | ||
| Nhiệt hóa học | |||
| Enthalpy hình thành ΔfH | −13,66 kJ/g (gas) −14.99 kJ/g (liquid) | ||
| Entropy mol tiêu chuẩn S | 8,687 J/g K (gas) | ||
| Các nguy hiểm | |||
| NFPA 704 |
| ||
| PEL | TWA 3 ppm | ||
| LC50 | 1276 ppm (rat, 1 hr) 1774 ppm (monkey, 1 hr) 4327 ppm (guinea pig, 15 min)[3] | ||
| REL | TWA 3 ppm (2.5 mg/m³) C 6 ppm (5 mg/m³) [15-minute] | ||
| IDLH | 30 ppm | ||
| Các hợp chất liên quan | |||
| Anion khác | Hydro chloride Hydro bromide Hydro iodide Hydrogen astatide | ||
| Cation khác | Natri fluoride Kali fluoride Rubidi fluoride Caesi fluoride | ||
| Hợp chất liên quan | Nước Ammonia | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Hydro fluoride là một loại khí nguy hiểm, tạo thành acid hydrofluoric ăn mòn và xâm nhập khi tiếp xúc với độ ẩm. Loại khí này cũng có thể gây ra chứng mù do sự hủy hoại nhanh chóng của giác mạc.
Nhà hoá học người Pháp Edmond Frémy (1814-1894) được cho là đã phát hiện ra hydro fluoride khan trong khi cố gắng cô lập fluor. Mặc dù Carl Wilhelm Scheele chuẩn bị acid hydrofluoric với số lượng lớn vào năm 1771, acid này đã được biết đến trong ngành công nghiệp thủy tinh trước đó.