Loading AI tools
З Вікіпедії, вільної енциклопедії
Анестезі́я (грец. αν — не, та грец. αισθησις — відчуття; знеболювання) — це стан контрольованої, тимчасової втрати відчуття або свідомості, викликаний у медичних або ветеринарних цілях. Може включати часткову або повну аналгезію[en] (полегшення або запобігання болю), параліч (розслаблення м'язів), амнезію (втрату пам'яті) і втрату свідомості[en]. Особа під дією анестетичних препаратів називається анестезованою.
| Анестезія | |
|---|---|
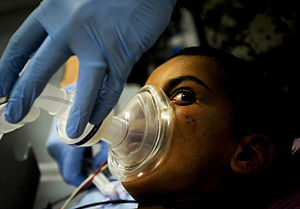 Дитину готують до анестезії | |
| MeSH | E03.155 |
| MedlinePlus | anesthesia |
| eMedicine | 1271543 |

Також, у неврології один із симптомів захворювання.
Анестезія дозволяє безболісно виконувати процедури, які в іншому випадку вимагали б фізичного знерухомлення[en] для не анестезованої особи або були б технічно нездійсненними. Існує три широкі категорії анестезії:
Готуючись до медичної або ветеринарної процедури, медичний працівник обирає один або кілька препаратів для досягнення типу і ступеня анестезії, що відповідають типу процедури та конкретному пацієнту. Використовувані типи препаратів включають загальні анестетики[en], місцеві анестетики, снодійно-седативні засоби, дисоціативні речовини, суто седативні засоби, ад'юванти, нервово-м'язові блокатори[en], наркотики та анальгетики.
Ризики ускладнень під час або після анестезії часто важко відокремити від ускладнень процедури, для якої використовується анестезія, але в основному вони пов'язані з трьома факторами: здоров'ям людини, складністю та стресом самої процедури і методом анестезії. З цих факторів найбільший вплив має здоров'я людини. Серйозні періопераційні ризики можуть включати смерть, серцевий напад і емболію легеневої артерії, тоді як незначні ризики можуть включати післяопераційну нудоту і блювання та повторну госпіталізацію[en]. Деякі стани, як-от токсичність місцевої анестезії, травма дихальних шляхів[en] або злоякісна гіпертермія, можна більш прямо віднести до конкретних анестезуючих препаратів і методів.
Мета анестезії може бути зведена до трьох основних цілей або бажаних ефектів[1]:
Різні типи анестезії мають різні бажані ефекти. Місцева анестезія, наприклад, впливає на аналгезію; седативні засоби бензодіазепінового типу (використовуються для седації або «сутінкової анестезії[en]») сприяють амнезії; а загальні анестетики можуть досягати всіх типів бажаних ефектів. Метою анестезії є досягнення бажаного ефекту, необхідного для даної хірургічної процедури, з найменшим ризиком для суб'єкта процедури.

Для досягнення цілей анестезії препарати діють на різні, але взаємопов'язані відділи нервової системи. Гіпноз, наприклад, створюється шляхом впливу на ядра в мозку і схожий на активацію сну. В результаті люди стають менш свідомими та менше реагують на шкідливі подразники[en][1].
Втрата пам'яті (амнезія) виникає внаслідок дії препаратів на кілька (але специфічних) ділянок мозку. Спогади створюються як декларативні або недекларативні в кілька етапів (короткочасний, довготривалий[en], тривалий) міцність яких визначається міцністю зв'язків між нейронами, що називається синаптичною пластичністю[1]. Кожен анестетик викликає амнезію завдяки унікальному впливу на формування пам'яті у різних дозах. Інгаляційні анестетики[en] надійно викликають амнезію через загальне пригнічення ядер у дозах, нижчих від необхідних для втрати свідомості. Такі препарати, як мідазолам, викликають амнезію різними шляхами, блокуючи формування довгострокових спогадів[1].
Тим не менш, людина може бачити сновидіння під час анестезії або усвідомлювати процедуру, не проявляючи жодних ознак цього. Підраховано, що 22 % людей бачать сновидіння під час загальної анестезії і в 1–2 випадках на 1000 мають певну свідомість, що називається «усвідомленням під час загальної анестезії»[1]. Невідомо, чи бачать сни тварини, під час загальної анестезії.
Анестезія унікальна тим, що вона не є прямим засобом лікування; скоріше вона дозволяє медичному працівнику виконувати процедури діагностування, полегшення симптомів або лікування, які в іншому випадку були б болючими або складними. Таким чином, найкращим анестетиком є той, який має найменший ризик для пацієнта, але досягає бажаного ефекту, необхідного для завершення процедури. Першим етапом анестезії є передопераційна оцінка ризику, яка складається з медичної історії, фізичного огляду та лабораторних досліджень. Діагностика передопераційного фізичного стану пацієнта дозволяє мінімізувати ризики анестезії. Правильно складена історія хвороби дозволяє поставити правильний діагноз у 56 % випадків, це значення збільшується до 73 % після фізичного огляду. Лабораторні тести допомагають поставити діагноз, але лише в 3 % випадків, що підкреслює необхідність повного збору анамнезу та фізичного огляду перед анестезією. Неправильна передопераційна оцінка або підготовка є основною причиною 11 % усіх несприятливих подій, пов'язаних з анестезією[1].
Безпечна анестезіологічна допомога значною мірою залежить від добре функціонуючої групи висококваліфікованих медичних працівників. Медична спеціальність, зосереджена навколо анестезії, називається анестезіологією, а лікарі, які спеціалізуються в цій галузі, називаються анестезіологами[2]. Додаткові медичні працівники, залучені до надання анестезії, мають різні посади та ролі залежно від юрисдикції, і включають періопераційних медсестер[en], медсестер-анестезіологів[en], асистентів анестезіологів[en], техніків-анестезіологів[en], асоційованих спеціалістів з анестезії[en], практикуючих лікарів відділу операцій[en] та технологів анестезії[en]. Міжнародні стандарти безпечної практики анестезії, спільно схвалені Всесвітньою організацією охорони здоров'я та Всесвітньою федерацією товариств анестезіологів[en], настійно рекомендують, щоб анестезія здійснювалася, контролювалася або проводилася анестезіологами, за винятком мінімальної седації або поверхневих процедур, які виконуються під місцевою анестезією[2]. Підготовлений, пильний анестезіолог повинен постійно доглядати за пацієнтом; якщо постачальник анестезії не є анестезіологом, їм повинен керувати та контролювати місцевий анестезіолог, а в країнах або в умовах, де це неможливо, допомога повинна надаватися найбільш кваліфікованою місцевою особою в межах регіональної чи національної структури під керівництвом анестезіолога[2]. Ті самі мінімальні стандарти безпеки пацієнтів[en] застосовуються незалежно від постачальника, включаючи постійний клінічний і біометричний моніторинг оксигенації тканин, перфузії та артеріального тиску; підтвердження правильності розміщення пристроїв для проходження дихальних[en] шляхом аускультації та визначення вуглекислого газу; використання контрольного списку хірургічної безпеки ВООЗ[en]; і безпечний подальший догляд за пацієнтом після процедури[2].
| Клас АТА (ASA) | Фізичний статус |
|---|---|
| АТА 1 | Здорова людина |
| АТА 2 | Легке системне захворювання[en] |
| АТА 3 | Важке системне захворювання |
| АТА 4 | Важке системне захворювання, що є постійною загрозою для життя |
| АТА 5 | Вмираюча людина, яка, як очікується, не виживе без операції |
| АТА 6 | Людина, мозок якої оголошений мертвим, чиї органи вилучаються для донорських цілей |
| E | Суфікс додано для пацієнтів, які проходять Екстрену процедуру |
Частина оцінки ризику базується на стані здоров'я пацієнта. Американське товариство анестезіологів (АТА, англ. ASA) розробило шестирівневу шкалу, яка розділяє фізичний стан пацієнта перед операцією на класи. Вона називається «Система класифікації фізичного стану АТА (ASA)». Шкала оцінює ймовірність того, що під час або після анестезії виникнуть ускладнення або проблеми, на основі загального стану здоров'я пацієнта та типу анестезії[3].
Більш детальний передопераційний анамнез має бути спрямований на виявлення генетичних розладів (таких як злоякісна гіпертермія або дефіцит псевдохолінестерази[en]), звичок (вживання тютюну, наркотиків і алкоголю[en]), фізичних атрибутів (таких як ожиріння або утруднені дихальні шляхи[en]) і будь-яких супутніх захворювань (особливо серцевих та респіраторних захворювань), які можуть вплинути на анестезію. Фізичне обстеження допомагає кількісно визначити вплив будь-яких факторів, знайдених в історії хвороби на додаток до лабораторних тестів[1].
Окрім загальної оцінки стану здоров'я пацієнта, для анестезії також необхідно враховувати оцінку конкретних факторів, які стосуються операції. Наприклад, анестезія при пологах повинна враховувати не тільки мати, але і дитину. Злоякісні пухлини та новоутворення, які знаходяться в легенях або в горлі[en], створюють особливі виклики для загальної анестезії. Після визначення стану здоров'я пацієнта, який проходить анестезію, і бажаного ефекту, необхідного для завершення процедури, можна вибрати тип анестетика. Вибір хірургічного методу та техніки анестезії має на меті знизити ризик ускладнень, скоротити час, необхідний для відновлення, та мінімізувати реакцію на хірургічний стрес[en].


Анестезія є комбінацією бажаних ефектів (обговорюваних вище), які досягаються за допомогою препаратів, що діють на різні, але пов'язані між собою, ділянки центральної нервової системи. Загальна анестезія (на відміну від седації або місцевої анестезії) має три основні цілі: відсутність рухів (параліч), втрату свідомості[en] та притуплення реакції на стрес. На ранніх етапах використання анестезії анестетики могли надійно досягати перших двох цілей, дозволяючи хірургам виконувати необхідні процедури, але багато пацієнтів помирали через те, що екстремальні значення артеріального тиску та пульсу, викликані хірургічним ушкодженням, врешті-решт були шкідливими. Зрештою, Гарві Кушинг виявив необхідність притуплення реакції на хірургічний стрес[en], коли він зробив ін'єкцію місцевого анестетика перед вправлення грижі[1]. Це призвело до розробки інших ліків, які могли б притупити реакцію на стрес, що призвело до зниження рівня хірургічної смертності.
Найпоширенішим підходом до досягнення бажаних ефектів загальної анестезії є використання інгаляційних загальних анестетиків. Кожен анестетик має власну силу, яка залежить від його розчинності в олії. Ця залежність пояснюється тим, що препарати зв'язуються безпосередньо з порожнинами в білках центральної нервової системи, хоча існує декілька теорій дії загального наркозу[en]. Вважається, що інгаляційні анестетики впливають на різні відділи центральної нервової системи. Наприклад, іммобілізуючий ефект інгаляційних анестетиків є наслідком впливу на спинний мозок, тоді як седація, гіпноз і амнезія залучають ділянки в мозку[1]. Ефективність інгаляційного анестетика кількісно визначається його мінімальною альвеолярною концентрацією (МАК). МАК — це відсоткова доза анестетика, яка запобігає реакції на больовий подразник у 50 % суб'єктів. Як правило, чим вище МАК, тим менш потужний анестетик.

Ідеальний анестетик забезпечував би гіпноз, амнезію, аналгезію та розслаблення м'язів без небажаних змін артеріального тиску, пульсу чи дихання. У 1930-х роках лікарі почали доповнювати інгаляційні загальні анестетики загальними внутрішньовенними анестетиками. Препарати, які використовувалися в комбінації, забезпечували кращий профіль ризику для суб'єкта під анестезією та швидше одужання. Пізніше було показано, що комбінація препаратів знижує ймовірність смерті в перші сім днів після анестезії. Наприклад, пропофол (ін'єкція) може використовуватися для початку анестезії, фентаніл (ін'єкція) використовується для притуплення реакції на стрес, мідазолам (ін'єкція) для забезпечення амнезії та севофлуран (інгаляція) під час процедури для підтримки ефекту. Нещодавно було розроблено кілька препаратів для внутрішньовенного введення, які, за бажання, дозволяють повністю відмовитися від інгаляційних загальних анестетиків[1].
Основним інструментом у системі постачання інгаляційної анестезії є наркозний апарат. Він має випарники, вентилятори, дихальний контур анестезії, систему видалення відпрацьованих газів і манометри. Призначення наркозного апарату полягає в тому, щоб подавати анестетичний газ під постійним тиском, кисень для дихання та видалити вуглекислий газ або інші відпрацьовані анестетичні гази. Оскільки інгаляційні анестетики легкозаймисті, було розроблено різні контрольні списки, щоб підтвердити, що апарат готовий до використання, що функції безпеки активні та небезпеки, пов'язані з електрикою, усунено[4]. Внутрішньовенна ін'єкція анестетика здійснюється болюсними[en] дозами або інфузійним насосом[en]. Існує також багато менших інструментів, які використовуються для управління дихальними шляхами[en] та спостереження за пацієнтом. Загальною рисою сучасного обладнання[en] в цій галузі є використання безвідмовних систем[en], які зменшують шанси катастрофічного неправильного використання апарата[5].

Пацієнти під загальним наркозом повинні проходити постійний фізіологічний моніторинг для забезпечення безпеки. У США Американське товариство анестезіологів[en] (АТА) встановило мінімальні вказівки щодо моніторингу пацієнтів, які отримують загальну анестезію, регіональну анестезію або седацію. До них відносяться електрокардіографія (ЕКГ), частота серцевих скорочень, артеріальний тиск, гази, що вдихаються і видихаються, насичення крові киснем (пульсоксиметрія) і температура[6]. У Великобританії Асоціація анестезіологів (англ. AAGBI) встановила мінімальні рекомендації щодо моніторингу загальної та регіональної анестезії. Для невеликих хірургічних втручань це, як правило, включає моніторинг частоти серцевих скорочень, насичення крові киснем[en], артеріального тиску, а також концентрації кисню, вуглекислого газу та інгаляційних анестетиків у вдиху та видиху. Для більш інвазивних операцій моніторинг може також включати температуру, виділення сечі, артеріальний тиск, центральний венозний тиск, тиск у легеневій артерії та тиск оклюзії легеневої артерії[en], серцевий викид, церебральну активність[en] і нервово-м'язову функцію. Крім того, в операційній необхідно контролювати температуру та вологість навколишнього середовища, а також накопичення видихуваних інгаляційних анестетиків, які можуть бути шкідливими для здоров'я персоналу операційної[7].
Седація (також відома як диссоціативна анестезія або сутінкова анестезія) створює гіпнотичні, седативні, анксіолітичні, амнезійні, протисудомні властивості та властивості розслаблення м'язів, які створюються завдяки впливу на центральну нервову систему. З точки зору людини, яка надає седативний засіб, пацієнт виглядає сонним, розслабленим і забудькуватим, що дозволяє легше завершити неприємні процедури. Заспокійливі, такі як бензодіазепіни, зазвичай дають разом із знеболюючими (такими як наркотики, або місцеві анестетики або обидва), оскільки вони самі по собі не забезпечують значного полегшення болю[8].
З точки зору суб'єкта, який отримує заспокійливий засіб, ефектами є відчуття загального розслаблення, амнезія (втрати пам'яті) і швидкий плин часу. Багато препаратів можуть мати седативний ефект, включаючи бензодіазепіни, пропофол, тіопентал, кетамін та інгаляційні загальні анестетики. Перевага седації перед загальною анестезією полягає в тому, що вона, як правило, не вимагає підтримки дихальних шляхів або дихання (без інтубації трахеї чи штучної вентиляції легенів) і може мати менший вплив на серцево-судинну систему, що може збільшити запас безпеки для деяких пацієнтів[1].
У хірургічній практиці з метою знеболювання застосовують тимчасову анестезію (місцеву або загальну, тобто наркоз). Початок методу місцевої анестезії поклав російський вчений В. К. Анреп, який відкрив знеболювальні властивості кокаїну (1879)[джерело?].
З 1885 анестезію почали широко використовувати. У СРСР її всебічно розробив радянський хірург О. В. Вишневський.
Коли біль блокується з частини тіла за допомогою місцевих анестетиків, це зазвичай називають регіональною анестезією. Існує багато типів регіональної анестезії — ін'єкція в саму тканину, в вену, яка живить область або в місце навколо нервового стовбура, який забезпечує відчуття в цій області. Останні називаються нервовими блокадами і поділяються на периферичні або центральні нервові блокади.
Нижче наведені види регіонарної анестезії[1]:
Огляд Кокранівської співпраці 2018 року виявив докази помірної якості, що регіонарна анестезія може зменшити частоту стійкого післяопераційного болю від 3 до 18 місяців після торакотомії та від 3 до 12 місяців після кесаревого розтину[10]. Докази низької якості були знайдені щодо періоду через 3-12 місяців після операції, пов'язаної з раком молочної залози[10]. В огляді згадуються певні обмеження, які впливають на його застосування за межами розглянутих хірургічних втручань і методів регіональної анестезії[10].
Методи місцевої анестезії достатньо різноманітні. Анестезією, залежно від потреби, можна викликати змазуванням або зрошуванням (закапуванням) слизових оболонок: ока (кон'юнктиви), носа, рота, гортані, трахеї, бронхів, стравоходу 1-3 % розчином дикаїну, лідокаїну або іншими знеболювальними засобами. Анестезія шкіри досягається охолодженням її за допомогою етеру або хлоретилу, рідше холодовими пакетами (вода, лід). Ефективніше місцеве знеболювання — введення за допомогою шприца та голки в тканини місцевого знеболювального (наприклад, 0,25-0,5 % розчину новокаїну).
Також при хірургічних втручаннях застосовують інфільтраційну анестезію, суть якої полягає в просяканні тканин значною кількістю 0,25 % розчину новокаїну («повзучий інфільтрат» за О. В. Вишневським). Для складніших оперативних втручань використовують провідникову анестезію (за Лукашевичем-Оберстом), яка створює знеболювання певної (анатомічної) ділянки (або декількох ділянок) тіла. Виконують цей вид знеболення ін'єкцією анестезійного розчину по ходу нервів, у нервові сплетіння, в кровоносні судини (блокада Біра англ. Biera[11]), в кістку, в підпавутинний простір спинного мозку (спинномозкова анестезія), в клітковину між листками твердої оболони спинного мозку (епідуральна анестезія).
Коли місцевий анестетик вводять навколо нерва більшого діаметру, який передає відчуття від усієї області, це називається блокадою нерва[en] або блокадою регіонального нерва. Нервові блокади зазвичай використовуються в стоматології, коли блокується нижньощелепний нерв для проведення процедур на нижніх зубах. З нервами більшого діаметру (наприклад, міжлусковинний блок для верхніх кінцівок або блок поперекового відділу[en] для нижніх кінцівок) нерв і положення голки локалізуються за допомогою ультразвукової або електричної стимуляції. Існують докази, які підтверджують, що використання ультразвукового контролю окремо або в поєднанні зі стимуляцією периферичних нервів, є найкращим використанням для покращення сенсорної та моторної блокади, зменшення потреби в добавках і меншої кількості ускладнень[12]. Через велику кількість місцевого анестетика, необхідного для впливу на нерв, слід враховувати максимальну дозу місцевого анестетика. Нервові блокади також використовуються в якості безперервної інфузії після серйозних операцій, таких як операція по заміні коліна, стегна та плеча, і можуть бути пов'язані з меншою кількістю ускладнень[13]. Нервові блокади також пов'язані з меншим ризиком неврологічних ускладнень порівняно з більш центральними епідуральними або спінальними нейроаксіальними блоками[1].
Центральна нейроаксіальна анестезія[en] – це ін'єкція місцевого анестетика навколо спинного мозку для забезпечення знеболення в черевній порожнині, тазі або нижніх кінцівках. Поділяється на спінальну (ін'єкція в субарахноїдальний простір), епідуральну (ін'єкція за межі субарахноїдального простору в епідуральний простір) і каудальну (ін'єкція в кінський хвіст або хвіст спинного мозку). Спінальна та епідуральна є найбільш часто використовуваними формами центральної нейроаксіальної блокади.
Спінальна анестезія — це «одноразова» ін'єкція, яка забезпечує швидкий початок і глибоку сенсорну анестезію меншими дозами анестетика та зазвичай пов'язана з нервово-м'язовою блокадою[en] (втратою контролю над м'язами). Епідуральна анестезія використовує більші дози анестетика, введеного через постійний катетер, що дозволяє підсилити анестезію, якщо ефекти починають розсіюватися. Епідуральна анестезія зазвичай не впливає на контроль м'язів.
Оскільки центральна нейроаксіальна блокада викликає артеріальну та венозну вазодилатацію[en], падіння артеріального тиску є поширеним явищем. Це падіння значною мірою продиктовано венозною частиною кровоносної системи, яка містить 75 % об'єму циркулюючої крові. Фізіологічні ефекти набагато сильніші, коли блок розміщується над 5-м грудним хребцем[en]. Неефективна блокада найчастіше виникає через неадекватний анксіоліз або седацію, а не через неспрацювання самої блокади[1].

Ноцицепція[en] (відчуття болю) не закріплена в організмі. Натомість це динамічний процес, у якому постійні больові подразники можуть посилити чутливість системи та ускладнити лікування болю або сприяти розвитку хронічного болю. З цієї причини превентивне лікування гострого болю може зменшити як гострий, так і хронічний біль і має бути налаштоване у відповідності до операції, середовища, в якому вона проводиться (стаціонар/амбулаторна процедура), та окремої людини[1].
Управління болем класифікується як запобіжний засіб або засіб на вимогу. Знеболювальні препарати на вимогу зазвичай включають опіоїдні або нестероїдні протизапальні препарати, але також можуть використовуватися нові підходи, такі як інгаляційний закис азоту[14] або кетамін[15]. Ліки на вимогу може вводити лікар (ліки прописують лише тоді, коли пацієнт їх просить або коли вони необхідні для конкретної ситуації) або пацієнт за допомогою контрольованої пацієнтом аналгезії[en] (КПА). Було показано, що КПА забезпечує дещо кращий контроль болю та підвищує задоволеність пацієнтів порівняно зі звичайними методами[16]. Загальні превентивні підходи включають епідуральну нейроаксіальну блокаду[17] або нервові блоки[14]. В одному огляді, який вивчав контроль болю після операції на черевній аорті, було встановлено, що епідуральна блокада забезпечує краще полегшення болю (особливо під час рухів) у період до трьох днів після операції. Тривалість післяопераційної інтубації трахеї скорочується приблизно вдвічі. Частота тривалої післяопераційної штучної вентиляції легень та інфаркту міокарда також зменшується завдяки епідуральній аналгезії[18].
Ризики та ускладнення, пов'язані з анестезією, класифікуються як захворюваність (хвороба чи розлад, що є наслідком анестезії) або смертність[en] (смерть, що є результатом анестезії). Кількісно визначити, як анестезія впливає на захворюваність і смертність, може бути важко, оскільки стан здоров'я пацієнта до операції та складність хірургічної процедури також можуть сприяти ризикам.

До появи анестезії на початку 19 століття фізіологічний стрес від операції викликав значні ускладнення та багато смертей від шоку. Чим швидше була операція, тим менший був рівень ускладнень (що призводило до повідомлень про дуже швидкі ампутації). Поява анестезії дозволила завершувати складніші операції, які рятували життя, зменшила фізіологічний стрес операцій, але також додала елемент ризику. Перший смертельний випадок, безпосередньо пов'язаний із застосуванням анестезії, було зареєстровано через два роки після появи етерних анестетиків[20].
Захворюваність може бути серйозною (інфаркт міокарда, пневмонія, емболія легеневої артерії, ниркова недостатність/хронічна хвороба нирок, післяопераційна когнітивна дисфункція[en] та алергія[en]) або незначною (незначна нудота, блювання, повторна госпіталізація). Зазвичай існує зв'язок між факторами, що призводять до захворюваності та смертності, між станом здоров'я пацієнтів, типом операції, що виконується, та анестетиком. Щоб зрозуміти відносний ризик кожного сприяючого фактора, візьміть до уваги, що співвідношення кількості смертей, які повністю пов'язані зі здоров'ям пацієнта, становить 1:870. Порівняйте це з співвідношенням кількості смертей, повною мірою пов'язаних з хірургічними факторами (1:2860) або лише з анестезією (1:185 056), що свідчить про те, що найбільшим фактором смертності від анестезії є здоров'я пацієнта. Цю статистику також можна порівняти з першим подібним дослідженням смертності під час анестезії з 1954 року, яке повідомляло про співвідношення смертності 1:75 від усіх причин та 1:2680 від причин, пов'язаних лише з анестезією[1]. Пряме порівняння між статистичними даними про смертність не можна достовірно зробити в часі та між країнами через відмінності в стратифікації факторів ризику, проте є докази того, що було досягнуто значного покращення безпеки анестетиків[21] але ступінь покращення залишається непевною[19].
Замість того, щоб використовувати фіксований рівень захворюваності або смертності, розглядають багато факторів, які сприяють відносному ризику процедури та анестетики разом. Наприклад, операція для пацієнта віком від 60 до 79 років ставить в 2,3 рази більший ризик, ніж для особи молодше 60 років. Пацієнти з класом 3, 4 або 5 за шкалою АТА мають ризик у 10,7 разів більший, ніж пацієнти з класом 1 або 2. Інші змінні включають вік понад 80 років (ризик у 3,3 рази більший порівняно з особами, яким менше 60 років), стать (жінки мають нижчий ризик з коефіцієнтом 0,8), терміновість процедури (невідкладні випадки мають у 4,4 рази більший ризик), досвід особи, яка виконує процедуру (менше 8 років досвіду та/або менше 600 виконаних процедур мають в 1,1 рази більший ризик) і тип анестетика (регіональні анестетики мають менший ризик, ніж загальні анестетики)[1]. Акушерські пацієнтки, дуже молоді та дуже старі пацієнти мають більший ризик ускладнень, тому можуть знадобитися додаткові заходи[1].
14 грудня 2016 року Управління з контролю за якістю харчових продуктів і медикаментів США випустило попередження з питань громадської безпеки, що «повторне або тривале використання загальних анестетиків і седативних препаратів під час операцій або процедур у дітей молодше 3 років або у вагітних жінок протягом третього триместру може вплинути на розвиток дитячого мозку»[22]. Це попередження було розкритиковане Американським коледжем акушерів і гінекологів, який вказав на відсутність прямих доказів щодо застосування анестетиків вагітними жінками і можливість того, що «це попередження може неналежним чином переконати постачальників анестезії від надання медичної допомоги під час вагітності»[23]. Прихильники пацієнтів зазначили, що рандомізоване клінічне випробування було б неетичним, що механізм ушкодження добре вивчений на тваринах і що дослідження показали, що багаторазове використання анестетиків значно підвищує ризик розвитку труднощів у навчанні у маленьких дітей, з співвідношенням ризику[en] 2,12 (95 % довірчий інтервал, 1,26–3,54)[24].
Безпосередній період після анестезії називається пробудженням. Пробудження із загальної анестезії або седації вимагає ретельного моніторингу, оскільки на цьому етапі все ще існує ризик ускладнень[25]. Нудота та блювота спостерігаються у 9,8 % пацієнтів, але цей відсоток залежить від типу анестезії та процедури. Існує потреба в підтримці дихальних шляхів[en] у 6,8 %, можлива ішурія (частіше у людей старше 50 років) і гіпотензія у 2,7 %. Гіпотермія, тремтіння та сплутаність свідомості також є поширеними у найближчий післяопераційний період через відсутність руху м'язів (і пов'язану з цим відсутність виробництва тепла організмом) під час процедури[1]. Крім того, рідкісним проявом у період після анестезії може бути поява розладу функціональних неврологічних симптомів[26].
Післяопераційна когнітивна дисфункція[en] також відома як ПОКД і сплутаність свідомості після анестезії) — це порушення сприйняття після операції. Ця назва широко використовується для опису делірія пробудження[en] (безпосередня післяопераційна сплутаність свідомості) та ранньої когнітивної дисфункції (зниження когнітивних функцій у перший післяопераційний тиждень). Незважаючи на те, що ці три сутності (делірій, рання ПОКД і тривала ПОКД) є різними, наявність делірія після операції передбачає наявність ранньої ПОКД. Наразі відсутні докази зв'язку між делірієм або ранньою ПОКД і довготривалою ПОКД[27]. Згідно з нещодавнім дослідженням, проведеним у медичній школі Девіда Геффена при Каліфорнійському університеті Лос-Анджелеса[en], мозок повертається до свідомості через серію кластерів активності або «хабів». Ендрю Хадсон, доцент кафедри анестезіології, стверджує: «Відновлення після анестезії є не просто результатом „вивітрювання“ анестезії, а й того, що мозок знаходить шлях назад через лабіринт можливих станів активності до тих, які дозволяють свідомий досвід. Простіше кажучи, мозок сам перезавантажується»[28].
Довготривала ПОКД — це незначне погіршення когнітивних функцій, яке може тривати тижнями, місяцями або довше. Найчастіше родичі людини повідомляють про брак уваги, пам'яті та втрату інтересу до занять, які раніше були для людини цікавими (наприклад, до кросвордів). Подібним чином в робочому середовищі можуть повідомляти про нездатність людей виконувати завдання з тією ж швидкістю, що й раніше[29]. Існують переконливі докази того, що ПОКД виникає після кардіохірургічних операцій і основною причиною її виникнення є утворення мікроемболів. ПОКД також виникає в не-серцевих хірургічних втручаннях. Причини в не-серцевій хірургії менш зрозумілі, але старший вік є фактором ризику для виникнення ПОКД[1].

Першими спробами загальної анестезії були, ймовірно, трав'яні засоби, які використовували в доісторичні часи. Алкоголь є одним із найстаріших відомих седативних засобів, і його використовували в стародавній Месопотамії тисячі років тому[30]. Шумери, ймовірно, культивували та збирали опіумний мак (лат. Papaver somniferum) у нижній Месопотамії ще в 3400 р. до н. е.[31][32]. Стародавні єгиптяни використовували хірургічні інструменти[33][34], а також прості анальгетики та седативні засоби, включно з, можливо, екстрактом плодів мандрагори[35].
У Китаї Бянь Цао (кит.: 扁鹊, Система Вейда-Джайлза: Pien Ch'iao, бл. 300 р. до н. е.) був легендарним китайським терапевтом і хірургом, який, імовірно, використовував загальну анестезію для хірургічних процедур[джерело?]. Незважаючи на це історики вважали, що перша розробка (яка піддається історичній перевірці) певного типу суміші анестезії, належить китайському лікарю Хуа То, хоча його рецепт ще повністю не розкрито[36].
По всій Європі, Азії та Америці для анестезії використовували різноманітні види пасльонових, що містять потужні алкалоїди тропану[en]. В Італії 13-го століття Теодорік Боргоньоні[en] використовував подібні суміші разом з опіатами, щоб викликати втрату свідомості; лікування комбінованими алкалоїдами було основою анестезії до 19-го століття. Місцеві анестетики використовувалися в цивілізації інків[en], де шамани жували листя коки і проводили операції на черепі, плюючи в рани, які вони створювали, для знеболювання[37]. Пізніше був виділений кокаїн, який став першим ефективним місцевим анестетиком. Вперше він був використаний у 1859 році Карлом Коллером[en] за пропозицією Зигмунда Фрейда в хірургії ока[en] в 1884 році[38]. Німецький хірург Август Бір (1861—1949) першим застосував кокаїн для інтратекальної[en] анестезії в 1898 році[39]. Румунський хірург Ніколае Раковічану-Пітешті (1860—1942) першим застосував опіоїди опіоїди для інтратекальної аналгезії; він представив свій досвід у Парижі в 1901 році[40].
При тривалому прийманні, кокаїн викликав хворобливе звикання. Новий етап в місцевому знеболюванні розпочався з появою новокаїну, що створений на основі кокаїну, але не викликає звикання. З введенням в практику розчинів новокаїну стали розвиватися різні способи місцевого знеболювання: інфільтраційна, провідникова і спинномозкова анестезія.
«Снодійна губка» («губка для сну»), яку використовували арабські лікарі, була завезена в Європу Салернською медичною школою наприкінці 12 століття та Уго Боргоньоні[en] (1180—1258) у 13 столітті. Губку пропагував і описував син Уго, який також був хірургом — колегою Уго, Теодорік Боргоньоні[en] (1205—1298). При цьому методі знеболення губку змочували розчином опію, мандрагори, соку болиголова та інших речовин. Потім губку висушували та зберігали; безпосередньо перед операцією губку змочували, а потім тримали під носом пацієнта. Якщо все йшло за планом, випари призводили до того, що пацієнт втрачав свідомість[41].

Найвідоміший анестетик, етер, імовірно був синтезований ще у VIII столітті[42][43], але знадобилося багато століть, щоб оцінити його анестетичну важливість, навіть незважаючи на те, що лікар і ерудит 16-го століття Парацельс помітив, що кури, які його вдихали, не тільки засинали, але й не відчували болю. На початку 19 століття етер використовувався людьми, але лише як рекреаційний наркотик[44].
Тим часом у 1772 році англійський вчений Джозеф Прістлі відкрив газ закис азоту. Спочатку люди вважали цей газ смертельним навіть у малих дозах, як і деякі інші оксиди азоту. Однак у 1799 році британський хімік і винахідник Гамфрі Деві вирішив це з'ясувати, експериментуючи на собі. На свій подив, він виявив, що закис азоту змушує його сміятися, тому він назвав його «звеселяючим газом»[45]. У 1800 році Деві писав про потенційні анестетичні властивості закису азоту для полегшення болю під час операції, але в той час ніхто більше не займався цим питанням[45].
14 листопада 1804 року Ханаока Сейшу[en], японський лікар, став першою людиною, яка успішно провела операцію під загальною анестезією[46]. Ханаока вивчав традиційну японську медицину, а також імпортовану з Голландії європейську хірургію та китайську медицину. Після років досліджень і експериментів він нарешті розробив формулу, яку він назвав tsūsensan (також відому як mafutsu-san), яка поєднувала корейську іпомею та інші трави[47].
Успіх Ханаоки у виконанні цієї безболісної операції незабаром став широко відомий, і пацієнти почали прибувати з усіх частин Японії. Ханаока продовжував виконувати багато операцій з використанням tsūsensan, включаючи резекцію злоякісних[en] пухлин, вилучення каменів із сечового міхура та ампутації кінцівок[48]. До своєї смерті в 1835 році Ханаока виконав понад 150 операцій з приводу раку грудей. Однак це відкриття не принесло користі решті світу до 1854 року, оскільки політика національної ізоляції сьогунату Токуґава не дозволила оприлюднити досягнення Ханаоки до закінчення ізоляції[49]. Минуло майже сорок років, перш ніж Кроуфорд Лонг[en], якого називають винахідником сучасних анестетиків Західного світу, застосував загальну анестезію у Джефферсоні, штат Джорджія[50].
Лонг помітив, що його друзі не відчували болю, коли вони поранилися, хитаючись під дією діетилового етеру. Він одразу подумав про можливе використання етеру у хірургії. Так склалося, що учасник однієї з тих «ефірних розваг», студент на ім'я Джеймс Венейбл, мав дві невеликі пухлини, які він хотів видалити. Але побоюючись болю від операції, Венейбл постійно відкладав її. Тому Лонг запропонував йому зробити операцію під дією етеру. Венейбл погодився, і 30 березня 1842 року йому зробили безболісну операцію. Однак Лонг не оголосив про своє відкриття до 1849 року[51].


Хорас Уеллс[en] провів першу публічну демонстрацію інгаляційного анестетика в Массачусетській загальній лікарні[en] в Бостоні в 1845 році. Однак закис азоту було введено неправильно, і людина закричала від болю[52]. 16 жовтня 1846 року дантист з Бостона Вільям Томас Грін Мортон провів успішну демонстрацію використання діетилового етеру для студентів-медиків в тій же лікарні[53]. Мортона, який не знав про попередню роботу Лонга, запросили до загальної лікарні штату Массачусетс[en], щоб продемонструвати свою нову техніку безболісної операції. Після того, як Мортон ввів наркоз, хірург Джон Коллінз Уоррен[en] видалив пухлину з шиї Едварда Гілберта Еббота[en]. Це сталося в хірургічному амфітеатрі, який зараз називається Етерним куполом[en]. Раніше скептично налаштований Уоррен був вражений і заявив: «Панове, це не обман». У листі до Мортона незабаром після цього лікар і письменник Олівер Венделл Холмс-старший запропонував назвати стан, що виробляється, «анестезією», а процедуру — «анестетичною»[44].
Мортон спочатку намагався приховати справжню природу своєї анестетичної речовини, називаючи її летеоном. Він отримав патент США[en] на свою речовину, але новина про успішний анестетик швидко поширилася до кінця 1846 року. Поважні хірурги в Європі, включаючи Лістона[en], Діффенбаха[en], Пирогова та Сайма[en], швидко провели численні операції з етером. Лікар американського походження Бутт заохочував лондонського стоматолога Джеймса Робінсона[en] провести стоматологічну процедуру на міс Лонсдейл. Це був перший випадок оператора-анестезіолога (коли особа, яка виконує операцію, також відповідає за моніторинг і керування анестезією пацієнта). Того ж дня, 19 грудня 1846 року, в Королівській лікарні Дамфріса, Шотландія, доктор Скотт використав етер для хірургічної процедури[54]. Перше застосування анестезії в південній півкулі відбулося в Лонсестоні, Тасманія, того ж року. Недоліки етеру, такі як викликана їм надмірна блювота та його вибухонебезпечна займистість, призвели до заміни етеру в Англії хлороформом.[джерело?]
В 1844 році у газеті «Російський інвалід» була опублікована стаття Я. Чистовича «Про ампутацію стегна при посередництві сірчаного етеру»[джерело?][55]. Провідником застосування передопераційної та операційної анестезії був Микола Іванович Пирогов[джерело?].
Відкритий у 1831 році американським лікарем Семюелем Гутрі (1782—1848), а через кілька місяців незалежно від нього французом Еженом Субейраном (1797—1859) і Юстусом фон Лібіхом (1803—1873) у Німеччині, хлороформ був названий і хімічно охарактеризований у 1834 році Жаном-Батістом Дюма (1800—1884). У 1842 році доктор Роберт Мортімер Гловер[en] у Лондоні виявив анестезуючу дію хлороформу на лабораторних тваринах[56].
У 1847 році шотландський акушер Джеймс Янг Сімпсон[en] першим продемонстрував анестетичні властивості хлороформу на людях і допоміг популяризувати препарат для використання в медицині[57]. Ця перша поставка надійшла від місцевих фармацевтів Джеймса Дункана та Вільяма Флокхарта[en], і його використання швидко поширилося, до 750 000 доз щотижня в Британії в 1895 році. Сімпсон домовився з Флокхартом про постачання хлороформом Флоренс Найтінгейл[58]. Хлороформ отримав королівське схвалення в 1853 році, коли Джон Сноу дав його королеві королеві Вікторії, коли вона народжувала принца Леопольда. Щодо досвіду народження дитини, хлороформ виправдав усі очікування королеви; вона описала досвід як «чудовий понад міру»[59]. Однак хлороформ був не без недоліків. Перший смертельний випадок, безпосередньо пов'язаний із застосуванням хлороформу, був зареєстрований 28 січня 1848 року після смерті Ханни Ґрінер[60]. Це був перший з багатьох смертельних випадків, пов'язаних з недостатнім навчанням поводження з хлороформом. Хірурги почали розуміти потребу в кваліфікованих анестезіологах. Як пише Тетчер, необхідно було, щоб анестезіолог "(1) приймав як належне підпорядкованість ролі, якої вимагатиме робота, (2) зробив анестезію своїм єдиним поглинаючим інтересом, (3) не розглядав свою роль анестезіолога як таку, що надасть можливість спостерігати за роботою хірургів і вчитися в них, (4) погоджувався на порівняно низьку оплату праці та (5) мав природні здібності та інтелект, щоб розвивати високий рівень навичок у забезпеченні плавної анестезії та релаксації, яких вимагає хірург[61]. Ці якості анестезіолога часто зустрічалися у підпорядкованих студентах-медиках[en] і навіть у представниках громадськості. Частіше, хірурги шукали медсестер для проведення анестезії. До початку громадянської війни в США, багато медсестер пройшли професійну підготовку за підтримки хірургів.
Джон Сноу з Лондона публікував декілька статей з травня 1848 року «Про наркотизм шляхом вдихання парів» у «Лондонській медичній газеті»[62]. Сноу також брав участь у виробництві обладнання, необхідного для введення інгаляційних анестетиків[en], попередника сучасних апаратів для наркозу[63].
Також в 1867 році британський медик і анестезіолог Бенджамін Уорд Річардсон створив розпилювач Річардсона, який за допомогою пульверизатора розпилював сірчаний етер на шкіру, після чого вона біліла і заморожувалася. На той час це був один з найбільш досконалих методів місцевої анестезії[64].
Еліс Маго, яка народилася в листопаді 1860 року, часто називають «матір'ю анестезії». Її відомість як особистого анестезіолога для Вільяма та Чарльза Мейо була підкреслена власними словами Мейо в його статті 1905 року, в якій він описав своє задоволення та довіру до медсестер-анестезіологів: «Питання анестезії є найважливішим. У нас є постійні анестезіологи, на кого я можу покластися, щоб я мав змогу присвятити всю свою увагу хірургічній роботі». Маго вела ретельний облік своїх пацієнтів і записувала практику застосування анестезії. У своїй публікації, в якій розглядається понад 14 000 випадків хірургічних операцій із застосування анестезії, Маго вказує, що вона успішно застосовувала анестезію без випадків смерті, пов'язаних тільки з анестезією. В іншій статті Маго описує: «Ми вводили анестетик 1092 рази; тільки етер 674 рази; тільки хлороформ 245 разів; етер і хлороформ разом 173 рази. Я можу повідомити, що з цих 1092 випадків у нас не було нещасних випадків». Записи та результати Маго створили спадщину, яка визначає, що проведення анестезії медсестрами буде служити хірургічному співтовариству без збільшення ризиків для пацієнтів. Насправді, результати Маго затьмарили б результати практиків сьогодення[65].
Перший всеосяжний медичний підручник з цього питання, Анестезія, був написаний у 1914 році анестезіологом, доктором Джеймсом Тейло Гватмі[en] та хіміком, доктором Чарльзом Баскервілем[en][66]. Ця книга слугувала стандартним довідником для спеціальності протягом десятиліть і містила детальну інформацію про історію анестезії, а також фізіологію та техніку інгаляційної, ректальної, внутрішньовенної та спинномозкової анестезії[66].
З цих перших відомих анестетиків тільки закис азоту все ще широко використовується сьогодні, при цьому хлороформ і етер були замінені більш безпечними, але іноді дорожчими загальними анестетиками[en], а кокаїн — більш ефективними місцевими анестетиками, які мають менші можливості неправильного використання[67].
Майже всі постачальники медичних послуг певною мірою використовують анестетики, але більшість медичних професій мають власних спеціалістів у цій галузі, включаючи медицину, сестринську справу та стоматологію.
Лікарі, які спеціалізуються на анестезіології, включаючи періопераційний догляд, розробку плану анестезії та застосування анестетиків, відомі в США як англ. anesthesiologists , а у Великобританії, Канаді, Австралії та Новій Зеландії як англ. anaesthetists або англ. anaesthesiologists. Усі застосування анестезії у Великій Британії, Австралії, Новій Зеландії, Гонконзі та Японії проводяться лікарями. Медсестри-анестезіологи[en] також проводять анестезію в 109 країнах[68]. В США в 35 % випадках анестезію надають лікарі в індивідуальній практиці, приблизно у 55 % випадках анестезію надають анестезіологічні бригади з анестезіологами, які керують сертифікованими медсестрами-анестезіологами або асистентами анестезіологів, і у близько 10 % випадках анестезію надають анестезіологи[68][69][70]. З процедурою анестезії також можуть допомагати асистенти анестезіолога[en] (США) або асистенти лікаря (анестезіолог)[en] (Велика Британія)[71].
Існує багато випадків, коли анестезію потрібно змінити для особливих обставин через процедуру (наприклад, у кардіохірургії, кардіоторакальній анестезіології[en] чи нейрохірургії), пацієнта (наприклад, у педіатричній, геріатричній[en], баріатричній або акушерській анестезії) або особливі обставини (наприклад, під час травм, догоспітальної допомоги, роботизованої хірургії або екстремальних умов).
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.