Loading AI tools
Бензальдегід (C6H5CHO) — органічна сполука, що складається з бензольного кільця заміщенного формільною групою. Він є найпростішим ароматичним альдегідом та одним з найбільш промислово корисних. Ця безбарвна рідина має характерний приємний запах, схожий на запах мигдалю. Дійсно, бензальдегід є головним компонентом гіркої мигдалевої олії і може бути екстрагований з великого числа інших природних джерел.[2] Бензальдегід вперше був екстрагований з гіркого мигдалю у 1803 році французьким аптекарем Мартре.[3] У 1832 році німецькі хіміки Фрідріх Велер та Юстус фон Лібіх вперше синтезували бензальдегід.[4]
| Benzaldehyde | |
|---|---|
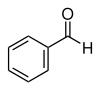 Структурна формула |
 Просторова модель |
| Назва за IUPAC | Бензальдегід |
| Систематична назва | Бензолкарбальдегід Фенілформальдегід |
| Інші назви | Бензойний альдегід |
| Ідентифікатори | |
| Номер CAS | 100-52-7 |
| PubChem | 240 |
| Номер EINECS | 202-860-4 |
| Номер EC | 202-860-4 |
| KEGG | D02314 |
| ChEBI | 17169 |
| RTECS | CU437500 |
| SMILES | O=Cc1ccccc1 |
| InChI | 1/C7H6O/c8-6-7-4-2-1-3-5-7/h1-6H |
| Номер Бельштейна | 471223 |
| Властивості | |
| Молекулярна формула | C7H6O |
| Молярна маса | 106,12 г/моль |
| Зовнішній вигляд | безбарвна або жовтувата рідина сильно заломлююча |
| Запах | схожий на мигдаль |
| Густина | 1.0415 g/ml, рідина |
| Тпл | -26 |
| Розчинність (вода) | 0.3 g/100 mL (20 °C)[1] |
| Розчинність | розчинний у рідкому амоніаці |
| Кислотність (pKa) | 14.90 |
| Показник заломлення (nD) | 1.5456 |
| В'язкість | 1.321 cP (25 °C) |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
−36.8 kJ/mol |
| Ст. ентальпія згоряння ΔcH 298 |
−3525.1 kJ/mol |
| Небезпеки | |
| ЛД50 | 1300 mg/kg (rat, oral) |
| MSDS | J. T. Baker |
| Класифікація ЄС | Harmful (Xn) |
| R-фрази | R22 |
| S-фрази | S2, S24 |
| NFPA 704 | |
| Вибухові границі | 1.4-8.5 % |
| Пов'язані речовини | |
| Пов'язані речовини | Бензиловий спирт Бензойна кислота |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Основним способами промислового отримання бензальдегіду є хлорування та окислення толуену. Відомо й багато альтернативних шляхів зокрема окислення бензилового спирту та карбонілювання бензену .[5]
Вступає в усі типові реакції приєднання нуклеофілів по альдегідній групі
Де Nu- може бути HSO3-, CN-, HCC-
З бензальдегідом може бути проведена Реакція Канніццаро[6], Бензоїнова конденсація та інші реакції конденсації де він виступає карбонільною компонентою
Бензальдегід селективно нітрується в мета положення

Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.



