Xenontetraoxid
From Wikipedia, the free encyclopedia
Xenontetraoxid är en kemisk förening av xenon och syre med formeln XeO4. Ämnet är något så ovanligt som en relativt stabil ädelgasförening. Det är bara i fast form (under −35,9 °C) som ämnet är stabilt, över smältpunkten är ämnet explosivt. Vid explosion sönderfaller xenontetraoxid till xenon och syrgas (ΔH = −643 kJ/mol) enligt följande reaktionsformel:[2][3]
| Xenontetraoxid | |
 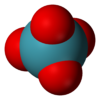 | |
| Systematiskt namn | Xenon(VIII)tetroxid |
|---|---|
| Övriga namn | Perxenicanhydrid |
| Kemisk formel | XeO4 |
| Molmassa | 195,29 g/mol |
| Utseende | Färglös gas eller gula kristaller (under -36 °C) |
| CAS-nummer | 12340-14-6 |
| SMILES | [O-][Xe+4]([O-])([O-])[O-] |
| Egenskaper | |
| Smältpunkt | -35,9 °C |
| Kokpunkt | 0[1] °C |
| Faror | |
| Huvudfara | |
| SI-enheter & STP används om ej annat angivits | |
Alla åtta valenselektronerna av xenon är involverade i bindningarna med syret, och oxidationstillståndet för xenonatomen är +8. Syre är det enda elementet som kan föra xenon upp till sitt högsta oxidationstillstånd, men även fluor kan bara ge XeF6 (+6).
Två andra kortlivade xenonföreningar med ett oxidationstillstånd av +8, XeO3F2 och XeO2F4, är tillgängliga genom reaktion av xenontetroxid med xenonhexafluorid. Vidare kan XeO3F2 och XeO2F4 identifieras med masspektrometri. Perxenaterna är också föreningar där xenon har oxidationstillståndet +8.
