From Wikipedia, the free encyclopedia
Херпес симплек вирус (акроним ХСВ) или ХСВ-1 и ХСВ-2, такође познати под својим таксономским називима Људски алфахерпесвирус 1 и Људски алфахерпесвирус 2, су два члана из хумане породице Herpesviridae, групе новијих вируса који производе вирусне инфекције код већине људи.[1][2] И ХСВ-1 (који производи већину херпеса) и ХСВ-2 (који производи већину гениталног херпеса) су уобичајени и заразни, и могу се пренети када заражена особа почне да преноси вирус.
| Херпес симплекс вирус | |
|---|---|
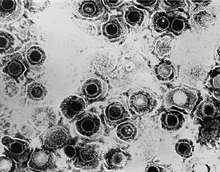 | |
| Микрографија херпес симплекс вируса | |
| Научна класификација | |
| (нерангирано): | Virus |
| Realm: | Duplodnaviria |
| Царство: | Heunggongvirae |
| Тип: | Peploviricota |
| Класа: | Herviviricetes |
| Ред: | Herpesvirales |
| Породица: | Herpesviridae |
| Потпородица: | Alphaherpesvirinae |
| Род: | Simplexvirus |
| Укључене групе | |
| |
| Кладистички укључене, мада традиционално искључене из таксона | |
|
All other Simplexvirus spp.:
| |
Око 67% светске популације млађе од 50 година има ХСВ-1.[3] У Сједињеним Америчким Државама се верује да је око 47,8% особа заражено ХСВ-1, а 11,9% особа ХСВ-2.[4] Пошто се може пренети било којим интимним контактом, спада у групу изазивача најчешћих полно преносивих инфекција.[5]
ХСВ-1 и ХСВ-2 се преносе контактом са зараженом особом која има реактивацију вируса.
ХСВ-2 се периодично излучује преко људских гениталних органа, најчешће код асимптоматских облика. Већина сексуалних преноса се дешава током периода асимптоматске реактивације инфекције.[6] Асимптоматска реактивација значи да вирус изазива атипичне, суптилне или тешко уочљиве симптоме који нису идентификовани као активна херпес инфекција, тако да је стицање вируса могуће чак и ако нема активних ХСВ пликова или раница.
У једној студији, дневни узорци брисева гениталних органа открили су ХСВ-2 у просеку у 12–28% случајева међу онима који су имали епидемију и у 10% међу онима који пате од асимптоматске инфекције, при чему су се многе од ових епизода дешавале без видљивих манифестација („субклинички осип“).[7]
У другој студији, 73 субјекта су рандомизована да примају валацикловир 1 грам дневно или плацебо током 60 дана сваки у двосмерном унакрсном дизајну. Дневни брис гениталног подручја је самостално узет за детекцију ХСВ-2 ланчаном реакцијом полимеразе, да би се упоредио ефекат валацикловира у односу на плацебо на асимптоматским излучивањем вируса код имунокомпетентних, ХСВ-2 серопозитивних субјеката без историје симптоматске инфекције гениталног херпеса. Студија је открила да је валацикловир значајно смањио излучивање током субклиничких дана у поређењу са плацебом, показујући смањење од 71%; док 84% испитаника није имало осип док су примали валацикловир у односу на 54% испитаника који су били а плацебу. Око 88% пацијената лечених валацикловиром није имало препознате знакове или симптоме у односу на 77% код плацеба.[8]
За ХСВ-2, субклиничко излучивање може представљати најзначајнији начин преношења.[7] Студије на нескладним партнерима (један заражен ХСВ-2, један не) показују да је стопа преношења приближно 5 на 10.000 сексуалних контаката.[9] Атипични симптоми се често приписују другим узроцима, као што је гљивична инфекција.
ХСВ-1 се често добија орално током детињства. Такође се може пренети полно, укључујући контакт са пљувачком, као што је љубљење и контакт уста са гениталијама (орални секс).[10]
ХСВ-2 је првенствено полно преносива инфекција, али стопа гениталних инфекција ХСВ-1 све више расте.[11]
Оба вируса се такође могу преносити вертикално током порођаја,[12] па се често вирус назива „негенитални херпес симплекс вирус“.[13] Међутим, ризик од преношења инфекције је минималан ако мајка нема симптоме или пликове током порођаја. Ризик је значајнији када се мајка први пут зарази вирусом током касне трудноће.[14]
Супротно популарним митовима, херпес се не може пренети са површина као што су тоалетне даске јер вирус херпеса почиње да умире одмах по изласку из тела.[15] Иако херпес симплекс вируси могу утицати на делове коже који су изложена контакту са зараженом особом. Пример за то је херпес инфекција прстију, нпр. стоматолога пре рутинске употребе рукавица приликом лечења пацијената.[16] Руковање са зараженом особом не преноси ову болест.


Сви вируси херпеса код животиња имају нека заједничка својства. Структура херпес вируса састоји се од релативно великог, дволанчаног, линеарног ДНК генома умотаног у икосаедарски протеински кавез који се зове капсид, који је умотан у липидни двослој који се назива омотач. Коверта је спојена са капсидом помоћу тегумента. Ова потпуна честица је позната као вирион.[18] Сваки од ХСВ-1 и ХСВ-2 садржи најмање 74 гена (или отворених оквира читања, ОРФ) унутар својих генома,[19] иако спекулације о гомилању гена дозвољавају чак 84 јединствена гена који кодирају протеине помоћу 94 наводна ОРФ-а.[20] Ови гени кодирају различите протеине укључене у формирање капсида, тегумента и омотача вируса, као и контролу репликације и инфективности вируса. Ови гени и њихове функције су приказани у табели испод.
Геноми ХСВ-1 и ХСВ-2 су сложени и садрже два јединствена региона који се називају дуги јединствени регион (УЛ) и кратки јединствени регион (УС). Од 74 позната ОРФ-а, УЛ садржи 56 вирусних гена, док УС садржи само 12.[19] Транскрипцију ХСВ гена катализује РНК полимераза ИИ инфицираног домаћина.[19] Непосредни рани гени, који кодирају протеине који регулишу експресију раних и касних вирусних гена, први су који се експримирају након инфекције. Следи рана експресија гена, како би се омогућила синтеза ензима укључених у репликацију ДНК и производњу одређених гликопротеина омотача. Експресија касних гена се дешава последња; ова група гена претежно кодира протеине који формирају вирионску честицу.[19]
Пет протеина из (УЛ) формирају вирусни капсид - УЛ6, УЛ18, УЛ35, УЛ38 и главни капсид протеин УЛ19.[18]
Улазак ХСВ-а у ћелију домаћина укључује везивање неколико гликопротеина на површини вируса са омотачем за њихове трансмембранске рецепторе на површини ћелије. Многи од ових рецептора се затим повлаче према унутра од стране ћелије, за коју се сматра да отвара прстен од три хетеродимера гХгЛ који стабилизују компактну конформацију гБ гликопротеина, тако да он избија и пробија ћелијску мембрану.[21] Омотач који покрива вирусну честицу се затим спаја са ћелијском мембраном, стварајући пору кроз коју садржај вирусног омотача улази у ћелију домаћина.
Узастопне фазе уласка ХСВ-а су аналогне онима код других вируса. У почетку, комплементарни рецептори на вирусу и на површини ћелије доводе вирус и ћелијске мембране у близину. Интеракције ових молекула затим формирају стабилну улазну пору кроз коју се садржај вирусног омотача уноси у ћелију домаћина. Вирус се такође може ендоцитозирати након везивања за рецепторе, а фузија се може десити на ендосому. На електронским микрографијама, спољни листићи вирусног и ћелијског липидног двослоја су виђени спојени;[22] ова хемифузија може бити на уобичајеном путу ка уласку или обично може бити заустављено стање које је вероватније да ће бити заробљено него пролазни механизам уласка.
У случају херпес вируса, почетне интеракције се јављају када се два вирусна гликопротеина омотача названа гликопротеин Ц (гЦ) и гликопротеин Б (гБ) вежу за честицу на површини ћелије која се зове хепаран сулфат. Затим, главни протеин који везује рецепторе, гликопротеин Д (гД), везује се специфично за најмање један од три позната улазна рецептора.[тражи се извор] Ови ћелијски рецептори укључују посредник уласка херпесвируса (ХВЕМ), нектин-1 и 3-О сулфатни хепаран сулфат. Нектински рецептори обично производе адхезију ћелија-ћелија, да би обезбедили јаку тачку везивања вируса за ћелију домаћина.[21] Ове интеракције доводе површине мембране у међусобну близину и омогућавају другим гликопротеинима уграђеним у омотач вируса да ступе у интеракцију са другим молекулима површине ћелије. Једном везан за ХВЕМ, гД мења своју конформацију и ступа у интеракцију са вирусним гликопротеинима Х (гХ) и Л (гЛ), који формирају комплекс. Интеракција ових мембранских протеина може довести до стања хемифузије. гБ интеракција са гХ/гЛ комплексом ствара улазне поре за вирусни капсид.[22] гБ ступа у интеракцију са гликозаминогликанима на површини ћелије домаћина
Након што вирусни капсид уђе у ћелијску цитоплазму, транспортује се до језгра ћелије. Једном када се закачи за језгро у нуклеарној улазној пору, капсид избацује свој ДНК садржај преко каписног портала. Капсидни портал је формиран од 12 копија порталног протеина, УЛ6, распоређених у облику прстена; протеини садрже леуцински рајсфершлус секвенцу аминокиселина, што им омогућава да се приањају једни за друге.[23] Сваки икосаедарски капсид садржи један портал, смештен у једном тјемену.[24] ДНК излази из капсида у једном линеарном сегменту.[25]
ХСВ избегава имунолошки систем преко интерференције са презентацијом антигена МХЦ класе И на површини ћелије, блокирањем транспортера повезаног са обрадом антигена (ТАП) индукованог секрецијом ИЦП-47 од стране ХСВ. У ћелији домаћину, ТАП преноси дигестивне пептиде епитопа вирусног антигена из цитосола у ендоплазматски ретикулум, омогућавајући да се ови епитопи комбинују са молекулима МХЦ класе И и представе на површини ћелије. Презентација вирусног епитопа са МХЦ класе И је предуслов за активацију цитотоксичних Т-лимфоцита (ЦТЛ), главних ефектора имуног одговора посредованог ћелијама против ћелија инфицираних вирусом. ИЦП-47 спречава покретање ЦТЛ одговора на ХСВ, омогућавајући вирусу да преживи дужи период у домаћину.[26] ХСВ обично производи цитопатски ефекат (ЦПЕ) у року од 24-72 сата након инфекције у пермисивним ћелијским линијама, што се примећује класичним формирањем плака. Међутим, пријављени су и клинички изолати ХСВ-1 који нису показали никакав ЦПЕ у Веро и А549 ћелијским културама током неколико пасуса са ниским нивоом експресије протеина вируса. Вероватно ови изолати ХСВ-1 еволуирају ка „загонетнијем“ облику да би се успоставила хронична инфекција и на тај начин открила још једну стратегију за избегавање имунолошког система домаћина, осим неуронске латенције.[27]

Након инфекције ћелије, производи се каскада протеина вируса херпеса, који се називају непосредно рани, рани и касни. Истраживање помоћу проточне цитометрије на другом члану породице херпес вируса, херпесвирусу повезаном са Капосијевим саркомом, указује на могућност додатног литичког стадијума, одложено-касно.[28] Ове фазе литичке инфекције, посебно касне литичке, разликују се од фазе латенције. У случају ХСВ-1, протеински производи се не детектују током латенције, док се детектују током литичког циклуса.
Рани транскрибовани протеини се користе у регулацији генетске репликације вируса. Приликом уласка у ћелију, α-ТИФ протеин се придружује вирусној честици и помаже у непосредној раној транскрипцији. Протеин за затварање вириона (ВХС или УЛ41) је веома важан за репликацију вируса.[29] Овај ензим искључује синтезу протеина у домаћину, разграђује мРНК домаћина, помаже у репликацији вируса и регулише експресију гена вирусних протеина. Вирусни геном одмах путује у језгро, али ВХС протеин остаје у цитоплазми.[30][29]
Касни протеини формирају капсид и рецепторе на површини вируса. Паковање вирусних честица - укључујући геном, језгро и капсид - се дешава у језгру ћелије. Овде се конкатемери вирусног генома раздвајају цепањем и стављају у формиране капсиде. ХСВ-1 пролази кроз процес примарног и секундарног омотача. Примарни омотач се добија пупањем у унутрашњу нуклеарну мембрану ћелије. Ово се затим спаја са спољном нуклеарном мембраном. Вирус добија свој коначни омотач пупањем у цитоплазматске везикуле.[31]
ХСВ-ови могу опстати у мирном, али упорном облику познатом као латентна инфекција, посебно у нервним ганглијама.[1] ХСВ-1 има тенденцију да борави у тригеминалним ганглијима, док ХСВ-2 има тенденцију да борави у сакралним ганглијима, али то су само тенденције, а не фиксно понашање. Током латентне инфекције ћелије, ХСВ експримирају РНК транскрипта повезану са латенцијом (ЛАТ). ЛАТ регулише геном ћелије домаћина и омета природне механизме ћелијске смрти. Одржавањем ћелија домаћина, експресија ЛАТ чува резервоар вируса, што омогућава накнадне, обично симптоматске, периодичне рецидиве или „избијања“ карактеристичне за нелатентност. Без обзира на то да ли су рецидиви симптоматски или не, долази до ослобађања вируса да би се инфицирао нови домаћин.
Протеин који се налази у неуронима може се везати за ДНК вируса херпеса и регулисати латенцију. ДНК вируса херпеса садржи ген за протеин назван ИЦП4, који је важан трансактиватор гена повезаних са литичком инфекцијом код ХСВ-1.[32] Елементи који окружују ген за ИЦП4 везују протеин познат као хумани неуронски протеин неуронски рестриктивни фактор утишавања (НРСФ) или фактор транскрипције утишавања елемента репресора човека (РЕСТ). Када се веже за елементе вирусне ДНК, деацетилација хистона се дешава на врху ИЦП4 генске секвенце како би се спречило покретање транскрипције са овог гена, чиме се спречава транскрипција других вирусних гена укључених у литички циклус.[32] Други ХСВ протеин преокреће инхибицију синтезе протеина ИЦП4. ИЦП0 одваја НРСФ од ИЦП4 гена и на тај начин спречава утишавање вирусне ДНК.[33]
ХСВ геном се састоји од два јединствена сегмента, названа јединствени дуги (УЛ) и јединствени кратки (УС), као и терминалних инвертираних понављања пронађених на два краја названа дуго понављање (РЛ) и кратко понављање (РС). Постоје и мањи елементи „залиха терминала“ (α) који се налазе на даљим крајевима РС. Укупан распоред је РЛ-УЛ-РЛ-α-РС-УС-РС-α са сваким паром понављања који се међусобно инвертују. Цела секвенца се затим капсулира у терминалну директну понављање. Дуги и кратки делови имају своје порекло репликације, при чему се ОриЛ налази између УЛ28 и УЛ30 и ОриС који се налази у пару близу РС.[34] Како се Л и С сегменти могу саставити у било ком смеру, они се могу слободно окретати један у односу на други, формирајући различите линеарне изомере.[35]
| ОРФ | Лажни протеин | ХСВ-1 | ХСВ-2 | Функција/опис |
|---|---|---|---|---|
| Дуго понављање (RL) | ||||
| ICP0/RL2 | ICP0; IE110; α0 | P08393 | P28284 | E3 убиквитин лигаза која активира транскрипцију вирусног гена супротстављајући се хроматинизацији вирусног генома и супротставља се интринзичним и антивирусним одговорима заснованим на интерферону. |
| RL1 | RL1; ICP34.5 | O12396 | Фактор неуровируленције. Антагонизира ПКР дефосфорилацијом еИФ4а. Веже се за БЕЦН1 и инактивира аутофагију. | |
| LAT | LRP1, LRP2 | P17588
P17589 |
Транскрипт повезан са кашњењем и протеински производи (протеини повезани са кашњењем) | |
| Јединствена дуга (UL) | ||||
| UL1 | Glycoprotein L | P10185 | Површина и мембрана | |
| UL2 | UL2 | P10186 | Урацил-ДНК гликозилаза | |
| UL3 | UL3 | P10187 | Непознат | |
| UL4 | UL4 | P10188 | Непознат | |
| UL5 | UL5 | Q2MGV2 | ДНК репликација | |
| UL6 | Портални протеин UL-6 | P10190 | Дванаест од ових протеина чине каписдни портални прстен кроз који ДНК улази и излази из капсида. | |
| UL7 | UL7 | P10191 | Сазревање вириона | |
| UL8 | UL8 | P10192 | Протеин повезан са комплексом ДНК вируса хеликазе и примазе | |
| UL9 | UL9 | P10193 | Протеин који се везује пореко репликације | |
| UL10 | Glycoprotein M | P04288 | Површина и мембрана | |
| UL11 | UL11 | P04289 | Излаз вириона и секундарни омотач | |
| UL12 | UL12 | Q68978 | Алкална ексонуклеаза | |
| UL13 | UL13 | Q9QNF2 | Серин-треонин протеин киназа | |
| UL14 | UL14 | P04291 | Тегумент протеин | |
| UL15 | Terminase | P04295 | Обрада и паковање ДНК | |
| UL16 | UL16 | P10200 | Тегумент протеин | |
| UL17 | UL17 | P10201 | Обрада и паковање ДНК | |
| UL18 | VP23 | P10202 | Капсидни протеин | |
| UL19 | VP5; ICP5 | P06491 | Главни капсидни протеин | |
| UL20 | UL20 | P10204 | Мембрански протеин | |
| UL21 | UL21 | P10205 | Тегумент протеин | |
| UL22 | Glycoprotein H | P06477 | Површина и мембрана | |
| UL23 | Thymidine kinase | O55259 | Периферна репликација ДНК | |
| UL24 | UL24 | P10208 | Непознат | |
| UL25 | UL25 | P10209 | Обрада и паковање ДНК | |
| UL26 | P40; VP24; VP22A; UL26.5 (HHV2 кратка изоформа) | P10210 | P89449 | Капсидни протеин |
| UL27 | Glycoprotein B | A1Z0P5 | Површина и мембрана | |
| UL28 | ICP18.5 | P10212 | Обрада и паковање ДНК | |
| UL29 | UL29; ICP8 | Q2MGU6 | Главни протеин који везује ДНК | |
| UL30 | DNA polymerase | Q4ACM2 | ДНК репликација | |
| UL31 | UL31 | Q25BX0 | Протеин нуклеарног матрикса | |
| UL32 | UL32 | P10216 | Гликопротеин омотача | |
| UL33 | UL33 | P10217 | Обрада и паковање ДНК | |
| UL34 | UL34 | P10218 | Протеин унутрашње нуклеарне мембране | |
| UL35 | VP26 | P10219 | Капсидни протеин | |
| UL36 | UL36 | P10220 | Протеин великог тегумента | |
| UL37 | UL37 | P10216 | Састављање капсида | |
| UL38 | UL38; VP19C | P32888 | Састављање капсида и сазревање ДНК | |
| UL39 | UL39; RR-1; ICP6 | P08543 | Рибонуклеотид редуктаза (мала подјединица) | |
| UL40 | UL40; RR-2 | P06474 | Рибонуклеотид редуктаза (мала подјединица) | |
| UL41 | UL41; VHS | P10225 | Тегумент протеин; искључивање домаћина вириона | |
| UL42 | UL42 | Q4H1G9 | Фактор процесивности ДНК полимеразе | |
| UL43 | UL43 | P10227 | Мамбрански протеин | |
| UL44 | Glycoprotein C | P10228 | Површина и мембрана | |
| UL45 | UL45 | P10229 | Мембрански протеин; Ц-тип лектина | |
| UL46 | VP11/12 | P08314 | Тегумент протеини | |
| UL47 | UL47; VP13/14 | P10231 | Тегумент протеини | |
| UL48 | VP16 (Alpha-TIF) | P04486 | Сазревање вириона; активирају ИЕ гене интеракцијом са ћелијским транскрипционим факторима Оцт-1 и ХЦФ. Везује се за секвенцу5'TAATGARAT3'. | |
| UL49 | UL49A | O09800 | Протеин омотача | |
| UL50 | UL50 | P10234 | dUTP дифосфатаза | |
| UL51 | UL51 | P10234 | Тегумент протеини | |
| UL52 | UL52 | P10236 | Протеин комплекса ДНК хеликазе/примазе | |
| UL53 | Glycoprotein K | P68333 | Површина и мембрана | |
| UL54 | IE63; ICP27 | P10238 | Регулација транскрипције и инхибиција СТИНГ сигналома | |
| UL55 | UL55 | P10239 | Непознат | |
| UL56 | UL56 | P10240 | Непознат | |
| Обрнуто понављање дуго (IRL) | ||||
| Обрнуто понављање кратко (IRS) | ||||
| Јединствено кратко (US) | ||||
| US1 | ICP22; IE68 | P04485 | Репликација вируса | |
| US2 | US2 | P06485 | Непознат | |
| US3 | US3 | P04413 | Серин/треонин-протеин киназа | |
| US4 | Glycoprotein G | P06484 | Површина и мембрана | |
| US5 | Glycoprotein J | P06480 | Површина и мембрана | |
| US6 | Glycoprotein D | A1Z0Q5 | Површина и мембрана | |
| US7 | Glycoprotein I | P06487 | Површина и мембрана | |
| US8 | Glycoprotein E | Q703F0 | Површина и мембрана | |
| US9 | US9 | P06481 | Тегумент протеин | |
| US10 | US10 | P06486 | Капсид/Тегумент протеин | |
| US11 | US11; Vmw21 | P56958 | Везује ДНК и РНК | |
| US12 | ICP47; IE12 | P03170 | Инхибира пут МХЦ класе 1 спречавањем везивања антигена за ТАП | |
| Кратко понављајући терминал (TRS) | ||||
| RS1 | ICP4; IE175 | P08392 | Главни активатор транскрипције. Неопходан за напредовање након непосредне ране фазе инфекције. ИЕГ репресор транскрипције. | |
Геноми херпес симплекса 1 могу се класификовати у шест класа.[36] Четири од њих се јављају у источној Африци, један у источној Азији и један у Европи и Северној Америци. Ово сугерише да вирус можда потиче из источне Африке. Чини се да је најновији заједнички предак евроазијских сојева еволуирао пре око 60.000 година.[37] Источноазијски изолати ХСВ-1 имају необичан образац који се тренутно најбоље објашњава са два таласа миграција одговорних за насељавање Јапана.[37]
Херпес симплек 2 геноми се могу поделити у две групе: једна је глобално распрострањена, а друга је углавном ограничена на подсахарску Африку.[38] Глобално распрострањени генотип је прошао кроз четири древне рекомбинације са херпес симплексом 1. Такође је објављено да ХСВ-1 и ХСВ-2 могу имати савремене и стабилне догађаје рекомбинације код домаћина који су истовремено инфицирани са оба патогена. Сви случајеви су ХСВ-2 који преузима делове ХСВ-1 генома, понекад мењајући у еволуционом процесу делове епитопа антигена.[39]
Стопа мутације је процењена на ~1,38×10−7 супституција/локацији/години.[36] У клиничком окружењу, мутације у гену тимидин киназе или гену ДНК полимеразе изазвале су отпорност на ацикловир. Међутим, већина мутација се јавља у гену тимидин киназе, а не у гену ДНК полимеразе.[40]
Друга анализа је проценила да је стопа мутације у геному херпес симплекса 1 1,82×10−8 супституција нуклеотида по месту годишње. Ова анализа је поставила најновијег заједничког претка овог вируса пре ~710.000 година.[41]
Херпес симплекс 1 и 2 су се раздвојили у два посебна подтипа пре око 6 милиона година.[39]
Многи од оних који су заражени никада не развију симптоме.[тражи се извор] Симптоми, када се појаве, могу укључивати воденасте пликове на кожи или слузокожи уста, усана, носа или гениталија,[1] или очију (очни херпес).[тражи се извор] Лезије лече крастама карактеристичним за херпетичну болест. Понекад вируси изазивају благе или атипичне симптоме током избијања. Међутим, они такође могу изазвати проблематичније облике херпес симплекса. Као неуротропни и неуроинвазивни вируси, ХСВ-1 и -2 опстају у телу скривајући се од имуног система у ћелијским телима неурона. Након почетне или примарне инфекције, неки заражени људи доживљавају спорадичне епизоде вирусне реактивације или избијања. У избијању, вирус у нервној ћелији постаје активан и транспортује се преко аксона неурона до коже, где долази до умножавања и избацивања вируса и изазива нове ране.[тражи се извор]


Херпес вируси успостављају доживотне инфекције (и стога се не могу искоренити из тела).[42]
Третман обично укључује антивирусне лекове опште намене који ометају репликацију вируса, смањују физичку тежину лезија повезаних са епидемијом и смањују могућност преношења на друге. Студије рањивих популација пацијената су показале да свакодневна употреба антивирусних лекова као што су ацикловир[43] валацикловир може смањити стопе реактивације.[44] Екстензивна употреба антихерпетичких лекова довела је до развоја резистенције на лекове, што заузврат доводи до неуспеха лечења. Стога се нови извори лекова широко истражују како би се решио проблем. У јануару 2020. објављен је опсежан прегледни чланак који је показао ефикасност природних производа као обећавајућих лекова против ХСВ.[45]
Пиритион, јонофор цинка, показује антивирусну активност против вируса херпес симплекса.[46]
Реактивација вишеструкости (МР) је процес којим вирусни геноми који садрже оштећење међусобно делују унутар заражене ћелије да би створили одрживи вирусни геном. МР је првобитно откривен са бактеријским вирусом бактериофагом Т4, али је потом пронађен и код патогених вируса, укључујући вирус грипа, ХИВ-1, аденовирусни симиан вирус 40, вирус вакциније, реовирус, полиовирус и вирус херпес симплекса.[47]
Када су ХСВ честице изложене дозама агенса који оштећује ДНК који би био смртоносан у појединачним инфекцијама, али им се затим дозволи да се подвргну вишеструкој инфекцији (два или више вируса у ћелији домаћина), примећује се реактивација вишеструкости. Побољшано преживљавање ХСВ-1 услед реактивације вишеструкости настаје након излагања различитим агенсима који оштећују ДНК, укључујући метил метансулфонат,[48] триметилпсорален (који узрокује умрежавање ДНК у ланцима)[49][50] и УВ светлост.[51]
Након третмана генетски обележеног ХСВ триметилпсораленом, повећава се рекомбинација између обележених вируса, што сугерише да оштећење триметилпсоралена стимулише рекомбинацију. Изгледа да реактивација вишеструкости ХСВ делимично зависи од рекомбинационих функција за поправку ћелија домаћина, јер ћелије фибробласта коже оштећене у оквиру ове функције (ћелије пацијената са Блумовим синдромом) немају реактивацију вишеструкости.[51]
Ова запажања сугеришу да реактивација вишеструкости код ХСВ инфекција укључује генетску рекомбинацију између оштећених вирусних генома што резултује производњом одрживих вируса потомака. ХСВ-1, након заразе ћелија домаћина, изазива упалу и оксидативни стрес.[52] Стога се чини да геном ХСВ може бити изложен оксидативном оштећењу ДНК током инфекције, а да реактивација вишеструкости може побољшати преживљавање вируса и вируленцију под овим условима.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.