Fosfat, je u neorganskoj hemiji so fosforne kiseline. U organskoj hemiji, fosfat, ili organofosfat, je estar fosforne kiseline. Organski fosfati su važni u biohemiji i biogeohemiji ili ekologiji. Neorganiski fosfati se iskopavaju da bi se dobio fosfor za upotrebu u agrikulturi i industriji.[5][6][7] Na povišenim temperaturama u čvrstom stanju, fosfati mogu da se kondenzuju i formiraju pirofosfate.
 | |||
| |||
| Nazivi | |||
|---|---|---|---|
| Sistemski naziv
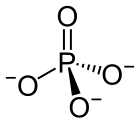
Fosfat[1] | |||
| Identifikacija | |||
3D model () |
|||
| Bajlštajn | 3903772 | ||
| Gmelin Referenca | 1997 | ||
| MeSH | Phosphates | ||
| UNII | |||
| Svojstva | |||
| Molarna masa | |||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 ° [77 °], 100 ). | |||
| Reference infokutije | |||


Hemijske osobine
Fosfatni jon je poliatomski jon sa empirijskom formulom 43− i molarnom masom od 94.973 g/mol. On se sastoji od jednog centralnog atoma fosfora atom okruženog sa četiri atoma kiseonika u tetraedarskoj konfiguraciji. Fosfatni jon nosi tri negativa formalna naelektrisanja i on je konjugovana baza hidrogen fosfatnog jona, 42-, koji je konjugovana baza 24-, dihidrogen fosfatnog jona, koji je konjugovana baza 3PO4, fosforne kiseline. On je hipervalentni molekul (atom fosfora ima 10 elektrona u svojoj valentnoj ljuski). Fosfat je takođe organofosforno jedinjenje sa formulom .
Fosfatne soli se formiraju kad se pozitivno-naelektrisani jon veže za negativno-naelektrisane atome kiseonika, formirajući jonsko jedinjenje. Mnogi fosfati nisu rastvorni u vodi na standardnoj temperaturi i pritisku. Natrijum, kalijum, rubidijum, cezijum i amonijum fosfati su rastvorni u vodi. Većina drugih fosfata su veoma malo rastvorni ili nerastvorni u vodi. Kao pravilo, hidrogen i dihidrogen fosfati su nešto rastvorniji od korespondirajućih fosfata. Pirofosfati su uglavnom rastvorni u vodi.
U razređenim vodenim rastvorima, fosfat postoji u četiri oblika. U jako-baznoj sredini, fosfatni jon (43−) predominira, dok u slabo-baznim uslovima, hidrogen fosfatni jon (42−) je prevalentan. U slabo-kiselim uslovima, dihidrogen fosfatni jon () je najzastupljeniji. U jako-kiseloj sredini, fosforna kiselina () je glavna forma.
Precizniji, polazeći od sledeće tri ravnotežne reakcije:
- ⇌ +
- ⇌ +
- ⇌ +
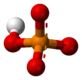
korespondirajuće konstante disocijacije na 25 ° (u mol/L) su:
- (pKa1 2.12)
- (pKa2 7.21)
- (pKa3 12.67)
Reference
Spoljašnje veze
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.





![{\displaystyle K_{a1}={\frac {[{\mbox{H}}^{+}][{\mbox{H}}_{2}{\mbox{PO}}_{4}^{-}]}{[{\mbox{H}}_{3}{\mbox{PO}}_{4}]}}\simeq 7.5\times 10^{-3}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/7e81fc5d22c187e5acc19c15b8422a604474b916)
![{\displaystyle K_{a2}={\frac {[{\mbox{H}}^{+}][{\mbox{HPO}}_{4}^{2-}]}{[{\mbox{H}}_{2}{\mbox{PO}}_{4}^{-}]}}\simeq 6.2\times 10^{-8}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/c10e3502ce38d504ebf659f7411f2d2f24015c25)
![{\displaystyle K_{a3}={\frac {[{\mbox{H}}^{+}][{\mbox{PO}}_{4}^{3-}]}{[{\mbox{HPO}}_{4}^{2-}]}}\simeq 2.14\times 10^{-13}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/42097ca31fd0468791802af675f407bda4e4c871)
