From Wikipedia, the free encyclopedia
Natrijev hidrogenkarbonat, tudi ali natrijev bikarbonat, soda bikarbona ali bikarbona[7], je sol, tvorjena iz natrija in hidrogenkarbonata. Ker nastane v reakciji nevtralizacije iz natrijevega hidroksida, ki je močna baza, in šibke ogljikove kisline, izkazuje bazičen pH (okoli 9) in zato reagira s kislinami (reakcija kislin s karbonati) zelo burno, pri tem pa nastanejo sol (natrij + nekovina), ogljikov dioksid (CO2) in voda (H2O). Reakcija kislin z natrijevim hidrogenkarbonatom lahko poteče v vodni raztopini in pa v trdnem agregatnem stanju.
 | |||
| |||
 | |||
| Imena | |||
|---|---|---|---|
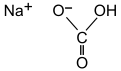
| IUPAC ime
Natrijev hidrogenkarbonat | |||
| Druga imena
soda bikarbona, natrijev bikarbonat | |||
| Identifikatorji | |||
3D model (JSmol) |
|||
Beilstein |
4153970 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.122 | ||
| EC število |
| ||
| Število E | E500(ii) (sredstva za uravnavanje Ph, ...) | ||
| KEGG | |||
| MeSH | Sodium+bicarbonate | ||
PubChem CID |
|||
| RTECS število |
| ||
| UNII | |||
CompTox Dashboard (EPA) |
|||
| |||
| |||
| Lastnosti | |||
| NaHCO 3 | |||
| Molska masa | 84,007 g mol−1 | ||
| Videz | beli kristali | ||
| Vonj | brez vonja | ||
| Gostota | 2,20 g cm−3[1] | ||
| Tališče | 50 °C (122 °F; 323 K) | ||
| 9 g/100 mL
69 g/L (0 °C)[2] | |||
| Topnost | aceton: 0,02 %wt, metanol: 2,13 %wt pri 22 °C[4]. netopen v etanolu | ||
| log P | -0.82 | ||
| Kislost (pKa) | 10,329[5]
6,351 (ogljikova kislina)[5] | ||
| Lomni količnik (nD) | 1,3344 | ||
| Farmakologija | |||
| Aplikacija zdravila | intravensko, peroralno | ||
| Termokemija | |||
| Standardna molarna entropija S |
102 J·mol−1·K−1[6] | ||
Std tvorbena entalpija (ΔfH⦵298) |
−948 kJ·mol−1[6] | ||
| Nevarnosti | |||
| Glavne nevarnosti | Povzroča hudo draženje oči. | ||
| NFPA 704 (diamant ognja) | |||
| Smrtni odmerek ali koncentracija (LD, LC): | |||
LD50 (srednji odmerek) |
4,22 g kg−1 | ||
| Sorodne snovi | |||
| Drugi anioni | natrijev karbonat | ||
| Drugi kationi | amonijev hidrogenkarbonat | ||
| Sorodne snovi | natrijev hidrogensulfat natrijev hidrogenfosfat | ||
| Sklici infopolja | |||
Sol je ena redkih hidrogenkarbonatov, ki so topni v vodi, sicer pa je njena topnost precej majhna.
Pri segrevanju razpade na natrijev karbonat (Na2CO3), vodo (H2O) in ogljikov(IV) oksid (CO).
Sproščeni plin je "kriv" za vzhajanje testa in rahlost peciv.
Je glavna sestavina pecilnega praška.
Natrijev hidrogenkarbonat se uporablja kot antacid (nevtralizira želodčno kislino)[8] ter kot sredstvo proti presnovni acidozi[7].
Za nevtraliziranje želodčne kisline se uporablja natrijev hidrogenkarbonat peroralno (z zaužitjem). V želodcu nevtralizira kislino in s tem oblaži zgago, dispepsijo in slabost zaradi prekomerne kislosti želodčnega soka. Primeren je za kratkotrajno lajšanje težav.[9]
Pri presnovni acidozi se uporablja parenteralno. Delovanje izhaja iz njegove fiziološke vloge v puferskem sistemu HCO3ˉ/CO2. V telo vnesen natrijev hidrogenkarbonat hitro absorbira vodikove ione iz zunajceličnega prostora in tako povzroči zvišanje pH v organizmu in tudi seč se naalkali. Pri reakciji med hidrogenkabonatnim anionom in vodikovim kationom nastane ogljikov dioksid, ki se izloči z dihanjem. Zaradi naalkaljenja seča se lahko natrijev hidrogenkarbonat daje tudi pri zastrupitvi s šibkimi organskimi kislinami (npr. barbiturati ali acetilsalicilno kislino), za izboljšanje topnosti zdravilnih učinkovin, ki so težko topne v nevtralnih ali kislih medijih (npr. metotreksat, sulfonamidi) in za naalkaljenje urina v primeru hemolize.[10]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.