chemická zlúčenina From Wikipedia, the free encyclopedia
Izoleucín (skratka Ile alebo I[1]) je α-aminokyselina, ktorá sa objavuje pri biosyntéze bielkovín. Obsahuje α-aminoskupinu (ktorá je za fyziologických podmienok v protónovanom stave −NH3+), α-karboxylovú skupinu (ktorá je za fyziologických podmienok v deprotónovanej forme −COO-) a uhľovodíkový bočný reťazec (s centrálnym atómom uhlíka viazanom na tri ďalšie atómy uhlíka). Je klasifikovaný ako nepolárna, nenabitá (pri fyziologickom pH), alifatická aminokyselina s rozvetveným reťazcom. Pre ľudí je nevyhnutný, čo znamená, že telo si ho nedokáže syntetizovať a musí byť prijímané v strave. Izoleucín sa syntetizuje z pyruvátu pomocou enzýmov biosyntézy leucínu v iných organizmoch, ako sú baktérie.[2] Je kódovaný kodónmi AUU, AUC a AUA.
| Izoleucín | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C6H13NO2 |
| Systematický názov | Kyselina (2S,3S)-2-amino-3-metylpentánová |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 131,175 g/mol |
| Ďalšie informácie | |
| Číslo CAS | L: 73-32-5 |
| SMILES | CC[C@H](C)[C@@H](C(=O)O)N |
| 3D model (JSmol) | Interaktívny 3D model |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Izoleucín je konštitučný izomér leucínu. Sú to jediné dve proteinogénne aminokyseliny s rovnakým sumárnym vzorcom, čo komplikuje ich rozlíšenie pri stanovení hmotnostnou spektrometriou peptidov. V takých prípadoch je možné ich súhrnne označiť skratkami Xle[3] alebo J.[3][4]
Izoleucín je možné syntetizovať viacstupňovým postupom z 2-brómbutánu a dietylmalonátu.[5] Syntetický izoleucín bol pôvodne opísaný v roku 1905 francúzskym chemikom Louisom Bouveaultom.[6]
Nemecký chemik Felix Ehrlich objavil izoleucín v roku 1903 v hemoglobíne.[chýba zdroj]

Izoleucín je esenciálna aminokyselina, takže sa v tele nesyntetizuje, preto sa musí prijímať v strave, zvyčajne ako súčasť bielkovín. V rastlinách a mikroorganizmoch sa syntetizuje v niekoľkých krokoch, počínajúc pyruvátom a alfa-ketobutyrátom. Enzýmy zapojené do tejto biosyntézy sú:[7]
Izoleucín je glukogénna aj ketogénna aminokyselina. Po transaminácii s alfa-ketoglutarátom sa uhlíkový skelet oxiduje a štiepi na propionyl-CoA a acetyl-CoA. Propionyl-CoA sa premieňa na sukcinyl-CoA, jeden z medziproduktov citrátového cyklu, ktorý sa môže premeniť na oxaloacetát a vstúpiť do glukoneogenézy (preto je izoleucín glukogénny). U cicavcov sa acetyl-CoA nemôže premeniť na uhľohydráty, ale môže vstúpiť do citrátového kondenzáciou s oxaloacetátom za vzniku citrátu, takisto sa môže použiť pri syntéze ketolátok (preto je izoleucín aj ketogénny) alebo mastných kyselín.[8]
Izoleucín, podobne ako iné aminokyseliny s rozvetveným reťazcom, je spojený s inzulínovou rezistenciou: v krvi diabetických myší, potkanov a ľudí sú pozorované vyššie hladiny izoleucínu.[9] Myši kŕmené jeden deň izoleucínovou deprivačnou diétou mali zlepšenú citlivosť na inzulín a kŕmenie izoleucínovou deprivačnou diétou počas jedného týždňa výrazne znížilo hladinu glukózy v krvi.[10] U obéznych myší (ktorých obezita bola dosiahnutá pomocou stravy) a myší rezistentných na inzulín mala diéta so zníženými hladinami izoleucínu (s alebo bez iných aminokyselín s rozvetveným reťazcom) za následok zníženie adipozity a zlepšenie citlivosti na inzulín.[11][12] Pre priaznivé metabolické účinky nízkobielkovinovej diéty sú potrebné nižšie hladiny izoleucínu v strave.[12] U ľudí diéta s obmedzeným množstvom bielkovín znižuje hladinu izoleucínu v krvi a znižuje hladinu glukózy v krvi nalačno.[13] Vyššia hladina izoleucínu v strave je u ľudí spojená s vyšším indexom telesnej hmotnosti.[12]
Aj keď sa táto aminokyselina u zvierat nevytvára, uchováva sa vo veľkých množstvách. Potraviny s vysokým obsahom izoleucínu zahŕňajú vajcia, sójový proteín, morské riasy, morčacie mäso, kuracie mäso, jahňacie mäso, syry a ryby.[14]
Výbor pre potravu a výživu (FNB) amerického Inštitútu medicíny stanovil odporúčané denné dávky pre esenciálne aminokyseliny v roku 2002. V prípade izoleucínu je to pre dospelých vo veku 19 rokov a starších 19 mg/kg telesnej hmotnosti/deň.[15]
Okrem svojej biologickej úlohy ako živiny sa ukázalo, že izoleucín sa podieľa aj na regulácii metabolizmu glukózy.[16]
Niektoré zdroje uvádzajú, že izoleucín znižuje únavu,[17] avšak podľa review z roku 2019 nemajú BCAA výrazný efekt na zníženie únavy.[18] Pomáhajú však so znížením hladiny laktátu (ktorý vzniká počas cvičenia a jeho hromadenie v svaloch sa prejavuje ako svalovica) a okrem toho pomáhajú regulovať hladiny amoniaku (ktorý spolu s laktátom spôsobuje únavu), glukózy, voľných mastných kyselín a kreatínkinázy.[18]
Izoleucín je jednou z dvoch proteinogénnych aminokyselín, ktoré majú dve chirálne centrá. Druhou je treonín. Prítomnosť dvoch chirálnych centier v tomto prípade vedie k celkom štyrom rôznym izomérom podľa Le Belovho-van ’t Hoffov vzťahu. V živých systémoch je prítomný len L-izoleucín.
Izoleucín je konštitučný izomér leucínu.
Z izoméru L-aloizoleucínu sa syntetizuje kyselina koronamová, ktorá je súčasťou fytotoxínu koronatínu, ktorý produkuje baktéria Pseudomonas syringae.[19] Ako aloizoleucín vzniká nie je známe.
| Izoméry izoleucínu | |||||||
|---|---|---|---|---|---|---|---|
| Triviálny názov | izoleucín | d-izoleucín | l-izoleucín | dl-izoleucín | d-aloizoleucín | l-aloizoleucín | dl-aloizoleucín |
| Synonymum | (R)-izoleucín | L-(+)-izoleucín | (R*,R*)-izoleucín | aloizoleucín | |||
| CAS číslo | 443-79-8 | 319-78-8 | 73-32-5 | 1509-35-9 | 1509-34-8 | 3107-04-8 | |
  |
| L-izoleucín (2S,3S) a D-izoleucín (2R,3R) |
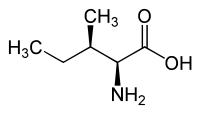  |
| L-aloizoleucín (2S,3R) a D-aloizoleucín (2R,3S) |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.