Amoniak
chemická zlúčenina From Wikipedia, the free encyclopedia
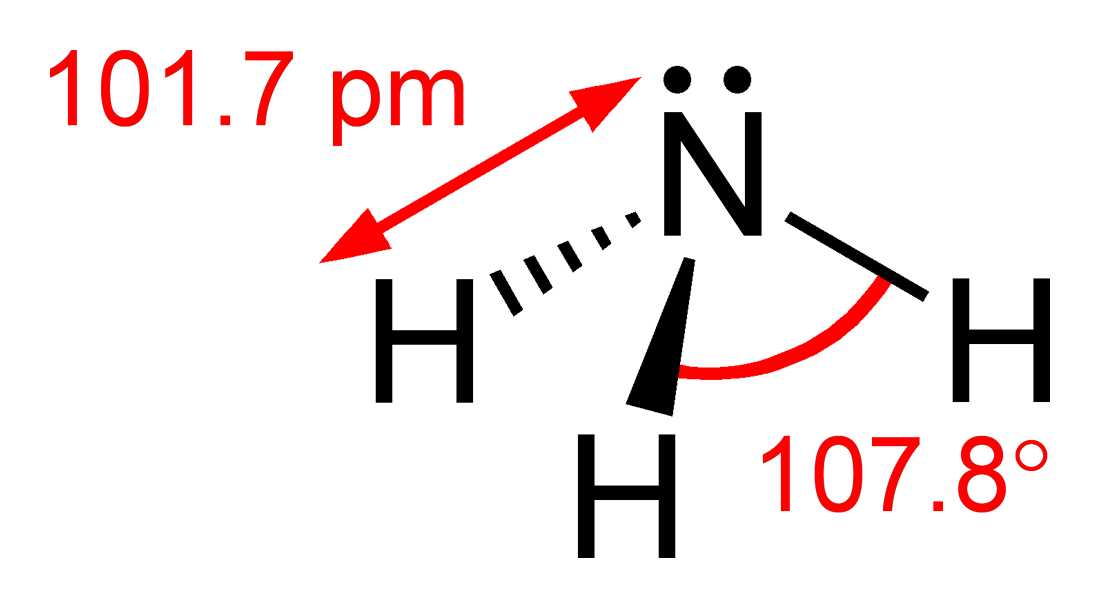
Amoniak je binárna zlúčenina dusíka a vodíka so vzorcom NH3.[1] V organickej chémii sa pre amoniak zaviedol systémový názov azán (a podobne pre jeho derivát hydrazín H2N-NH2 názov diazán).[2] Pri bežnom tlaku a teplote je to toxický, žieravý, bezfarebný plyn s charakteristickým prenikavým, ostrým, silne dráždivým zápachom.[3]
| Amoniak | |||||||||||||||||||
 | |||||||||||||||||||
 | |||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||
| Sumárny vzorec | NH3 | ||||||||||||||||||
| Systematický názov | Azán | ||||||||||||||||||
| Vzhľad | bezfarebný plyn | ||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||
| Molekulová hmotnosť | 17,031 g/mol | ||||||||||||||||||
| Teplota topenia | −77,73 °C | ||||||||||||||||||
| Teplota varu | −33,34 °C | ||||||||||||||||||
| Kritická teplota | 132,4 °C | ||||||||||||||||||
| Kritický tlak | 11,280 kPa | ||||||||||||||||||
| Hustota | 0,86 kg/m3 | ||||||||||||||||||
| pKB | 4,75 | ||||||||||||||||||
| |||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||
| Číslo CAS | 7664-41-7 | ||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||
Kvapalný amoniak podlieha autoprotolýze, podobne ako voda:[3]
2 NH3 ⇌ NH4+ + NH2-
V procese vzniká amónny katión a amidový anión. Hodnota rovnovážnej konštanty tejto reakcie je pKam = 34,00 pri -33 °C.[3]
Vodný roztok
Molekula amoniaku je výrazne polárna a rozpúšťa sa vo vode, kde z disociovanej molekuly vody preberá hydrón za vzniku amónneho katiónu:[1]
- NH3 + H2O → NH4+ + OH−
Výsledný roztok je slabo zásaditý a nazýva sa tiež čpavok alebo hydroxid amónny.[1] Toto označenie je však len triviálne a nemá svoje opodstatnenie, lebo molekula "NH4OH" neexistuje (dusík totiž nie je schopný vytvoriť päť väzieb).[4] Neexistencia molekuly "NH4OH" je v súlade s faktom, že amoniak je Brønstedova a nie Arrheniova zásada. Zásaditý charakter amoniaku je totiž podmienený jeho schopnosťou viazať protón, teda katión vodíka, H+, a nie tvorbou hydroxidových iónov OH− v priebehu reakcie NH3 + H2O → NH4+ + OH− (podľa tejto reakcie reagujú len 4 z 1000 molekúl amoniaku, pKb amoniaku je 4,75[3]). Správne označenie vodného roztoku amoniaku je teda NH3 (aq).
Výroba
Až do začiatku 1. svetovej vojny sa amoniak vyrábal destiláciou rastlinného a živočíšneho materiálu, redukciou kyseliny dusitej a dusitanov vodíkom, alebo rozkladom amónnych solí hydroxidmi či priamo nehaseným vápnom (oxid vápenatý). [chýba zdroj] Ako amónna soľ sa najčastejšie používal salmiak:[1]
- 2 NH4Cl + 2 CaO → CaCl2 + Ca(OH)2 + 2 NH3
Začiatkom 1. svetovej vojny nemeckí chemici Fritz Haber a Carl Bosch navrhli postup, dnes zvaný Haber-Boschov proces, na priamu syntézu amoniaku z plynného dusíka a vodíka:[1][3][5][6]
- N2 + 3 H2 → 2 NH3
Reakcia prebieha pri vysokej teplote (450 °C) a vysokom tlaku (100 atm).[3] Prebieha za prítomnosti železa ako katalyzátora,[1] ako promótor (látka aktivujúca katalyzátor) sa používa oxid hlinitý, pričom celá sústava sa zahrieva (napriek tomu, že reakcia je exotermická; je to z čisto ekonomických dôvodov).
Použitie
Amoniak sa používa pri výrobe priemyselných hnojív a na výrobu močoviny.[1] Takisto sa z neho vyrábajú plasty a výbušniny.[3]
V analytickej chémii sa využíva ako zrážadlo. Niekedy sa používa ako rozpúšťadlo pre rôzne chemické reakcie.[1] Veľmi dobre sa vňom rozpúšťajú alkalické kovy (rozpustnosť cézia v amoniaku je až 330 g Cs na 100 g NH3), ktoré tvoria vodívé farebné roztoky.[3]
Referencie
Iné projekty
Wikiwand - on
Seamless Wikipedia browsing. On steroids.