chemická zlúčenina From Wikipedia, the free encyclopedia
Hem A je druh hemu, čo je koordinačný komplex pozostávajúci z makrocyklického ligandu, patriaceho medzi porfyrín, ktorý cheluje atóm železa. Hem A je biomolekula, ktorá je prirodzene produkovaná mnohými organizmami. V roztoku má dichroicku zeleno-červenú farbu. Štruktúrne je podobný hemu B, ktorý je súčasťou hemoglobínu, červeného farbiva v krvi.
| Hem A | |
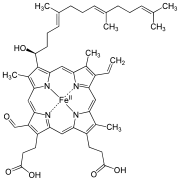 | |
 | |
| Všeobecné vlastnosti | |
| Sumárny vzorec | C49H56O6N4Fe |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 852,837 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 18535-39-2 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Hem A sa líši od hemu B v tom, že metylová skupina na uhlíku 8 v kruhu je oxidovaná na formylovú skupinu a na vinylovú skupinu na uhlíku 2 je naviazaná hydroxyfarnezylová skupina, ktorá patrí medzi izoprenoidy. Hem A sa podobá na hem O, keďže obe majú farnezylovú skupinu na uhlíku 2, ale hem O nemá formylovú skupinu na uhlíku 8, namiesto ktorej má metylovú skupinu. Správna štruktúra hemu A, určená pomocou meraní NMR a IR spektroskopií, zistená pre redukované podobnu komplexu (s FeII), bola prvýkrát publikovaná v roku 1975.[1] Štruktúra bola potom potvrdená syntézou dimetylesteru hemu A bez atómu železa.[2]
Hem A ako prvý izoloval nemecký biochemik Otto Warburg v roku 1951. Warburg takisto ukázal, že je to aktívna zložka integrálneho membránového metaloproteínu cytochróm c oxidázy.[3]
Poslednou otázkou v štruktúre hemu A bolo presné geometrické usporiadanie na prvom uhlíku na pozícii 3 v kruhu I, teda uhlíku viazanom na hydroxylovú skupinu. V roku 2005 bolo ukázané, že konfigurácia tohto chirálneho uhlíku je S.[4]
Podobne ako hem B, aj hem A je často naviazaný na apoproteín pomocou koordinačnej väzby medzi atómom železa a bočnými reťazcami zachovaných aminokyselín. V enzýme respiračného reťazca, cytochróm c oxidáze (CCO), je piatym ligandom hemu A, ktorý tvorí reakčné miesto pre kyslík, histidylová skupina.[5] Tento ligand (histidín) sa takisto bežne nachádza aj v iných hemoproteínoch, ako sú hemoglobín a myoglobín.

Príkladom metaloproteínu, ktorý viaže hem A, je cytochróm c oxidáza (CCO). Táto zložitá bielkovina obsahuje hem A na dvoch rôznych miestach, každý s inou finkciou. Jednotlivé miesta sú označované ako cytochróm a a cytochróm a3. Atóm železa v heme A v cytochróme a je hexakoordinovaný, teda viazaný na 6 ďalších atómov. V molekule cytochrómu a3 ja niekedy viazaný na 5 iných atómov (pentakoordinácia), čo necháva voľné šieste väzbové miesto, kam sa môže viazať molekula kyslíku (O2).[6] Okrem toho tento enzým viaže tri ióny mede, horčík, zinok a niekoľko iónov sodíka a draslíka. Predpokladá sa, že tieto dve hemové skupiny si vymieňajú elektróny medzi sebou, iónmi mede a proteínom cytochrómom c poblíž.
Predpokladá sa, že formylová skupina a izoprenoidový bočný reťazec majú v CCO dôležitú úlohu v zachovávaní energie pri redukcii kyslíka. CCO je podľa všetkého zodpovedaná za zachovávanie energie redukcie dikyslíku tým, že pumpuje protóny do intermembránového priestoru mitochondrie. Tento predpoklad bol publikovaný skupinou S. Yoshikawovej.[7]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.