Hidrazin
From Wikipedia, the free encyclopedia
From Wikipedia, the free encyclopedia
Hidrazin (diazan) neorgansko jedinjenje je sa formulom N2H4. On je bezbojna zapaljiva tečnost sa mirisom sličnom amonijaku. Hidrazin je veoma toksičan i veoma je nestabilan, osim ako se njime rukuje u rastvoru. Godine 2002. je proizvedeno oko 260.000 tona.[12] Hidrazin se uglavnom koristi kao agens za formiranje pene u pripremi polimernih pena, a nalazi i znatnu primenu kao prekurzor za polimerizacione katalizatore i lekove. Osim toga, hidrazin se koristi u raznim raketnim gorivima i za pripremu gasnih prekurzora koji se koriste u vazdušnim jastucima. Hidrazin se koristi u nuklearnim i konvencionalnim elkctričnim centralama u sistemima vodene pare kao sakupljač kiseonika, kojim se kontrolišu koncentracije rastvorenog kiseonika radi redukovanja korozije.
| Hidrazin | |
|---|---|
 |
 |
 |
 |
 | |
| Naziv po klasifikaciji | Hidrazin[1] |
| Drugi nazivi | Diamin[2] Diazan[1] |
| Identifikacija | |
| CAS registarski broj | 302-01-2 |
| PubChem[3][4] | 9321 |
| ChemSpider[5] | 8960 |
| UNII | 27RFH0GB4R |
| EINECS broj | |
| UN broj | 2029 |
| KEGG[6] | |
| MeSH | |
| ChEBI | 15571 |
| ChEMBL[7] | CHEMBL1237174 |
| RTECS registarski broj toksičnosti | MU7175000 |
| Bajlštajn | 878137 |
| Gmelin Referenca | 190 |
| 3DMet | B00770 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | N2H4 |
| Molarna masa | 32,0452 g mol−1 |
| Agregatno stanje | Bezbojna tečnost |
| Gustina | 1,021 g cm−3 |
| Tačka topljenja |
2 °C, 275 K, 35 °F |
| Tačka ključanja |
114 °C, 387 K, 237 °F |
| log P | 0,67 |
| Napon pare | 1 kP (na 30,7 °C) |
| pKa | 8,10[8] |
| Baznost (pKb) | 5,90 |
| Indeks prelamanja (nD) | 1,46044 (na 22 °C) |
| Viskoznost | 0,876 cP |
| Struktura | |
| Oblik molekula (orbitale i hibridizacija) | Trougano piramidalni na N |
| Dipolni moment | 1,85 D[9] |
| Termohemija | |
| Standardna entalpija stvaranja jedinjenja ΔfH |
50,63 kJ mol−1 |
| Standardna molarna entropija S |
121,52 J K−1 mol−1 |
| Opasnost | |
| Podaci o bezbednosti prilikom rukovanja (MSDS) | ICSC 0281 |
| EU-klasifikacija | |
| EU-indeks | 007-008-00-3 |
| NFPA 704 | |
| R-oznake | R45, R10, R23/24/25, R34, R43, R50/53 |
| S-oznake | S53, S45, S60, S61 |
| Tačka paljenja | 52 °C |
| Tačka spontanog paljenja | 24–270 °C |
| Eksplozivni limiti | 1.8–99.99% |
| LD50 | 59–60 mg/kg (oralno u pacovima, miševima)[11] |
| Srodna jedinjenja | |
| Srodna jedinjenja | Amonijak |
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |
| Infobox references | |
Hidrazin formira monohidrat koji ima veću gustinu (1,032 g/cm3) od anhidratnog materijala.
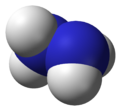
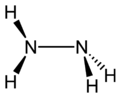
Hidrazin se može formirati iz dva molekula amonijaka uklanjanjem jednog vodonika po molekulu. Svaka H2N-N podjedinica je piramidalnog oblika. N-N rastojanje je 1,45 Å (145 pm), i molekul poprima gauche konformaciju.[13] Rotaciona barijera dva puta veća od etana. Ova strukturna svojstva su slična gasovitom vodonik peroksidu, koji poprima zakrivljenu antiklinalnu konformaciju, i takođe ima jaku rotacionu barijeru.
Hidrazin ima bazna (alkalna) hemijska svojstva, slična amonijaku:
sa vrednostima:[14]
(za amonijak Kb = 1,78 x 10−5)
Hidrazin se teško deprotonuje:[15]
Toplota sagorevanja hidrazina u kiseoniku (vazduhu) je 194,1 x 105 J/kg (9345 BTU/lb).[16]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.