Химерный рецептор антигена
Из Википедии, свободной энциклопедии
Химерный рецептор антигена (англ. Chimeric antigen receptor, CAR) — это рекомбинантный гибридный белок, сочетающий фрагмент антитела, обладающий способностью очень избирательно связываться с конкретными антигенами, с сигнализирующими доменами, способными активировать Т-клетки[1]. Поскольку такой гибридный белок состоит из частей, полученных из разных источников, его называют химерным[2]. Иммунные эффекторные клетки, имеющие сконструированные таким образом CAR, приобретают высокую селективность за счёт добавленного извне рецептора от моноклонального антитела.
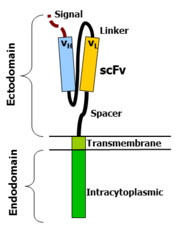
Технология CAR позволяет перепрограммировать собственные иммунные клетки пациента за пределами его тела, с тем чтобы создать CAR, позволяющий охотиться на раковые клетки и эффективно разрушать опухоли у пациента.[3][4] Полученные клетки CAR затем используют для так называемой адоптивной иммунотерапии[англ.] — разновидности иммунотерапии рака[5][6][7][8][9]. Обычно CAR состоят из внеклеточного антигенраспознающего фрагмента, который связан, с помощью спейсера-шарнира и трансмембранного домена, со внутриклеточным доменом сигнализации, который может состоять из костимулирующего домена[10][11] и участка Т-клеточной активации.
CARs опознают антигены не только по основным антигенам гистосовместимости, что и отличает их от физиологических Т-клеточных рецепторов (ТКР). Поэтому CAR-Т-клетки могут преодолеть некоторые из основных механизмов, посредством которых опухолям удаётся избежать опознания их Т-клеткой по антигенам гистосовместимости[12]
Ещё одной особенностью CARs является их способность связывать не только белки, но и углеводы[13], ганглиозиды[14][1], протеогликаны[15], а также гликозилированные белки[16], тем самым расширяя спектр потенциальных целей.


В дополнение к антиген-специфическому связыванию, разработаны так называемые «универсальные системы CAR». Так например, разработаны CAR, связывающие авидин[18], что позволило использовать единожды полученный CAR не против одного антигена, ассоциированного с опухолью, а против бесчисленного множества различных антигенов, распознаваемых с помощью различных антител, модифицированных биотином[18], что позволяет выявлять их авидином (реакция авидин-биотин[англ.]). Аналогичным образом устроена универсальная система CAR, связывающая флуоресцеинизотиоцианат[англ.] (FITC)[19][20] Универсальная система CAR названная «Supra CAR» состоит из двух модулей: универсального рецептора (zipCAR) и адаптерного модуля scFv распознающего антиген опухоли (zipFv). Универсальный рецептор zipCAR образуется в результате слияния внутриклеточных сигнальных доменов и лейциновой «застёжки-молнии» (zipper) в качестве внеклеточного домена. Молекула адаптера zipFv состоит из домена узнающего и соединяющегося с лейциновой «застёжкой-молнией» и домена scFv. ScFv молекулы zipFv связывается с опухолевым антигеном, а лейциновая молния связывает и активирует zipCAR на иммунных клетках. Модуль универсального рецептора zipCAR может быть расположен на различных типах клеток: на T-лимфоцитах с CD4+ и CD8+ корецепторами Т-клеточных рецепторов; на регуляторных Т-клетках, а также на NK-клетках. Множество различных zipFv молекул позволяет легко и быстро перенастраивать систему на новые антигены без необходимости заново конструировать CAR-Т-клетки.[21]
При терапии с помощью CAR-Т-клеток возможны осложнения в виде синдрома высвобождения цитокинов, в частности повышение уровня интерлейкина 6 и интерлейкина 2[22]. Система SUPRA CAR даёт возможность быстро остановить развитие синдрома высвобождения цитокинов так как позволяет добавить при необходимости конкурентные zipFv, что защитит zipCAR от активации[21]
Использование CAR-модифицированных клеток для терапии рака
Суммиров вкратце
Перспектива

В течение многих десятилетий большинство видов рака лечили по стандартному набору терапевтических подходов, в числе которых были хирургия, радиационная терапия и химиотерапия. Теперь этот список дополнила иммунотерапия — тип лечения, который для борьбы с заболеванием использует иммунную систему пациента. Повышению значимости иммунотерапии для лечения рака способствовала разработка CAR-модифицированных T-клеток, нацеленных на раковые антигены. Так например, были разработаны CAR, направленные против подопланина (PDPN), белка, который, как правило, в изобилии содержится в солидных опухолях, в том числе в клетках глиобластомы[24] наряду с, вызванной делецией, мутантной формой рецептора эпидермального фактора роста (EGFR) — белком EGFRvIII[25][26], а также против эпитопа Tn муцина MUC1 опухолевого антигена, обнаруженного при различных карциномах[27], что позволило (пока в опытах на мышах) успешно лечить эти заболевания.
В случае, когда здоровые ткани имеют те же целевые антигены, что и опухолевые клетки, терапия с помощью CAR, направленная на подобный антиген, может вызвать значительный токсический эффект. Кроме того, CD4+-Treg-клетки подавляют эффективность клеточной терапии CAR-Т. Поэтому нужно тщательно подбирать клоны CAR-Т[28].
CAR-Т-клеточные продукты, полученные из хорошо подобранных клонов Т-клеток, имеют значительно более высокую эффективность по сравнению с продуктами, полученными из неотобранных Т-клеток, которые различаются по фенотипическому составу. Поэтому селекция и отбраковка имеют важное значение для разработки CAR-Т, где синергично сочетается противоопухолевое действие самых мощных фенотипов CD4+- и CD8+-клонов[29]..
Снизить токсический эффект CAR на здоровые ткани можно также с помощью CAR, сконструированных так, что синтетический рецептор Notch для одного антигена индуцирует экспрессию CAR для второго антигена. Такие Т клетки с двухрецепторным «замком-затвором» способны активироваться только в отношении опухолевых клеток, имеющих оба антигена, что повышает их избирательность в отношении именно опухолевых клеток[30].
С середины 2010-х годов Т-клетки CAR были применены для лечения более тысячи пациентов с поздними стадиями лейкозов и лимфом. Большинство из них до сих пор живы, а сотни полностью излечились[31].
Терапия твердых (солидных) опухолей
В солидной опухоли часто формируется отклоняющаяся от нормы сосудистая сеть, которая может препятствовать инфильтрации Т-клеток и формировать иммуносупрессивное микроокружение опухоли. В частности усиленное отложение компонентов внеклеточного матрикса может служить физическим барьером для проникновения CAR-T-клеток и прямого их контакта с раковыми клетками. Кроме того необходимо преодолевать иммуносупрессивное микроокружение, которое выделяя различные цитокины ингибирует функцию CAR-T-клеток[3].
Поскольку характерной особенностью примерно 50 % твёрдых опухолей является гипоксическая среда, были спроектированы Т-клетки CAR, которые реагируют на гипоксическую среду — они неэффективны, если не находятся в гипоксической среде. С этой целью к ним добавлен субдомен HIF1α (hypoxia-inducible factor 1-alpha). Введение «датчика опухолевого микроокружения» обеспечивает дополнительный уровень безопасности за счёт сведения к минимуму внецелевого действия Т-клетки CAR[32]. Другой способ сведения к минимуму внецелевого действия Т-клетки CAR, (называемый CytomX Probody-технология), заключается в «маскировании» (блокировке) распознающего мишень участка антитела до тех пор пока Т-клетка CAR не попадёт в опухоль, где её маскировка будет удалена протеазой, уникальной для микроокружения опухоли[33].
Эффективность Т-клеточной иммунотерапии CAR против солидных опухолей зависит от накопления, пролиферации и продолжительности наличия Т-клеток в месте опухоли. Чтобы эффективно использовать Т-клетки, экспрессирующие CAR, в иммунотерапии солидных опухолей, крайне важно, чтобы внутривенно вводимые CAR-T-клетки накапливались и размножались в месте опухоли, а главное чтобы они непрерывно работали на протяжении достаточно долгого времени, находя и устраняя вредные раковые клетки. Чтобы противостоять дисфункции Т-клеток в микроокружении опухоли, CAR Т-клетки, были изменены так, чтобы они секретировали интерлейкин 10 (IL-10), что способствовало пролиферации и повышению эффективности функционирования CAR T-клеток, благодаря чему удалось достигнуть полной регрессии солидных опухолей и метастазов рака у мышей, включая рак толстой кишки, рак молочной железы, меланому и рак поджелудочной железы.[34] Т-клетки IL-10 CAR также индуцировали в лимфоидных тканях надежную защиту от повторного заражения опухолью.[34] В опытах на мышиной модели солидной опухоли, была разработана технология селекции клонов ИПСК несущих клетки обеспечивающие наиболее эффективную иммунотерапию после их дифференцировки в CAR-T-клетки. При этом клетки, с целью усилить их пролиферацию и персистенцию в опухолях, подвергали ещё двум дополнительным генетическим манипуляциям:
- генетическому нокауту киназы называемой диацилглицеролкиназой, которая ингибирует передачу сигналов антиген-рецептор;
- трансдукции клеток генами, кодирующими мембраносвязанный интерлейкин 15 (IL-15) и его рецепторную субъединицу IL-15Rα.[35]
Драйдукс (Drydux) технология
Разработан макропористый биоматериал для быстрой и эффективной генерации CAR Т-клеток in situ, непосредственно в теле пациента, позволивший сделать технологию более доступной, упростить, удешевить её и при этом сократить подготовку CAR-Т-клеток до трёх дней после сбора крови пациента, вместо обычных двух недель[36]. После того как каркас из Драйдукса имплантируют пациенту, он, в отличие от традиционной CAR-Т-клеточной терапии, которая обеспечивала лишь временный контроль над опухолью, обеспечивает пролонгированное высвобождение CAR-Т-клеток, их функциональность и повышенную устойчивость, на протяжении примерно пяти месяцев. Благодаря этому достигается длительная ремиссия опухоли[36].
Использование CAR-модифицированных клеток для предотвращения аутоиммунных реакций
Суммиров вкратце
Перспектива
Предотвращение реакции отторжения трансплантата
Использование терапии химерными анти-CD40-антителами, предотвращая активацию гуморальных механизмов отторжения и дисрегуляцию путей регуляции свёртывания крови, позволило ксенотрансплантату сердца свиньи проработать в теле у примата (бабуина) 945 дней. Подобные подходы в конечном счёте могут быть использованы и для трансплантации органов в организм человека, что очень актуально, учитывая острую нехватку пригодных для трансплантации органов[37].
Регуляторные Т-клетки (Tregs) играют существенную роль в предотвращении аутоиммунитета, и в частности в профилактике реакции отторжения трансплантата, препятствующей успешной трансплантации органов[38][39].
Применение регуляторных Т-клеток в клинической практике было ограничено крайне низким количеством этих клеток в периферийной крови и поликлональности — отсутствия у их популяции узкой направленности (из-за чего можно было вызвать нежелательное общее понижение иммунитета человека). Был разработан метод трансдукции регуляторных Т-клеток человека с помощью CAR, который нацелен на молекулу А2 человеческого лейкоцитарного антигена класса I. Использование химерных антигенных рецепторов HLA-A2-CAR, в которых регуляторные Т-клетки, генетически сконструированы для экспрессии внеклеточных одноцепочечных Ab (ScFv — Single-chain variable fragment) антиген-связывающих доменов, поможет защитить пересаженные ткани и органы от отторжения иммунной системой пациента[40][41][42].
Терапия аутоиммунных заболеваний
Разработана стратегия лечения аутоиммунных заболеваний с помощью химерного рецептора аутоантител CAAR (англ. chimeric autoantibody receptor), который нацеливает T-клетки на уничтожение аутореактивных В-клеток. Так, например, спроектированы человеческие Т-клетки, синтезирующие CAAR, состоящий из аутоантигена (в данном случае десмоглеина Dsg3), слитого с сигнальным доменом CD137-CD3ζ, который активирует T-клетки. Такие Dsg3-CAAR-T-клетки проявляют избирательную цитотоксичность против В-клеток, экспрессирующих анти-Dsg3 и поэтому способны избирательно устранить Dsg3-специфические В-клетки in vivo, не затрагивая при этом другие В-клетки[43] .
Технология ускоренного выращивания CAR
Внедрение последовательности Strep-tag II (пептидной последовательности из восьми остатков (Trp-Ser-His-Pro-Gln-Phe-Glu-Lys), которая проявляет сродство к стрептавидину[44]) в определённом участке CAR позволило использовать эту последовательность в качестве маркера для идентификации и быстрого выделения. С помощью специального антитела, которое связывается с Strep-tag, сконструированные клетки можно быстро размножить в 200 раз. При этом 95 % клеток содержат CAR (тогда как обычно число таких клеток не превышало 43 %)[45]
CAR T-клетки, сверхэкспрессирующие FOXO1
Обнаружено, что активность гена FOXO1 коррелировала с положительными клиническими результатами пациентов, получавших CAR T-клетки для иммунотерапии рака. CAR T-клетки, у которых искусственно вызвана сверхэкспрессия FOXO1, дольше сохраняли свои функции и лучше противостояли опухоли in vivo.[46][47]
CAR T-клетки секретирующие IL-18
Провоспалительный цитокин интерлейкин 18 (IL-18) обладает способностью увеличивать активность клеток ЕК в селезёнке, индуцировать экспрессию интерферона-γ (IFN-γ), а также активировать лимфоциты и моноциты, не вызывая при этом сильную дозозависимую токсичность[48]. Поэтому были созданы IL-18-секретирующие T клетки с химерным рецептором антигена (IL-18-CAR T), что позволило значительно увеличить пролиферацию CAR T клеток и противоопухолевую активность организма[49][50].
Универсальные CAR T-клетки, устойчивые к ингибированию PD1
Суммиров вкратце
Перспектива
С помощью тройного редактирования генома удалось создать CAR-T-клетки, у которых снижена «аллореактивность» — они не вызывают болезни «трансплантат против хозяина» и имеют повышенную противоопухолевую активность, так как устойчивы к ингибированию воздействием опухоли на PD1 (programmed cell death protein 1)[51][52][53]. Как известно, опухоли, воздействуя на ген PD1, способны предотвращать атаку на них иммунных клеток, поэтому, если иммунным клеткам не хватает PD1, то раковые клетки не могут ими манипулировать. Есть, однако, риск того, что такие иммунные клетки «без тормозов» могут начать атаковать и здоровые клетки. Эта разработка будет способствовать широкому внедрению в клинику технологии CAR, поскольку если до сих пор CAR-T-клетки создавали для каждого пациента персонально, что было очень дорого, сложно и требовало много времени, то со внедрением новой технологии процесс подбора CAR-T-клеток станет значительно проще.
Разработана также технология, использующая полимерные наночастицы для переноса в ядра Т-клеток ДНК с генами, нацеливающими CAR. Эти полимерные наночастицы просты в изготовлении и достаточно стабильны, что упрощает их хранение и снижает их стоимость[54][55]. Имея заранее заготовленную «библиотеку» таких наночастиц, можно быстро перепрограммировать специализацию CAR. Более того, авторы утверждают, что их технология позволяет проводить перепрограммирование in situ, просто вводя наночастицы, нацеленные на Т-клетки в кровотоке[55].
CAR-T-NKR-2-клетки
Суммиров вкратце
Перспектива
Фирма Celyad CAR-T создала принципиально новые CAR-T-NKR-2-клетки. В отличие от метода scFv-антител, используемого «классическим» CAR-T, Celyad CAR-T использует, как первичный рецептор в Т-клетках, для распознавания опухолевого антигена рецептор, состоящий из продукта полноразмерного нативного человеческого NKG2D-гена, слитого с цитоплазматическим сигнальным доменом нативного человеческого CD3ζ.
NKG2D является нормальным человеческим белком, который играет важную роль в защите человеческого организма от инфекций и рака. Лиганды к рецепторному белку NKG2D в норме не синтезируются. Они появляются на поверхности клетки лишь в случае стрессовых ситуаций, таких как вирусная инфекция, окислительный стресс, генотоксические препараты, повреждение тканей, тепловой шок, действие воспалительных цитокинов и главным образом при злокачественной трансформации. Этот рецептор распознаёт порядка 80 % всех раковых клеток (как солидные опухоли, так и различные виды рака крови), что значительно расширяет диапазон его использования. Клинические испытания в фазе 1а показали что препарат безопасен для человека[56][57]
«Готовый» ресурс для лечения рака представляют собой, полученные из ИПСК человека оптимизированные NK-клетки с трансмембранным доменом NKG2D (NK-CAR-iPSC-NK cells). Отмечается что они менее токсичны чем обычные CAR-T и при этом дольше живут в организме[58]
Разработана эффективная, безопасная и экономически выгодная технология получения высокофункциональных CAR NK-клеток с помощью невирусной инженерии использующей систему транспозона/транспозазы Спящей Красавицы (SB) и минимизированные репликоны-векторы ДНК, называемые мини-кольцами[59][60].
CAR-макрофаги
Известно что макрофаги могут поглощать и убивать клетки в процессе фагоцитоза. Новым подходом к терапии солидных (лат. solidus — твёрдый) опухолей, которые плохо поддавались терапии CAR-T-клетками, является попытка использовать макрофаги, генетически модифицированные добавлением химерного рецептора антигена, чтобы специально направлять их к опухолевым клеткам. Предполагается, что CARMA (Chimeric antigen receptor macrophages — CAR-макрофаги) помогут лечить метастатические солидные опухоли.[61]
Неиммунные клетки, перепрограммированные в аналоги Т-клеток
Суммиров вкратце
Перспектива
С целью упрощения и удешевления технологии получения Т-клеток, исследователи создали синтетические клетки, имитирующие Т-клетки. Для этого они перепрограммировали клетки человеческих почек (которые можно извлечь из мочи) и стволовые клетки, получаемые липосакцией[62][63][64]. Эти синтетические клетки оснащены сигнальным механизмом, который состоит из молекулярных антенн и антител которые могут распознавать целевые структуры раковой клетки, а также имеют генетический механизм, который генерирует ферментный комплекс, разрушающий мембрану клетки-мишени, и фермент который преобразует противораковое вещество проникшее во внутреннюю часть опухолевой клетки из неактивного предшественника (препарата, который должен быть добавлен в организм извне) в активное состояние. В результате раковые клетки разрываются, активное вещество высвобождается и разрушает другие опухолевые клетки в «зоне смерти» вокруг синтетической Т-клетки.
Появилась технология позволяющая производить CAR Т клетки в промышленных масштабах из генетически модифицированных индуцированных плюрипотентных стволовых клеток (ИПСК). Готовые линии таких клеток можно бесконечно долго размножать в качестве не дорогого лекарственного препарата. Перед употреблением такие модифицированные ИПСК клетки превращают в зрелые CAR Т клетки с помощью искусственного органоида тимуса, который работает, имитируя среду тимуса, органа, в котором Т-клетки развиваются из стволовых клеток крови[65][66].
Иммунотерапия аутоиммунных заболеваний CAR-МСК
С целью повышения терапевтической эффективности мезенхимальных стромальных клеток (МСК), путем усиления их способности к антиген-специфической иммуносупрессии, был предложен метод объединения химерных антигенных рецепторов с МСК, для получения модифицированных стволовых клеток, известных как CAR-МСК.[67]. При антигенспецифической стимуляции CAR-МСК активируют у себя экспрессию иммуносупрессивных генов и рецепторов для ингибирования Т-клеток, а также выработку иммуносупрессивных цитокинов, сохраняя при этом фенотип стволовых клеток.[67]
См. также
Примечания
Литература
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
