Tlenek baru
związek chemiczny Z Wikipedii, wolnej encyklopedii
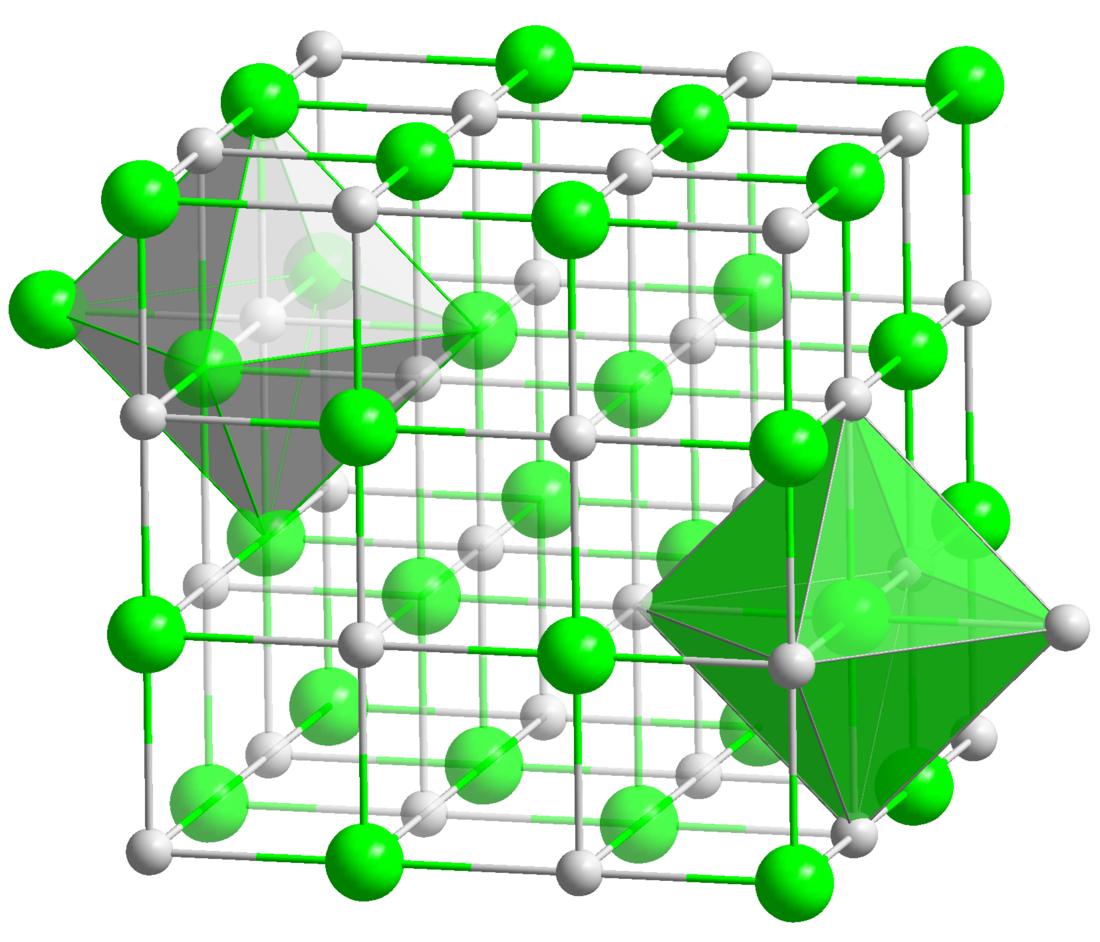
Tlenek baru, BaO – nieorganiczny związek chemiczny z grupy tlenków zasadowych zawierający bar na II stopniu utlenienia.
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ogólne informacje | |||||||||||||||||||||||||
| Wzór sumaryczny |
BaO | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Masa molowa |
153,33 g/mol | ||||||||||||||||||||||||
| Wygląd | |||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||
| Numer CAS | |||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Podobne związki | |||||||||||||||||||||||||
| Inne aniony | |||||||||||||||||||||||||
| Inne kationy | |||||||||||||||||||||||||
| Jeżeli nie podano inaczej, dane dotyczą stanu standardowego (25 °C, 1000 hPa) | |||||||||||||||||||||||||
Otrzymywanie
Jest otrzymywany w wyniku ogrzewania węglanu baru z węglem[1][5]:
- BaCO
3 + C → BaO + 2CO
Obecność węgla pozwala znacząco obniżyć temperaturę rozkładu BaCO
3[5].
Inną metodą jest termiczny rozkład azotanu baru[1].
Właściwości
Tlenek baru jest białym ciałem stałym. Występuje w postaci regularnych kryształów lub żółtawego proszku[1]. Ma właściwości higroskopijne[potrzebny przypis].
Jest tlenkiem alkaicznym i reaguje z wodą dając zasadowy wodorotlenek baru[1][6]:
- BaO + H
2O → Ba(OH)
2
Zastosowanie
Jest wykorzystywany do produkcji metalicznego baru metodą aluminotermiczną, zarówno w warunkach laboratoryjnych, jak i na skalę przemysłową[7][5]:
- 3BaO + 14Al → 3BaAl
4 + Al
2O
3 - 8BaO + BaAl
4 → 7Ba↑ + 2BaO·Al
2O
3 - BaO + Al
2O
3 → BaO·Al
2O
3- sumarycznie:
- 4BaO + 2Al → 3Ba↑ + BaO·Al
2O
3
Powstający bar w temperaturze procesu wynoszącej 1100–1200 °C wydziela się w formie gazowej i ulega kondensacji w chłodnej części reaktora[7][5].
Ponadto jest substratem do produkcji wodorotlenku baru[6]. Można z niego także otrzymać nadtlenek baru: tlenek ogrzewa się do 500 °C w obecności powietrza lub tlenu[1][8]:
- 2BaO + O
2 → 2BaO
2
Przypisy
Bibliografia
Wikiwand - on
Seamless Wikipedia browsing. On steroids.