
Antimoon(III)jodide
chemische verbinding / Uit Wikipedia, de vrije encyclopedia
Antimoon(III)jodide is een anorganische verbinding met de formule 


Snelle feiten Structuurformule en molecuulmodel, Algemeen ...
| Antimoon(III)jodide | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
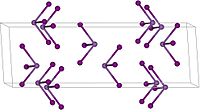 | ||||
Kristalrooster van  | ||||
 | ||||
Molecuulmodel van  | ||||
| Algemeen | ||||
| Molecuulformule |  | |||
| IUPAC-naam | Antimoon(III)jodide | |||
| Andere namen | Antimoontrijodide, Trijoodstibaan | |||
| Molmassa | 502,473 g/mol | |||
| SMILES | [SbH3+3].[I-].[I-].[I-] | |||
| CAS-nummer | 7790-44-5 | |||
| EG-nummer | 232-205-8 | |||
| PubChem | 24630 | |||
| Wikidata | Q2505731 | |||
| Beschrijving | Rode kristallen | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302+H332 - H317 - H411 | |||
| P-zinnen | P273 - P280 - P301+P312+P330 - P302+P352 - P304+P340+P312 | |||
| EG-Index-nummer | 232-205-8 | |||
| Fysische eigenschappen | ||||
| Dichtheid | 4,921 g/cm³ | |||
| Smeltpunt | 170,5 °C | |||
| Kookpunt | 401,6 °C | |||
| Oplosbaarheid in water | Oplosbaar,hydrlyseert langzaam | |||
| Goed oplosbaar in | Benzeen, Alcohol, Aceton, Koolstofdisulfide, Zoutzuur, Kaliumjodide, tin(IV)chloride, Dimethylamine, HI, alkalimetaaltriiodides[2] | |||
| Slecht oplosbaar in | Chloroform, Tetrachloormethaan[2] | |||
| Geometrie en kristalstructuur | ||||
| Dipoolmoment | 1,58 D | |||
| Thermodynamische eigenschappen | ||||
| ΔfH |
-100.4 kJ/mol | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Sluiten




