
Bikarbonat
From Wikipedia, the free encyclopedia
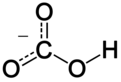
Dalam kimia tak organik, bikarbonat (nama saranan IUPAC: hidrogen karbonat[2]) ialah sebuah bentuk peralihan dalam penyahprotonan asid karbonik. Ini ialah anion poliatom dengan formula kimia HCO−
3. Bikarbonat berperanan penting dalam sistem penimbalan pH fisiologi dalam biokimia.[3]
Fakta Segera Nama, Pengecam ...
 | |
 | |
| Nama | |
|---|---|
| Nama IUPAC sistematik
Hidroksidodioksidokarbonat(1-) Hydroxidodioxidocarbonate(1−)[1] | |
| Nama lain
Hidrogenkarbonat[1] | |
| Pengecam | |
| |
Imej model 3D Jmol |
|
| 3DMet | |
| 3903504 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider |
|
| 49249 | |
| KEGG |
|
PubChem CID |
|
| UNII | |
CompTox Dashboard (EPA) |
|
| |
| |
| Sifat | |
| HCO− 3 | |
| Jisim molar | 61.0168 g mol−1 |
| log P | −0.82 |
| Keasidan (pKa) | 10.3 |
| Kebesan (pKb) | 7.7 |
| Asid konjugat | Asid karbonik |
| Bes konjugat | Karbonat |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| Rujukan kotak info | |
Tutup
Istilah "bikarbonat" (bicarbonate) diciptakan pada 1814 oleh ahli kimia Inggeris William Hyde Wollaston.[4] Awalan "bi" dalam "bikarbonat" berasal daripada sistem penamaan lapuk, iaitu berdasarkan pemerhatian bahawa terdapat dua kali lebih banyak karbonat (CO2−
3) bagi ion natrium dalam natrium bikarbonat (NaHCO3) dan bikarbonat lain berbanding natrium karbonat (Na2CO3) dan serta karbonat lain.[5] Kini, nama itu kekal sebagai nama trivia semata-mata.