
Сигма-врска
From Wikipedia, the free encyclopedia
Сигма-врска (σ-врска) — најсилниот вид дна ковалентна хемиска врска.[1] Се образува со челен преклоп на атомски орбитали. Сигма-сврзувањето најпросто се дефинира за двоатомски молекули со посредство на симетриски групи. Во овој формален приод, σ-врска е симетрична во однос на вртењето околу оска на врска. По таа дефиниција, чести облици на сигма-врски се s+s, pz+pz, s+pz и dz2+dz2 (каде z се дефинира како оската на врската или меѓујадрената врска).[2] Квантната теорија вели дека молекулските орбиали со истоветна симетрија всушност се мешаат или хибридизираат. Како практична последица од ова мешање на двоатомните молекули, брановите функции s+s и молекулските орбитали pz+pz се смешуваат. Степенот на ова смешување (или хибридизација) зависи од релативните енергии на молекулските орбитали со иста симетрија.


Кај еднојадрените двоатаомски молекули, сврзувачките σ-орбитали немат јазолни рамнини со нулта бранова функција, било низ сврзаните атоми или меѓу нив. Придружното антисврзување или σ*-орбитала се дефинира како присуство на една јазолна рамнина помеѓу двата сврзани атоми.
Сигма-врските се најсилниот вид на ковалентна врска поради непосредиот преклоп на орбиталите, па електроните во овие врски понекогаш се нарекуваат сигма-електрони.[3]
Симболот σ е грчката буква сигма. Кога се гледа долж оската на врската, σ-молекулската орбитала има кружна симетрија, и така наликува на атомската орбитала „s“ која има иста звучност.
Единечната врска типично е сигма-врска, а повеќекратната врска е составена од една сигма-врска заедно со пи- или други врски. Двојната врска има една сигма- и една пи-врска, а тројната врска има една сигма- и две пи-врски.
| —— | ———————————————— | ————— |
Атомски орбитали |  | |
| Симетрични (s–s и p–p) сигма-врски помеѓу атомските орбиали | Пи-врска, за споредба | |
| —— | ———————————————— | ————— |
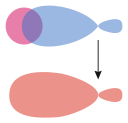 σs–хибрид | 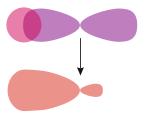 σs–p | |