トップQs
タイムライン
チャット
視点
HSPA8
ウィキペディアから
Remove ads
HSPA8(heat shock protein family A (Hsp70) member 8)またはHsc70(heat shock cognate 71 kDa protein)は、ヒトでは11番染色体に位置するHSPA8遺伝子にコードされる熱ショックタンパク質である[5]。Hsp70ファミリーのメンバー、そしてシャペロンタンパク質として、新たに翻訳されたタンパク質や誤ったフォールディングをしたタンパク質が正しくフォールディングするよう促進するとともに、変異タンパク質の安定化または分解も促進する[5][6]。このタンパク質の機能はシグナル伝達、アポトーシス、オートファジー、タンパク質恒常性、細胞成長や分化などの生物学的過程に寄与しており[6][7][8]、多くの種類のがん、神経変性疾患、細胞老化や加齢と関連している[6][7]。
Remove ads
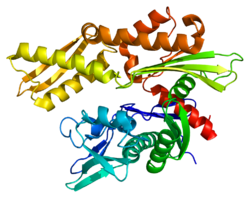
構造
HSPA8遺伝子は、Hsp70ファミリーの一員であるHSPA8タンパク質をコードする[5]。HSPA8はHsp70タンパク質の1つであるため、C末端に基質結合ドメイン、N末端にATP結合ドメインを有する[9][10][11]。基質結合ドメインは2層のβサンドイッチからなるサブドメイン(SBDβ)とαヘリカルサブドメイン(SBDα)の2つのサブドメインから構成され、両者はループLα,βによって連結されている。SBDβにはペプチド結合ポケットが含まれ、SBDαは基質が結合する溝を覆うふたとして機能する。ATP結合ドメインは4つのサブドメインから構成され、中心に位置するATP/ADP結合ポケットによって2つのローブへと分割される。2つのドメインはループLL,1と呼ばれる保存された領域によって連結されており、この領域はアロステリック調節に重要である。最もC末端の部分に存在する構造をとらない領域は、コシャペロンのドッキング部位となっていると考えられている[11]。
Remove ads
機能
要約
視点
Hsp70ファミリーには、熱誘導性のものと恒常的に発現しているものの双方が含まれている。後者はHsc(heat-shock cognate)タンパク質と呼ばれる。HSPA8はHsc70としても知られ、後者に属するタンパク質である。このタンパク質は新生ポリペプチドに結合して、正しいフォールディングを促進する[5]。また、非ネイティブ状態のタンパク質を正しくフォールディングさせるため、Hsp70シャペロンはATPに制御された形でタンパク質の疎水性ペプチドと相互作用する。正確な機構はいまだ不明であるものの、kinetic partitioningとlocal unfoldingと呼ばれる、少なくとも2つの代替的作用機構が存在する。Kinetic partitioning機構では、Hsp70は基質の結合と放出のサイクルを繰り返し、遊離している基質の濃度を低く維持する。この機構は凝集を効果的に防ぎ、遊離した基質のネイティブ状態へのフォールディングを可能にする。Local folding機構では、結合と放出のサイクルによって基質の局所的なフォールディングを誘導し、ネイティブ状態へのフォールディングのための速度論的障壁を越えるよう補助する。こうしたタンパク質フォールディング機能は、最終的にはシグナル伝達、アポトーシス、タンパク質恒常性、細胞成長、分化といった機能に寄与する[6][7]。
Hsc70は細胞質基質とリソソームに局在し、そこではシャペロン介在性オートファジーに関与している。Hsc70は基質タンパク質のアンフォールディングとリソソーム内腔への移行を補助し、リソソーム経路によって分解されるタンパク質の選択性を付与している[12][13][14]。Hsc70はこの経路を介してアポトーシスタンパク質BBC3/PUMAの正常条件下での分解に寄与し、細胞を保護している[13]。
さらに、Hsc70は細胞周期の移行や発がんの正の調節因子としても機能する。一例として、Hsc70はG1期からS期への移行の重要な因子であるサイクリンD1の核内蓄積を調節している[15][16]。
Hsc70は、膜要素の輸送におけるクラスリン被覆小胞の解体時のATPアーゼとしても機能する[5][14]。Hsc70はオーキシリンとともに機能し、被覆小胞からクラスリンを除去する。神経細胞においては、シナプトジャニンも小胞の被覆の除去に関与する重要なタンパク質である。
Hsc70と熱誘導性Hsp70との比較
ヒトのHsc70は、熱誘導性Hsp70と85%が同一である。両者は細胞内で類似した役割を果たしていると考えられてきたが、こうした予測は不正確なものであった。Hsc70は正常条件下でもシャペロン機能を果たしており、また恒常的に発現してタンパク質のユビキチン化や分解など正常な細胞過程と関連した機能を果たしている[14][17]。
Remove ads
臨床的意義
Hsp70ファミリーのタンパク質は、カスパーゼ依存性経路への作用、そしてTNF-α、スタウロスポリン、ドキソルビシンなどアポトーシス誘導因子に対抗することでアポトーシスを阻害する。こうした役割のため、Hsp70は発がん、神経変性、細胞老化など多くの病理過程に関係している。腫瘍細胞におけるHsp70濃度の上昇は、癌胎児蛋白との複合体形成と安定化、そして細胞内の部位への輸送を行うことで腫瘍細胞の増殖を促進し、腫瘍の悪性度や治療抵抗性を高めている可能性がある[7][18]。こうした理由により、Hsp70を標的としたがんワクチン戦略は動物モデルで高い成功を収めており、臨床試験へ進行している[7]。一方、Hsp70の過剰発現は心筋細胞における虚血再灌流による損傷や、アルツハイマー病、パーキンソン病、ハンチントン病、脊髄小脳変性症などの神経変性疾患による損傷、また加齢や細胞老化を緩和する。百寿者では、熱ショック後にHsp70産生の強力な誘導が観察される[18][19]。特に、Hsc70は上述した疾患のほか、統合失調症などの精神神経疾患においても保護的役割を果たしている[20]。Hsc70は他のHsp70タンパク質とともに幅広いシャペロンインタラクトームのネットワークを形成してタンパク質恒常性を保護する役割を果たしており、また老化した脳やアルツハイマー病、パーキンソン病、ハンチントン病の患者の脳では抑制されている[21]。
相互作用
Hsc70は、Hsp40、Hsp90、HIP、HOP、BAG1と相互作用してシャペロン複合体を形成する[12]。
HSPA8は次に挙げる因子と相互作用することが示されている。
出典
関連文献
外部リンク
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads