Timeline
Chat
Prospettiva
Laurilsolfato di sodio
composto chimico Da Wikipedia, l'enciclopedia libera
Remove ads
Il laurilsolfato di sodio (o sodio laurilsolfato, sodio lauril solfato, sodio dodecilsolfato, dodecilsolfato di sodio, SLS, SDS) è un tensioattivo usato in molte famiglie di prodotti come dentifrici, shampoo, schiuma da barba e bolle di sapone grazie al suo effetto schiumogeno.
Remove ads
A temperatura ambiente si presenta come una polvere cristallina bianca, abbastanza solubile in acqua e etanolo.
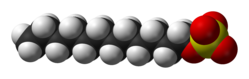
La molecola è costituita da una coda idrofoba di 12 atomi di carbonio attaccata ad un gruppo idrofilo solfato, da cui le proprietà anfifiliche necessarie ad un detergente. Probabilmente è il tensioattivo anionico più usato e studiato.
Remove ads
Produzione
Si ottiene dalla solfonazione dell'1-dodecanolo (o alcool laurilico, C12H25OH) seguita dalla neutralizzazione con il carbonato di sodio.
Reattività
Per etossilazione viene convertito nel sodio lauriletere solfato (SLES), meno aggressivo verso la pelle perché essendo un solvente meno efficace è meno aggressivo nei confronti delle proteine.
Utilizzo
È usato sia in ambienti industriali che per cosmesi casalinga (saponi detergenti, shampoo, bagni schiuma). Come tutti i detergenti tensioattivi, promuove il distacco e la rimozione del grasso (sebo) dalla pelle e ne può causare la sensazione di secchezza.
Utilizzo in biochimica
L'SDS è usato in biochimica per la preparazione di proteine per SDS-PAGE (elettroforesi su gel di poliacrilammide). L'SDS rompe i legami non-covalenti (interazioni idrofobiche e legami idrogeno) nelle proteine e dunque le denatura, facendo perdere loro la conformazione nativa.
Inoltre, la componente anionica dell'SDS lega la catena peptidica (uno ione SDS ogni due residui aminoacidici). Questo conferisce una carica negativa alla proteina proporzionale alla sua massa (circa 1,4 g SDS/g proteina). Questa carica negativa è significativamente maggiore della carica elettrica originale. La repulsione elettrostatica che si viene a creare dal legame dell'SDS causa la denaturazione della proteina ad una struttura filiforme, eliminando le differenze di migrazione dovute alla differenza di struttura. Ciò permette di separare le proteine esclusivamente in base al loro peso molecolare.
Effetti sulla salute
L'SDS ha stimolato diversi accertamenti circa la sua sicurezza, legati soprattutto a suoi effetti irritanti ad elevate concentrazioni.[2][3][4]
Tra gli effetti dimostrati:
- Possibili dermatiti.[4][5][6]
- Lo SLES (sodio lauriletere solfato) è sostanzialmente meno aggressivo dello SDS.
- Lo SDS può causare afte in soggetti predisposti.[7][8]
- SDS viene spesso usato al posto dello SLES in molti prodotti in quanto è più economico.
L'American Cancer Society ha dichiarato che l'SDS non è cancerogeno, e precisa che la sostanza, anche se nella sua funzione di detergente è irritante per la pelle, inizia ad essere pericolosa solo ad alte concentrazioni, maggiori di quelle usate correntemente in cosmesi.[9]
Remove ads
Note
Altri progetti
Collegamenti esterni
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads