Loading AI tools
composto chimico Da Wikipedia, l'enciclopedia libera
Il fluoruro di tionile o difluoruro di tionile è il composto inorganico con formula SOF2. In condizioni normali è un gas incolore di odore soffocante.[1] In questo composto lo zolfo ha stato di ossidazione +4.
| Fluoruro di tionile | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| difluoro(osso)-λ4-solfano | |
| Nomi alternativi | |
| difluoruro di tionile | |
| Caratteristiche generali | |
| Formula bruta o molecolare | F2OS |
| Aspetto | gas incolore |
| Numero CAS | |
| Numero EINECS | 231-997-2 |
| PubChem | 24548 |
| SMILES | O=S(F)F |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,780 (-100 °C)[1] |
| Solubilità in acqua | reagisce |
| Temperatura di fusione | −129,5 °C (144 K)[2] |
| Temperatura di ebollizione | −43,8 °C (229 K)[2] |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| Frasi H | 300 - 310 - 330 - 314 [3] |
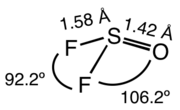
SOF2 è un composto molecolare, gassoso a temperatura ambiente. La forma della molecola è quella di una di piramide distorta, con simmetria Cs.[4] Le distanze S-O e S-F sono rispettivamente 142,0 pm e 158,3 pm; gli angoli O-S-F e F-S-F sono rispettivamente 106,2° and 92,8°. I corrispondenti alogenuri SOCl2 e SOBr2 hanno strutture simili, ma sono liquidi a temperatura ambiente. Sono noti anche alogenuri misti, tipo SOClF e SOBrF.[2]
Il fluoruro di tionile fu ottenuto per la prima volta nel 1896 da Maurice Meslans (1862-1938), allievo di Henri Moissan, trattando cloruro di tionile con fluoruro di zinco.[5] In seguito furono usate altre fonti di ioni fluoruro, come il fluoruro di idrogeno[1] o il trifluoruro di antimonio:[2][6]
Alternativamente si può fluorurare il diossido di zolfo con pentafluoruro di fosforo:[2]
SOF2 è un gas termicamente stabile fino al calor rosso. Al di sotto di 125 ºC non attacca né il vetro né i metalli ferro, nichel, cobalto, mercurio, magnesio alluminio e zinco.[1] A contatto con acqua si idrolizza formando diossido di zolfo e acido fluoridrico:[2]
Reagisce con il fluoro per formare tetrafluoruro di tionile:[2]
Chimicamente SOF2 si comporta come una base di Lewis debole, tramite il doppietto non condiviso sull'ossigeno, e anche come acido di Lewis debole, legandosi tramite lo zolfo; in questo senso reagisce con ioni F− formando l'anione [O=SF3]–.[2]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.