Loading AI tools
composto chimico Da Wikipedia, l'enciclopedia libera
Il pentafluoruro di platino o fluoruro di platino(V) è il composto binario di formula PtF5. È uno dei pochi composti dove il platino ha stato di ossidazione +5 (altri esempi sono quelli contenenti l'anione PF6− come O2PtF6 e XePtF6).[1]
| Pentafluoruro di platino | |
|---|---|
 | |
| Nome IUPAC | |
| pentafluoruro di platino, fluoruro di platino(V) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | PtF5 |
| Massa molecolare (u) | 290,07 |
| Aspetto | solido rosso |
| Numero CAS | |
| SMILES | F[Pt](F)(F)(F)F |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | reazione violenta |
| Temperatura di fusione | 80 °C (353 K)[1] |
| Temperatura di ebollizione | 300 °C (573 K)[1] |
| Indicazioni di sicurezza | |
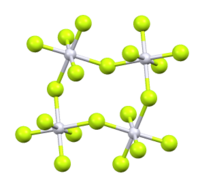
PtF5 ha una struttura tetramerica analoga ai pentafluoruri di rutenio e osmio. Ogni atomo di platino ha coordinazione ottaedrica, con due leganti fluoruro a ponte.[2]
PtF5 cristallizza nel sistema monoclino, gruppo spaziale P21/c, con costanti di reticolo a = 552 pm, c = 1243 pm e β = 99,98°, con 4 unità di formula per cella elementare.[3]
Il composto fu sintetizzato per la prima volta da Neil Bartlett nel 1960.[4] PtF5 si può ottenere tramite fluorurazione controllata ad alta temperatura e sotto pressione:[1]
oppure per reazione tra dicloruro di platino e fluoro a 350 °C:[5]
PtF5 è uno degli ossidanti più forti conosciuti. È stato usato per ossidare O2 a O2+[PtF6]− e Xe a XePtF6.[2] Reagisce violentemente in acqua ossidandola a ossigeno:[1]
Per riscaldamento disproporziona a PtF4 e PtF6:[5]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.