
Acido butirrico
composto chimico / Da Wikipedia, l'enciclopedia encyclopedia
Caro Wikiwand AI, Facciamo breve rispondendo semplicemente a queste domande chiave:
Puoi elencare i principali fatti e statistiche su Acido butirrico?
Riassumi questo articolo per un bambino di 10 anni
L'acido butirrico (dal greco βούτυρος, burro), anche denominato acido butanoico (secondo la terminologia IUPAC), è un acido carbossilico di formula CH3CH2CH2-COOH, che si trova principalmente esterificato col glicerolo in molti grassi naturali, animali e vegetali.
| Acido butirrico | |
|---|---|
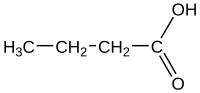 | |
 | |
| Nome IUPAC | |
| Acido butanoico | |
| Nomi alternativi | |
| Acido n-butirrico Acido etilacetico Acido propano-1-carbossilico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H8O2 |
| Massa molecolare (u) | 88,1 |
| Aspetto | liquido oleoso, incolore |
| Numero CAS | 107-92-6 |
| Numero EINECS | 203-532-3 |
| PubChem | 264 |
| DrugBank | DBDB03568 |
| SMILES | CCCC(=O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 0,959 |
| Indice di rifrazione | 1.3991 |
| Costante di dissociazione acida (pKa) a 298,15 K | 4,82 |
| Costante di dissociazione acida a 298,15 K | 1,52 × 10⁻⁵ |
| Temperatura di ebollizione | 163,5 °C (463,5 K) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 170 °C (443 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 302 - 314 |
| Consigli P | 260 - 280 - 301+312+330 - 303+340+310 - 305+351+338+310 [1] |
In forma libera si rinviene a seguito dei processi di rancidificazione (idrolisi) di detti grassi soprattutto nel burro rancido, nei formaggi stagionati (come Parmigiano Reggiano e Grana Padano), eccetera. Si forma in precisi processi di fermentazione degli zuccheri (fermentazione butirrica), e per i processi di digestione gastrica dei grassi, iniziante con l'idrolisi degli esteri gliceridi ad opera dell'acido cloridrico, si rinviene insieme agli altri acidi deboli nel vomito, oltre che nei frutti del Ginkgo biloba.
L'acido butirrico è caratterizzato dall'odore poco gradevole se presente in elevata concentrazione e dal sapore acre, con un retrogusto dolciastro (simile all'etere dietilico). In basse concentrazioni costituisce, insieme ai suoi esteri, aroma caratteristico di alcuni formaggi fermentati. L'acido butirrico è riconosciuto dai mammiferi dalle buone capacità olfattive (come i cani) in 10 ppb, e gli umani ne riconoscono concentrazioni in 10 ppm.
Il gliceride dell'acido butirrico costituisce dal 3% al 4% della massa del burro, e quando questo irrancidisce, l'acido si libera dal gliceride per idrolisi, generando il cattivo odore.
L'acido butirrico normale, detto anche acido butirrico di fermentazione, si trova anche come un estere esilico nell'olio di Heracleum giganteum e come estere octile nella Pastinaca sativa, piante della stessa famiglia; è anche stato rinvenuto nella carne viva, durante i processi di sudorazione.
Ordinariamente l'acido butirrico è un composto che si prepara dagli zuccheri o dall'amido, tramite fermentazione innescata da formaggi fermentati, con aggiunta di carbonato di calcio allo scopo di salificare altri acidi che dovessero formarsi nel processo. La fermentazione butirrica dell'amido è aiutata dall'aggiunta diretta di Bacillus subtilis.
L'acido butirrico è necessario nella preparazione di una quantità di esteri butirrati: Gli esteri dal basso peso molecolare nell'acido butirrico, come il metilbutirrato hanno in gran parte sapori e odori gradevoli, e conseguentemente trovano ampio uso nell'industria profumiera e degli aromi alimentari.
L'acido è un liquido oleoso e incolore, che solidifica a -8 °C, e bolle a 164 °C. È facilmente solubile in acqua, etanolo ed etere, ed emerge dalla sua soluzione acquosa con l'aggiunta di cloruro di calcio. Il dicromato di potassio e l'acido solforico lo ossidano in diossido di carbonio e acido acetico, mentre il basico permanganato di potassio lo ossida in diossido di carbonio. Il sale a base di calcio Ca(C4H7O2)2·H2O, è meno solubile in acqua calda che in quella fredda.
Esiste un isomero, l'acido isobutirrico, che condivide con l'acido butirrico la formula C4H8 O2, ma possiede una struttura diversa. A fronte di simili proprietà chimiche, esistono differenze tra le proprietà fisiche.