բակտերիայի տեսակ From Wikipedia, the free encyclopedia
Ոսկեգույն ստաֆիլոկոկ (լատ. Staphylococcus aureus), ֆիրմիկյուտների դասին պատկանող գրամ-դրական բակտերիա, մարմնի միկրոֆլորայի մաս, հիմնականում գտնվում է վերին շնչուղիներում և մաշկի վրա։ Այն հաճախ դրական է կատալազի և նիտրատների վերականգնման համար և հանդիսանում է ֆակուլտատիվ անաէրոբ, որը կարող է աճել առանց թթվածնի անհրաժեշտության[1]։ Չնայած S. aureus-ը սովորաբար հանդես է գալիս որպես մարդու միկրոֆլորայի համադրիչ, այն կարող է նաև դառնալ պաթոգեն՝ հանդիսանալով մաշկի վարակների տարածված պատճառ՝ ներառյալ թարախակույտերը, շնչառական վարակները, ինչպիսիք են սինուսիտը և սննդային թունավորումը։ հարուցիչշտամները հաճախ նպաստում են բորբոքումների առաջացմանը՝ առաջացնելով վիրուսային գործոններ, ինչպիսիք են ուժեղ սպիտակուցային տոքսինները և բջջային մակերեսի սպիտակուցի արտահայտումը, որը միանում և ապաակտիվացնում է հակամարմինները։ S. aureus-ը հակամանրէային դիմադրության և հակաբիոտիկների նկատմամբ շտամների առաջացմամբ, ինչպիսին է մետիցիլինի նկատմամբ կայուն S. aureus-ը (methicilin resistant S. Aureus, MRSA), մահացությունների առաջատար պաթոգեններից մեկն է, ինչը համաշխարհային խնդիր է կլինիկական բժշկության մեջ։ Չնայած բազմաթիվ հետազոտություններին և մշակումներին, S. aureus-ի դեմ պատվաստանյութ չի հաստատվել։
| Ոսկեգույն ստաֆիլոկոկ | |
|---|---|
 | |
| Տեսակ | տաքսոն |
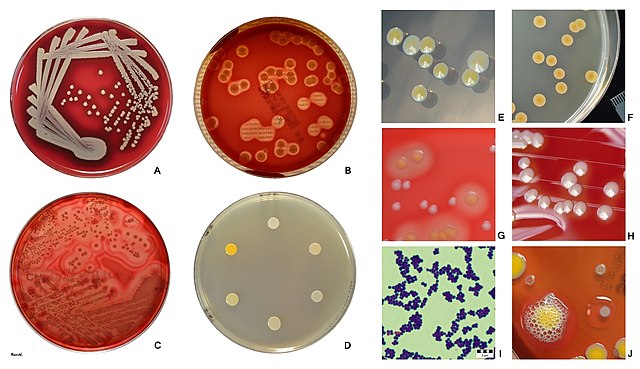

Մարդկային բնակչության մոտ 20%-ից 30%-ը S. aureus-ի երկարաժամկետ կրողներ են[2][3]. այն կարող է հայտնաբերվել նորմալ մաշկի միկրոֆլորայում, քթանցքներում[2][4] և կանանց ստորին վերարտադրողական տրակտում[5][6]։ S. aureus-ը կարող է առաջացնել մի շարք հիվանդություններ՝ սկսած աննշան մաշկային վարակներից, ինչպիսիք են բշտիկները[7], շփաբորբ, թարախակույտ, ցելյուլիտ, բշտիկաբորբ, կարբունկուլներ, այրված մաշկի համախտանիշ և թարախակույտներ, մինչև կյանքին սպառնացող հիվանդություններ, ինչպիսիք են թոքաբորբը, մենինգիտը, օստեոմիելիտը, էնդոկարդիտը, թունավոր շոկի համախտանիշ, բակտերեմիա և սեպսիս։ Այն դեռևս հիվանդանոցում ձեռք բերված վարակների հինգ ամենատարածված պատճառներից մեկն է և հաճախ վիրահատությունից հետո վերքերի վարակման պատճառ է հանդիսանում։ Ամեն տարի մոտ 500,000 հիվանդանոցային հիվանդներ ԱՄՆ-ում ստանում են ստաֆիլոկոկային վարակ, հիմնականում S. aureus-ով[8]։ ԱՄՆ-ում տարեկան մինչև 50,000 մահ կապված է ստաֆիլոկոկային վարակի հետ[9]։
1880 թվականին շոտլանդացի վիրաբույժ Ալեքսանդր Օգսթոնը՝ իր կատարած վիրահատական թարախակույտից բակտերիաների խմբերը նկատելուց հետո, հայտնաբերեց, որ ստաֆիլոկոկը կարող է վերքերի բորբոքումներ առաջացնել։ Նա այն անվանել է ստաֆիլոկոկ՝ մանրադիտակի տակ երևացող կլաստերային տեսքից պատճառով։ Այնուհետև, 1884 թվականին, գերմանացի գիտնական Ֆրիդրիխ Յուլիուս Ռոզենբախը հայտնաբերեց Staphylococcus aureus-ը՝ տարբերակելով և առանձնացնելով այն Staphylococcus albus-ից՝ հարակից բակտերիայից։ 1930-ականների սկզբին բժիշկները սկսեցին օգտագործել ավելի պարզ թեստ՝ կոագուլազի փորձարկման միջոցով հայտնաբերելու S. aureus վարակի առկայությունը, որը թույլ է տալիս հայտնաբերել բակտերիայից արտադրվող ֆերմենտը։ Մինչև 1940-ական թվականները, S. aureus վարակները մահացու էին հիվանդների մեծամասնության մոտ։ Այնուամենայնիվ, բժիշկները պարզեցին, որ պենիցիլինի օգտագործումը կարող է բուժել S. aureus վարակը։ Ցավոք, 1940-ականների վերջում պենիցիլինի դիմադրությունը լայն տարածում գտավ այս բակտերիաների պոպուլյացիայի շրջանում և սկսեցին առաջանալ դիմացկուն շտամի բռնկումներ[10]։
Staphylococcus aureus-ը կարելի է դասակարգել մարդում մարմնի վրայի տասը գերիշխող բակտերիալ ընտանիքներից։ Կան նաև բազմաթիվ փոքր ընտանիքներ, բայց դրանք այնքան էլ հաճախ չեն երևում բնակչության մեջ։ Նույն ընտանիքի մեջ գտնվող բակտերիաների գենոմները հիմնականում պահպանված են, բացառությամբ շարժական գենետիկական տարրերի։ Շարժական գենետիկական տարրերը, որոնք տարածված են ոսկեգույն ստաֆիլոկոկում, ներառում են բակտերիոֆագները, ախտածին կղզյակները, պլազմիդները, տրանսպոզոնները և ստաֆիլոկոկային կասետային քրոմոսոմները։ Այս տարրերը հնարավորություն են տվել S. aureus-ին շարունակաբար զարգանալ և ձեռք բերել նոր հատկանիշներ։ S. aureus տեսակի մեջ կան գենետիկական մեծ տատանումներ։ Fitzgerald et al.-ի (2001 թվական) ուսունասիրությունը պարզել է, որ S. aureus գենոմի մոտավորապես 22%-ը չկոդավորող է և, հետևաբար, կարող է տարբերվել բակտերիայից բակտերիա։ Այս տարբերության օրինակը երևում է տեսակի վիրուլենտության մեջ։ S. aureus-ի միայն մի քանի շտամներ են կապված մարդկանց վարակների հետ։ Սա ցույց է տալիս, որ տեսակների մեջ առկա է վարակիչ կարողությունների մեծ շրջանակ[11]։
Առաջարկվել է, որ տեսակի ներսում մեծ տարասեռության հնարավոր պատճառներից մեկը կարող է պայմանավորված լինել տարասեռ վարակների վրա նրա կախվածությամբ։ Սա տեղի է ունենում, երբ S. aureus-ի մի քանի տարբեր տեսակներ վարակ են առաջացնում տիրոջ ներսում։ Տարբեր շտամները կարող են արտազատել տարբեր ֆերմենտներ կամ խմբին բերել հակաբիոտիկների տարբեր դիմադրողականություն՝ մեծացնելով նրա ախտածին կարողությունը[12]։ Այսպիսով, մեծ թվով մուտացիաների և շարժական գենետիկ տարրերի ձեռքբերումների կարիք կա։
Մեկ այլ ուշագրավ էվոլյուցիոն գործընթաց S. aureus տեսակի ներսում նրա համատեղ էվոլյուցիան է իր մարդկային կրողների հետ։ Ժամանակի ընթացքում մակաբուծությունը հանգեցրել է նրան, որ բակտերիան կարող է տեղափոխվել մարդկանց քիթ-կոկորդում առանց ախտանիշների կամ վարակի առաջացնելու։ Սա թույլ է տալիս այն փոխանցել ողջ մարդկային պոպուլյացիան՝ բարձրացնելով ոսկեգույն ստաֆիլոկոկի դիմադրողականությունը որպես տեսակ[13]։ Այնուամենայնիվ, մարդկային պոպուլյացիայի մոտավորապես 50%-ն է S. aureus-ի կրողներ, ընդ որում 20%-ը որպես շարունակական, իսկ 30%-ը՝ ընդհատվող։ Սա գիտնականներին ստիպում է ենթադրել, որ կան բազմաթիվ գործոններ, որոնք որոշում են, թե արդյոք S. aureus-ը մարդկանց մոտ անցնում է ասիմպտոմատիկ, ներառյալ նրանք, որոնք հատուկ են առանձին անձին։ Համաձայն 1995 թվականին Հոֆմանի և այլոց կատարած ուսումնասիրության՝ այս գործոնները կարող են ներառել տարիքը, սեռը, շաքարախտը և ծխելը։ Նրանք նաև որոշեցին մարդկանց գենետիկական հատկանիշները, որոնք հանգեցնում են S. aureus-ի գաղութացման ունակության բարձրացմանը, մասնավորապես, գլյուկոկորտիկոիդային ընկալիչի գենի պոլիմորֆիզմին, որը հանգեցնում է կորտիկոստերոիդների ավելի մեծ արտադրության։ Եզրափակելով, կան ապացույցներ, որ այս մանրէի ցանկացած շտամ կարող է դառնալ ինվազիվ, քանի որ դա մեծապես կախված է մարդկային գործոններից[14]։
Թեև S. aureus-ն ունի արագ վերարտադրողական և միկրոէվոլյուցիոն տեմպեր, կան բազմաթիվ խոչընդոտներ, որոնք կանխում են այս տեսակների էվոլյուցիան։ Այդպիսի խոչընդոտներից մեկը AGR-ն է, որը բակտերիաների ներսում գլոբալ օժանդակ գեների կարգավորիչ է։ Նման կարգավորիչը կապված է բակտերիաների վիրուսային մակարդակի հետ։ Պարզվել է, որ այս գենում գործող մուտացիաների կորուստը մեծացնում է այն պարունակող բակտերիաների դիմադրողականությունը։ Այսպիսով, S. aureus-ը պետք է փոխզիջում կատարի՝ որպես տեսակ իրենց դիմադրությունը բարձրացնելու համար՝ փոխանակելով նվազեցված վիրուլենտությունը դեղորայքային դիմադրության բարձրացման հետ։ Էվոլյուցիայի մյուս խոչընդոտը Sau1 Type I սահմանափակման փոփոխման (restriction modification, RM) համակարգն է։ Այս համակարգը գոյություն ունի, որպեսզի պաշտպանի բակտերիան օտար ԴՆԹ-ից՝ մարսելով այն։ ԴՆԹ-ի փոխանակումը նույն ընտանիքի միջև արգելափակված չէ, քանի որ նրանք ունեն նույն ֆերմենտները, և RM համակարգը չի ճանաչում նոր ԴՆԹ-ն որպես օտար, բայց տարբեր ընտանիքների միջև փոխանցումն արգելափակված է[12]։


S. aureus (/ˌstæfᵻləˈkɒkəs ˈɔːriəs, -loʊ-/[15][16], հունարեն σταφυλόκοκκος, «խաղողի ողկույզ», լատիներեն aureus, «ոսկե») ֆակուլտատիվ անաէրոբ, գրամ-դրական կոկկալ (կլոր) բակտերիա է, որը հայտնի է "golden staph" և "oro staphira" անունով։ S. aureus-ը անշարժ է և սպորներ չի առաջացնում։ Բժշկական գրականության մեջ մանրէն հաճախ կոչվում է S. aureus, Staph aureus կամ Staph a.[17]։ Այն հայտնվում է որպես ստաֆիլոկոկ (խաղողի ողկույզներին նմանվող), երբ դիտվում է մանրադիտակով և ունի մեծ, կլոր, ոսկեդեղնավուն գաղութներ, հաճախ հեմոլիզով, երբ աճեցվում է արյան ագարի թիթեղների վրա[18]։ S. aureus-ը բազմանում է անսեռ ճանապարհով՝ երկուական տրոհումով։ Դուստր բջիջների ամբողջական տարանջատումը միջնորդվում է S. aureus ավտոլիզինի (autolysin) միջոցով, և դրա բացակայության կամ նպատակային արգելակման դեպքում դուստր բջիջները մնում են միմյանց կցված և հայտնվում որպես կլաստերներ[19]։
S. aureus-ը կատալազային դրական է (նշանակում է, որ այն կարող է արտադրել կատալազ ֆերմենտը)։ Կատալազը փոխակերպում է ջրածնի պերօքսիդը (H2Օ2) ջրի և թթվածնի. Կատալազի ակտիվության թեստերը երբեմն օգտագործվում են ստաֆիլոկոկը էնտերոկոկից և ստրեպտոկոկից տարբերելու համար։ Նախկինում այն տարբերվում էր այլ ստաֆիլոկոկներից կոագուլազային թեստի միջոցով։ Այնուամենայնիվ, S. aureus-ի ոչ բոլոր շտամներն են կոագուլազ-դրական[18][20], և տեսակների սխալ նույնականացումը կարող է ազդել բուժման և վերահսկման արդյունավետ միջոցառումների վրա[21]։
Բնական գենետիկական փոխակերպումը վերարտադրողական գործընթաց է, որը ներառում է ԴՆԹ-ի տեղափոխում մի բակտերիայից մյուսը միջանկյալ միջավայրի միջոցով և դոնորի հաջորդականության ինտեգրումը ստացողի գենոմին հոմոլոգ վերադասավորման միջոցով։ Պարզվել է, որ S. aureus-ն ունակ է բնական գենետիկ փոխակերպման, բայց միայն ցածր հաճախականությամբ՝ կիրառված փորձարարական պայմաններում[22]։ Հետագա ուսումնասիրությունները ցույց են տվել, որ բնական գենետիկական փոխակերպման իրավասության զարգացումը կարող է էականորեն ավելի բարձր լինել համապատասխան պայմաններում, որը դեռ պետք է բացահայտվի[23]։
Մարդկանց մոտ S. aureus-ը կարող է առկա լինել վերին շնչուղիներում, աղիների լորձաթաղանթում և մաշկի մեջ՝ որպես նորմալ միկրոֆլորայի մասնիկ[24][25][26]։ Այնուամենայնիվ, քանի որ S. aureus-ը կարող է հիվանդություն առաջացնել որոշակի հյուրընկալող և շրջակա միջավայրի պայմաններում, այն բնութագրվում է որպես «պաթոբիոնտ»[24]։


Թեև S. aureus-ը սովորաբար հանդես է գալիս որպես համակցված բակտերիա՝ ասիմպտոմատիկ կերպով գաղութացնելով մարդու բնակչության մոտ 30%-ին, այն երբեմն կարող է առաջացնել հիվանդություն[3]։ Մասնավորապես, S. aureus-ը բակտերեմիայի և վարակիչ էնդոկարդիտի ամենատարածված պատճառներից է։ Բացի այդ, այն կարող է առաջացնել մաշկի և փափուկ հյուսվածքների տարբեր ինֆեկցիաներ[3], հատկապես, երբ վնասվել են մաշկի կամ լորձաթաղանթի պաշտպանիչ շերտը։
S. aureus վարակը կարող է տարածվել վարակված վերքի թարախի, վարակված անձի հետ մաշկ-մաշկ շփման և վարակված անձի կողմից օգտագործվող առարկաների հետ շփման միջոցով, ինչպիսիք են սրբիչները, սավանները, հագուստը կամ սպորտային սարքավորումները։ Հոդերի փոխարինումը մարդուն դնում է սեպտիկ արթրիտի, ստաֆիլոկոկային էնդոկարդիտի (սրտի փականների ինֆեկցիա) և թոքաբորբի ռիսկի առաջ[27]։
Կանխարգելիչ միջոցառումները ներառում են ձեռքերը հաճախ օճառով լվանալը և ամեն օր լոգանք կամ ցնցուղ ընդունելը։
Այն բժշկական իմպլանտների վրա քրոնիկ կենսաթաղանթային վարակների զգալի պատճառ է հանդիսանում, և տոքսինների ռեպրեսորը վարակի ուղու մի մասն է[28]։
S. aureus-ը կարող է տարիներ շարունակ քնած մնալ մարմնում՝ չբացահայտված։ Երբ ախտանիշները սկսում են դրսևորվել, տերը վարակիչ է ևս երկու շաբաթ, և ընդհանուր հիվանդությունը տևում է մի քանի շաբաթ։ Այնուամենայնիվ, եթե չբուժվի, հիվանդությունը կարող է մահացու լինել[29]։ Խորը ներթափանցող S. aureus վարակները կարող են ծանր լինել։
Մաշկային բորբոքումները S. aureus վարակի ամենատարածված ձևն են։ Սա կարող է դրսևորվել տարբեր ձևերով, ներառյալ փոքր բարորակ թարախակույտերը, ֆոլիկուլիտը, շփաբորբ, ցելյուլիտը և փափուկ հյուսվածքների ավելի ծանր, ինվազիվ վարակները[3][7]։
Այն չափազանց տարածված է ատոպիկ դերմատիտով մարդկանց մոտ, որն ավելի հաճախ հայտնի է որպես էկզեմա[30]։ Այն հիմնականում հանդիպում է մարմնի ակտիվ մասերում, ներառյալ թևատակերը, մազերը և գլխամաշկը։ Խոշոր բշտիկները, որոնք հայտնվում են այդ հատվածներում, կարող են սրել վարակը, եթե պատռվեն։ Սա կարող է հանգեցնել ստաֆիլոկոկային այրված մաշկի համախտանիշի, որի ծանր ձևը կարելի է տեսնել նորածինների մոտ[31]։
Ատոպիկ դերմատիտով հիվանդների մոտ S. aureus-ի առկայությունը բերանային հակաբիոտիկներով բուժման ցուցում չէ, քանի որ ապացույցները ցույց չեն տվել, որ դա օգտակար է հիվանդին[32][33]։ Այնուամենայնիվ, պարզվել է, որ հակաբիոտիկները, որոնք զուգորդվում են կորտիկոստերոիդների հետ, բարելավում են վիճակը[34]։ S. aureus-ի գաղութացումը վատթարացնում է ատոպիկ դերմատիտը[30][35]։ Ենթադրվում է, որ S. aureus-ն օգտագործում է ատոպիկ դերմատիտով հիվանդների մաշկի պաշտպանիչ շերտի թերությունները՝ առաջացնելով ցիտոկինների էքսպրեսիա և, հետևաբար, սրելով ախտանիշները[36]։
S. aureus-ը պատասխանատու է սննդային թունավորումների համար նույնպես և դրան հասնում է մարդու օրգանիզմում տոքսիններ առաջացնելու միջոցով[37]։ Նրա ինկուբացիոն շրջանը տևում է մեկից վեց ժամ[38], իսկ ինքնին հիվանդությունը տևում է 30 րոպեից մինչև 3 օր[39]։ Կանխարգելիչ միջոցառումները, որոնք կարելի է ձեռնարկել՝ օգնելու կանխել հիվանդության տարածումը, ներառում են ձեռքերը մանրակրկիտ լվանալ օճառով և ջրով սնունդ պատրաստելուց առաջ։ Հիվանդության դեպքում հեռու մնացեք ցանկացած սննդից և կրեք ձեռնոցներ, եթե սնունդ պատրաստելիս ձեռքերին կամ դաստակներին բաց վերքեր են առաջանում։ Եթե սնունդը պահում եք 2 ժամից ավելի, սննդամթերքը պահեք 4.4-ից ցածր կամ 60 °C-ից բարձր (40 °F-ից ցածր կամ 140 °F-ից բարձր ջերմաստիճանում)[40]։
S. aureus-ը ոսկրերի և հոդերի ծանր վարակների, ներառյալ օստեոմիելիտի, սեպտիկ արթրիտի և հոդերի փոխարինման վիրահատություններից հետո վարակների տարածված պատճառն է[3][41][42]։
S. aureus-ը արդյունաբերական երկրների մեծ մասում արյան հոսքի վարակների առաջատար պատճառն է[41]։ Վարակումը սովորաբար կապված է մաշկի կամ լորձաթաղանթների վնասվածքների հետ՝ վիրահատության, վնասվածքի կամ ներանոթային սարքերի օգտագործման, ինչպիսիք են կաթետրը, հեմոդիալիզի մեքենաները կամ ներարկվող դեղերը[3][41]։ Բակտերիաները արյան մեջ մտնելուց հետո կարող են վարակել տարբեր օրգաններ՝ առաջացնելով վարակիչ էնդոկարդիտ, սեպտիկ արթրիտ և օստեոմիելիտ[41]։ Այս հիվանդությունը հատկապես տարածված և ծանր է շատ երիտասարդ և շատ մեծահասակների մոտ[3]։
Առանց հակաբիոտիկների բուժման, S. aureus բակտերեմիան ունի մահացության մակարդակ մոտ 80%[3]։ Հակաբիոտիկների բուժման դեպքում մահացության մակարդակը տատանվում է 15%-ից մինչև 50%՝ կախված հիվանդի տարիքից և առողջական վիճակից, ինչպես նաև S. aureus շտամի հակաբիոտիկ դիմադրողականությունից[3]։
S. aureus-ը հաճախ հանդիպում է կենսաթաղանթերում, որոնք ձևավորվում են մարմնում կամ մարդու հյուսվածքի վրա տեղադրված բժշկական սարքերի վրա։ Այն սովորաբար հայտնաբերվում է մեկ այլ հարուցչի՝ Candida albicans-ի հետ՝ ձևավորելով բազմատեսակ կենսաթաղանթներ։ Վերջինս կասկածվում է, որ օգնում է S. aureus-ին ներթափանցել մարդու հյուսվածք[9]։ Ավելի բարձր մահացությունը կապված է բազմատեսակ կենսաթաղանթերի հետ[43]։
S. aureus կենսաթաղանթը օրթոպեդիկ իմպլանտների հետ կապված ինֆեկցիաների գերակշռող պատճառն է, սակայն հայտնաբերված է նաև սրտի իմպլանտների, անոթային պատվաստումների, տարբեր կաթետրների և կոսմետիկ վիրաբուժական իմպլանտների վրա[44][45]։ Իմպլանտացիայից հետո այս սարքերի մակերեսը պատվում է հյուրընկալող սպիտակուցներով, որոնք հարուստ մակերես են ապահովում բակտերիաների կցման և կենսաթաղանթի ձևավորման համար։ Երբ սարքը վարակվում է, այն պետք է ամբողջությամբ հեռացվի, քանի որ S. aureus կենսաթաղանթը չի կարող ոչնչացվել հակաբիոտիկների միջոցով[45]։
S. aureus կենսաթաղանթի միջնորդավորված վարակների ներկայիս թերապիան ներառում է վարակված սարքի վիրահատական հեռացում, որին հաջորդում է հակաբիոտիկ բուժում։ Միայն սովորական հակաբիոտիկ բուժումը արդյունավետ չէ նման վարակների վերացման համար[44]։ Հետվիրահատական հակաբիոտիկ բուժման այլընտրանքը հակաբիոտիկներով հագեցած, լուծվող կալցիումի սուլֆատի գնդիկների օգտագործումն է, որոնք տեղադրվում են բժշկական սարքի հետ միասին։ Այս գնդիկները կարող են հակաբիոտիկների բարձր չափաբաժիններ թողարկել ցանկալի վայրում՝ նախնական վարակը կանխելու համար[45]։
Ուսումնասիրվում են S. aureus կենսաթաղանթի նոր բուժումները, որոնք ներառում են նանո արծաթի մասնիկներ, բակտերիոֆագներ և բույսերից ստացված հակաբիոտիկ նյութեր։ Այս նյութերը կենսաթաղանթերում ներկառուցված S. aureus-ի դեմ արգելակող ազդեցություն են ցուցաբերել[46]։ Հայտնաբերվել է, որ ֆերմենտների մի դաս ունեն կենսաթաղանթի մատրիցը քայքայելու հատկություն, ուստի կարող են օգտագործվել որպես կենսաթաղանթի ցրման միջոց՝ հակաբիոտիկների հետ համատեղ[47]։
S. aureus-ը կարող է գոյատևել շների[48], կատուների[49] և ձիերի վրա[50], իսկ հավերի մոտ կարող է առաջացնել իշամուղ[51]։ Ոմանք կարծում են, որ բուժաշխատողների շները պետք է համարվեն հակաբիոտիկների նկատմամբ կայուն S. aureus-ի զգալի աղբյուր, հատկապես համաճարակի բռնկման ժամանակ[48]։ 2008 թվականին Boost-ի, O'Donoghue-ի և James-ի կողմից իրականացված ուսումնասիրության մեջ պարզվել է, որ բակտերայի միայն մոտ 90%-ը գաղութացել է ընտանի շների մեջ, որոնք ներկայացված են որպես կայուն առնվազն մեկ հակաբիոտիկի նկատմամբ։ Քթի հատվածը ներգրավված է որպես շների և մարդկանց միջև փոխանցման ամենակարևոր վայր[52]։
S. aureus-ը կաթնատու կովերի մաստիտի պատճառական գործակալներից է։ Դրա մեծ բազմաշաքարային պարկուճը պաշտպանում է օրգանիզմը կովի իմունային պաշտպանությունից[53]։
S. aureus-ը արտադրում է տարբեր ֆերմենտներ, ինչպիսիք են կոագուլազը (կապված և ազատ կոագուլազներ), ինչը հեշտացնում է ֆիբրինոգենի վերածումը ֆիբրինի՝ առաջացնելով թրոմբներ, ինչը կարևոր է մաշկային վարակների դեպքում[54]։ Հիալուրոնիդազը (հայտնի է նաև որպես տարածման ազդակ) քայքայում է հիալուրոնաթթուն և օգնում դրա տարածմանը։ Դեզօքսիռիբոնուկլեազը, որը քայքայում է ԴՆԹ-ն, պաշտպանում է S. aureus-ը նեյտրոֆիլային արտաբջջային թակարդի միջոցով ոչնչացումից[55][56]։ Այն նաև արտադրում է լիպազ՝ լիպիդները մարսելու համար, ստաֆիլոկինազը՝ ֆիբրինը լուծելու և տարածմանը նպաստելու համար, և բետա-լակտամազ՝ դեղամիջոցների դիմադրության համար[57]։
Կախված շտամից, S. aureus-ը ունակ է արտազատել մի քանի էկզոտոքսիններ, որոնք կարելի է դասակարգել երեք խմբի։ Այս տոքսիններից շատերը կապված են կոնկրետ հիվանդությունների հետ[58]։
Սեկրեցիայի համակարգը բարձր մասնագիտացված բազմաբնույթ սպիտակուցային միավոր է, որը ներկառուցված է բջջային ծրարի մեջ՝ էֆեկտոր սպիտակուցները բջջի ներսից դեպի արտաբջջային տարածություն կամ թիրախ հյուրընկալող ցիտոզոլ տեղափոխելու ֆունկցիա։ T7SS-ի ճշգրիտ կառուցվածքը և գործառույթը դեռ պետք է լիովին պարզաբանվեն։ Ներկայումս չորս սպիտակուցներ հայտնի են S. aureus Type VII սեկրեցիայի համակարգի (T7SS) բաղադրիչներից. EssC-ը մեծ ինտեգրալ թաղանթային ATPase է, որը, ամենայն հավանականությամբ, ապահովում է սեկրեցիայի համակարգերը և ենթադրվում է, որ այն կազմում է տեղափոխման ալիքի մի մասը։ Մյուս սպիտակուցներն են EsaA, EssB, EssA, որոնք թաղանթային սպիտակուցներ են, որոնք գործում են EssC-ի կողքին՝ միջնորդելով սպիտակուցի սեկրեցումը։ Ճշգրիտ մեխանիզմը, թե ինչպես են ենթաշերտերը հասնում բջջի մակերեսին, անհայտ է, ինչպես նաև երեք թաղանթային սպիտակուցների փոխազդեցությունը միմյանց և EssC-ի հետ[64]։
T7 կախված էֆֆեկտոր սպիտակուցներ
EsaD-ը ԴՆԹ-ի էնդոնուկլեազային տոքսին է, որը արտազատված S. aureus-ի կողմից, և ապացուցված է, որ արգելակում է մրցակից S. aureus շտամի աճը in vitro[65]: EsaD-ն արտազատվում է շապերոն EsaE-ի հետ, որը կայունացնում է EsaD կառուցվածքը և EsaD-ն բերում է EssC-ի մոտ[64][65]՝ արտազատման համար։ EsaD արտադրող շտամները նաև համատեղ արտադրում են EsaG՝ ցիտոպլազմային հակատոքսին, որը պաշտպանում է արտադրող շտամը EsaD-ի թունավորությունից[65]։
TspA-ն ևս մեկ տոքսին է, որը միջնորդում է ներտեսակային մրցակցությանը։ Այն բակտերիոստատիկ տոքսին է, որն ունի թաղանթների ապաբևեռացման ակտիվություն, որը նպաստում է իր c-տերմինալ տիրույթին։ Tsai-ն տրանսմեմբրանային սպիտակուց է, որը իմունիտետ է հաղորդում TspA-ի արտադրող շտամին, ինչպես նաև հարձակման ենթարկված շտամներին։ TspA-ի c-տերմինալ տիրույթի գենետիկական փոփոխականություն կա, հետևաբար, թվում է, որ շտամները կարող են արտադրել տարբեր TspA տարբերակներ՝ մրցունակությունը բարձրացնելու համար[66]։
Տոքսինները, որոնք դեր են խաղում միջտեսակային մրցակցության մեջ, առավելություն են տալիս՝ խթանելով հաջող գաղութացումը պոլիմանրէային համայնքներում, ինչպիսիք են քիթ-կոկորդը և թոքերը՝ մրցակցելով ավելի փոքր շտամների հետ[66]։
Կան նաև T7 էֆեկտորային սպիտակուցներ, որոնք դեր են խաղում պաթոգենեզում, օրինակ՝ S. aureus-ի մուտացիոն ուսումնասիրությունները ցույց են տվել, որ EsxB-ն և EsxC-ն նպաստում են մկների թարախակույտի մոդելի մշտական վարակմանը[67]։
EsxX-ը ներգրավված է նեյտրոֆիլների լիզի մեջ, հետևաբար ներկայացվում է որպես նպաստող գործոն տիրոջ իմունային համակարգ ներխուժելու համար։ S. aureus-ում essX-ի ջնջումը հանգեցրել է նեյտրոֆիլների նկատմամբ դիմադրողականության զգալի նվազման և մկների մաշկի և արյան վարակման մոդելների վիրուլենտության նվազեցմանը[68]։
Ընդհանուր առմամբ, T7SS-ը և հայտնի արտազատվող էֆեկտորային սպիտակուցները պաթոգենեզի ռազմավարություն են՝ բարելավելով մրցակից S. aureus տեսակների դեմ դիմադրությունը, ինչպես նաև մեծացնում է վիրուլենտությունը՝ խուսափելով բնածին իմունային համակարգից և օպտիմալացնելով վարակները։
Փոքր ՌՆԹ-ների ցանկը, որոնք ներգրավված են S. aureus-ում բակտերիալ վիրուսայնության վերահսկման մեջ, աճում է։ Դրան կարող են նպաստել այնպիսի գործոններ, ինչպիսիք են կենսաթաղանթի ձևավորման ավելացումը նման փոքր ՌՆԹ-ների մակարդակների բարձրացման առկայության դեպքում[69]։ Օրինակ՝ RNAIII[70], SprD[71], SprC[72][73], RsaE[74], SprA1[75], SSR42[76], ArtR[77], SprX և Teg49[78]:
Տիրոջ նեյտրոֆիլները առաջացնում են ԴՆԹ-ի երկշղթա ճեղքեր S. aureus-ում՝ ռեակտիվ թթվածնի արտադրության միջոցով[79]։ Որպեսզի տիրոջ վարակումը հաջող լինի, S. aureus-ը պետք է վերապրի տիրոջ պաշտպանական միջոցների հետևանքով առաջացած նման վնասները։ Դրա կողմից կոդավորված RexAB երկսպիտակուցային կոմպլեքսը օգտագործվում է ԴՆԹ-ի կրկնակի շղթաների ճեղքերի ռեկոմբինացիոն վերանորոգման համար[79]։
Շատ ինֆորմացիոն ՌՆԹներ (mRNA-ներ) S. aureus-ում կրում են երեք հիմնական չթարգմանված շրջաններ (3'UTR) ավելի երկար, քան 100 նուկլեոտիդներ, որոնք կարող են պոտենցիալ կարգավորիչ գործառույթ ունենալ[80]։
icaR ինֆորմացիոն ՌՆԹ-ի հետագա հետազոտությունը (ինֆորմացիոն ՌՆԹ-ն, որը կոդավորում է բակտերիաների կենսաթաղանթի մատրիցայի հիմնական էքսպոլիսախարիդային միացության ռեպրեսորը) ցույց է տվել, որ 3'UTR-ը, որը կապվում է 5' UTR-ին, կարող է խանգարել թարգմանության մեկնարկի համալիրին և առաջացնել RNase III-ի համար կրկնակի շղթա ունեցող սուբստրատ։ Փոխազդեցությունը տեղի է ունենում UCCCCUG-ի մոտիվների միջև 3'UTR-ում և Shine-Dalagarno տարածաշրջանում 5'UTR-ում։ Մոտիվի ջնջումը հանգեցրեց IcaR ռեպրեսորների կուտակմանը և կենսաթաղանթի զարգացման արգելակմանը։ Կենսաթաղանթի ձևավորումը ստաֆիլոկոկային իմպլանտների վարակման հիմնական պատճառն է[81]։
Կենսաթաղանթները միկրոօրգանիզմների խմբեր են, որոնք կպչում են միմյանց և աճում խոնավ մակերեսների վրա[82]։ S. aureus-ի կենսաթաղանթը ներկառուցված է գլիկոկալիքս տիղմի շերտում և կարող է բաղկացած լինել տեյխոինաթթուներից, հյուրընկալող սպիտակուցներից, արտաբջջային ԴՆԹ-ից (eDNA) և բազմաշաքարային միջբջջային անտիգենից (PIA): S. aureus-ի ոչ բոլոր կենսաթաղանթերն են պարունակում PIA: S. aureus կենսաթաղանթերը կարևոր են հիվանդության պաթոգենեզում, քանի որ դրանք կարող են նպաստել հակաբիոտիկների դիմադրությանը և իմունային համակարգ ներխուժմանը[45]։ S. aureus կենսաթաղանթը բարձր դիմադրություն ունի հակաբիոտիկների բուժման և տիրոջ իմունային պատասխանի նկատմամբ[82]։ Սա բացատրելու վարկածներից մեկն այն է, որ կենսաթաղանթի մատրիցը պաշտպանում է ներկառուցված բջիջները՝ հանդես գալով որպես արգելք՝ կանխելու հակաբիոտիկների ներթափանցումը։ Այնուամենայնիվ, կենսաթաղանթի մատրիցը կազմված է բազմաթիվ ջրային ուղիներով, ուստի այս վարկածը գնալով ավելի քիչ հավանական է դառնում, բայց կենսաթաղանթի մատրիցը, հավանաբար, պարունակում է հակաբիոտիկները քայքայող ֆերմենտներ, ինչպիսիք են β-լակտամազները, որոնք կարող են կանխել հակաբիոտիկների ներթափանցումը[83]։ Մեկ այլ վարկածն այն է, որ կենսաթաղանթի մատրիցայի պայմանները նպաստում են կայուն բջիջների ձևավորմանը, որոնք խիստ հակաբիոտիկակայուն, քնած բակտերիաների բջիջներ են[45]։ S. aureus-ի կենսաթաղանթները նույնպես ունեն բարձր դիմադրություն տիրոջ իմունային պատասխանին։ Չնայած դիմադրության ճշգրիտ մեխանիզմը անհայտ է, S. aureus կենսաթաղանթերը աճում են տիրոջ իմունային համակարգի կողմից արտադրվող ցիտոկինների առկայության պայմաններում։ Ընդունող հակամարմիններն ավելի քիչ արդյունավետ են S. aureus կենսաթաղանթի համար՝ անտիգենի տարասեռ բաշխման պատճառով, որտեղ անտիգենը կարող է առկա լինել կենսաթաղանթի որոշ հատվածներում, բայց իսպառ բացակայել այլ հատվածներից[45]։
Կենսաթաղանթի զարգացման ուսումնասիրությունները ցույց են տվել, որ կապված են գեների արտահայտման փոփոխությունների հետ։ Կան հատուկ գեներ, որոնք որոշիչ նշանակություն ունեն կենսաֆիլմի աճի տարբեր փուլերում։ Այս գեներից երկուսը ներառում են rocD և gudB, որոնք կոդավորում են ֆերմենտի օրնիտին-օքսո-թթու տրանսամինազը և գլուտամատ դեհիդրոգենազը, որոնք կարևոր են ամինաթթուների նյութափոխանակության համար։ Ուսումնասիրությունները ցույց են տվել, որ կենսաթաղանթի զարգացումը հիմնված է ամինաթթուների վրա՝ գլուտամին և գլյուտամատ՝ նյութափոխանակության պատշաճ գործառույթների համար[84]։
Սպիտակուց A-ն խարսխված է ստաֆիլոկոկային պեպտիդոգլիկան պենտագլիկինի կամուրջների վրա (գլիցինի հինգ մնացորդներից բաղկացած շղթաներ) տրանսպեպտիդազ սորտազ A-ի միջոցով[85]։ Սպիտակուցը A-ն՝ IgG կապող սպիտակուցը, կապվում է հակամարմինի Fc շրջանին։ Իրականում, A սպիտակուցը կոդավորող գեների մուտացիայի հետ կապված ուսումնասիրությունները արյան մեջ գոյատևման միջոցով հանգեցրել են S. aureus-ի նվազման, ինչը հանգեցրել է ենթադրությունների, որ սպիտակուց A-ով պայմանավորված վիրուսային ուժը պահանջում է հակամարմինների Fc շրջանների կապում[86]։
Սպիտակուց A-ն տարբեր ռեկոմբինանտ ձևերով օգտագործվել է տասնամյակներ շարունակ հակամարմինների լայն տեսականի կապելու և մաքրելու համար իմունաաֆինիտային քրոմատագրման միջոցով։ Տրանսպեպտիդազները, ինչպիսիք են սորտազները, որոնք պատասխանատու են ստաֆիլոկոկային պեպտիդոգլիկանի վրա սպիտակուց A-ի նման գործոնների խարսխման համար, ուսումնասիրվում են նոր հակաբիոտիկներ մշակելու ակնկալիքով՝ MRSA վարակների թիրախավորման համար[87]։

Ոսկեգույն ստաֆիլոկոկի որոշ շտամներ կարող են արտադրել ստաֆիլոքսանտին՝ ոսկեգույն կարոտինոիդ պիգմենտ։ Այս պիգմենտը գործում է որպես վիրուսային գործոն՝ հիմնականում լինելով բակտերիալ հակաօքսիդանտ, որն օգնում է միկրոբին խուսափել ռեակտիվ թթվածնի տեսակներից, որոնք տիրոջ իմունային համակարգը օգտագործում է պաթոգեններին սպանելու համար[88][89]։
S. aureus-ի մուտանտ շտամները, որոնք ձևափոխված են ստաֆիլոքսանտինի բացակայության պատճառով, ավելի քիչ հավանական է, որ գոյատևեն օքսիդացնող քիմիական նյութով ինկուբացիայից, ինչպիսին է ջրածնի պերօքսիդը, քան պիգմենտային շտամները։ Մուտանտ գաղութները արագորեն սպանվում են, երբ ենթարկվում են մարդու նեյտրոֆիլներին, մինչդեռ պիգմենտավորված գաղութներից շատերը գոյատևում են[88]։ Մկների մոտ պիգմենտավորված շտամները վերքերի մեջ պատվաստվելիս առաջացնում են երկարատև թարախակույտ, մինչդեռ չպիգմենտացված շտամներով վարակված վերքերը արագ ապաքինվում են։
Այս թեստերը ցույց են տալիս, որ ստաֆիլոկոկի շտամներն օգտագործում են ստաֆիլոքսանտին որպես պաշտպանություն մարդու նորմալ իմունային համակարգի դեմ։ Ստաֆիլոքսանտինի արտադրությունը արգելակելու համար նախատեսված դեղամիջոցները կարող են թուլացնել բակտերիան և փոխել նրա զգայունությունը հակաբիոտիկների նկատմամբ[89]։ Փաստորեն, ստաֆիլոքսանտինի և մարդու խոլեստերինի կենսասինթեզի ուղիների նմանությունների պատճառով խոլեստերինի իջեցման թերապիայի համատեքստում մշակված դեղամիջոցը ցույց տվեց, որ արգելափակում է S. aureus-ի պիգմենտացիան և հիվանդության առաջընթացը մկների վարակման մոդելում[90]։

Կախված առկա վարակի տեսակից, համապատասխան նմուշ է ստացվում և ուղարկվում լաբորատորիա վերջնական նույնականացման համար՝ օգտագործելով կենսաքիմիական կամ ֆերմենտային թեստեր։ Սկզբում կատարվում է Գրամ բիծ՝ ուղղորդելու համար, որը պետք է ցույց տա տիպիկ գրամ դրական բակտերիաները՝ կոկիները, կլաստերներում։ Երկրորդ, առանձնացված գաղութը մշակվում է մանիտոլ աղի ագարի վրա, որը 7,5% NaCl-ով ընտրովի միջավայր է, որը թույլ է տալիս S. aureus-ին աճել՝ առաջացնելով դեղին գույնի գաղութներ մանիտոլի խմորման և հետագա միջավայրի pH-ի իջեցման արդյունքում[91][92]։
Ավելին, տեսակների մակարդակով տարբերակման համար կատարվում են կատալազը (դրական է ստաֆիլոկոկի բոլոր տեսակների համար), կոագուլազը (ֆիբրինի թրոմբի ձևավորում, դրական S. aureus-ի համար), ԴՆԹ-ազը (DNase ագարի մաքրման գոտի), լիպազ (դեղին գույն և ողողված հոտի հոտ)։ ֆոսֆատազի (վարդագույն գույն) թեստեր։ Ստաֆիլոկոկային սննդային թունավորման դեպքում ֆագերի տիպավորումը կարող է իրականացվել՝ պարզելու համար, թե արդյոք սննդից վերականգնված ստաֆիլոկոկները վարակի աղբյուր են եղել[93]։
Ախտորոշիչ մանրէաբանական լաբորատորիաները և տեղեկատու լաբորատորիաները առանցքային են S. aureus-ի բռնկումների և նոր շտամների հայտնաբերման համար։ Գենետիկական վերջին առաջընթացները հնարավորություն են տվել իրական ժամանակում S. aureus-ի կլինիկական առանձնացված գաղութների նույնականացման և բնութագրման հուսալի և արագ տեխնիկայի կիրառել։ Այս գործիքներն աջակցում են վարակի վերահսկման ռազմավարություններին՝ սահմանափակելու բակտերիաների տարածումը և ապահովելու հակաբիոտիկների համապատասխան օգտագործումը։ Քանակական PCR-ն ավելի ու ավելի է օգտագործվում վարակի բռնկումները բացահայտելու համար[94][95]։
S. aureus-ի զարգացումը և յուրաքանչյուր փոփոխված հակաբիոտիկին հարմարվելու նրա կարողությունը դիտարկելիս օգտագործվում են երկու հիմնական մեթոդ, որոնք հայտնի են որպես «շղթայական» կամ «հաջորդականության վրա հիմնված»։ Նկատի ունենալով այս երկու մեթոդները, այլ մեթոդներ, ինչպիսիք են բազմալոկուս հաջորդականության տիպավորումը (MLST), իմպուլսային դաշտային գելային էլեկտրոֆորեզը (PFGE), բակտերիոֆագի տիպավորումը, սպա լոկուսի մուտքագրումը և SCCmec տիպավորումը հաճախ ավելի շատ են իրականացվում, քան մյուսները[96][97]։ Այս մեթոդներով կարելի է որոշել, թե որտեղ են առաջացել MRSA-ի շտամները և որտեղ են դրանք ներկայումս[98]։
MLST-ի միջոցով մուտքագրման այս տեխնիկան օգտագործում է մի քանի գեների բեկորներ, որոնք հայտնի են որպես aroE, glpF, gmk, pta, tip և yqiL: Այս հաջորդականություններին այնուհետև տրվում է մի թիվ, որը տալիս է մի քանի թվերի շարան, որոնք ծառայում են որպես ալելային պրոֆիլ։ Թեև սա տարածված մեթոդ է, այս մեթոդի սահմանափակումը միկրոզանգվածի պահպանումն է, որը հայտնաբերում է նոր ալելային պրոֆիլները՝ դարձնելով այն ծախսատար և ժամանակատար փորձ[96]։
PFGE մեթոդը, որը դեռ շատ է օգտագործվում, սկսած 1980-ականներին իր առաջին հաջողությամբ, շարունակում է օգնել տարբերակել MRSA առանձնացված գաղութները[98]։ Դա անելու համար տեխնիկան օգտագործում է բազմաթիվ գելային էլեկտրոֆորեզ, ինչպես նաև լարման գրադիենտ՝ մոլեկուլների հստակ լուծաչափերը ցուցադրելու համար։ S. aureus-ի մասնիկներն այնուհետև անցնում են գելից ներքև՝ առաջացնելով հատուկ ժապավենային նախշեր, որոնք հետագայում համեմատվում են այլ առանձնացված գաղութների հետ՝ հարակից շտամները հայտնաբերելու հույսով։ Մեթոդի սահմանափակումները ներառում են գործնական դժվարություններ՝ կապված ժապավենի միատեսակ օրինաչափությունների և PFGE զգայունության հետ, որպես ամբողջություն։
Սպա լոկուսի մուտքագրումը համարվում է նաև հանրաճանաչ տեխնիկա, որն օգտագործում է մեկ տեղանոց գոտի S. aureus-ի պոլիմորֆ շրջանում՝ տարբերելու մուտացիաների ցանկացած ձև[98]։ Չնայած այս տեխնիկան հաճախ էժան է և քիչ ժամանակատար, մեծ է տարբերակող ուժը կորցնելու հնարավորությունը, ինչը դժվարացնում է MLST կլոնային կոմպլեքսների միջև տարբերակումը, ցույց է տալիս կարևոր սահմանափակում։
Զգայուն շտամների դեպքում S. aureus վարակի նախընտրելի բուժումը պենիցիլինն է։ Հակաբիոտիկ, որը ստացվում է Penicillium սնկային որոշ տեսակներից, պենիցիլինը արգելակում է պեպտիդոգլիկանի խաչաձև կապերի ձևավորումը, որոնք ապահովում են բակտերիաների բջջային պատի կոշտությունը և ամրությունը։ Պենիցիլինի չորս անդամներից բաղկացած β-լակտամ օղակը կապված է DD-տրանսպեպտիդազ ֆերմենտի հետ, ֆերմենտ, որը ֆունկցիոնալ ժամանակ կապում է պեպտիդոգլիկանի շղթաները, որոնք ձևավորում են բակտերիալ բջիջների պատերը։ β-լակտամի միացումը DD-տրանսպեպտիդազին արգելակում է ֆերմենտի ֆունկցիոնալությունը և այն այլևս չի կարող կատալիզացնել խաչաձեւ կապերի ձևավորումը։ Արդյունքում, բջջային պատի ձևավորումը և քայքայումը անհավասարակշռված են, ինչն էլ հանգեցնում է բջիջների մահվան։ Այնուամենայնիվ, շատ երկրներում պենիցիլինի դիմադրությունը չափազանց տարածված է (>90%), և առաջին գծի թերապիան ամենից հաճախ պենիցիլինազ կայուն β-լակտամ հակաբիոտիկն է (օրինակ՝ օքսացիլին կամ ֆլյուկլոքսացիլին, որոնք երկուսն էլ ունեն գործողության նույն մեխանիզմը։ որպես պենիցիլին) կամ վանկոմիցին, կախված տեղական դիմադրության ձևերից։ Գենտամիցինի հետ համակցված թերապիան կարող է օգտագործվել լուրջ վարակների, օրինակ՝ էնդոկարդիտի[99][100], բուժման համար, սակայն դրա օգտագործումը հակասական է երիկամների վնասման բարձր ռիսկի պատճառով[101]։ Բուժման տևողությունը կախված է վարակի վայրից և ծանրությունից։ Աջակցող ռիֆամպիցինը պատմականորեն օգտագործվել է S. aureus-ի բակտերեմիայի բուժման համար, սակայն պատահական վերահսկվող փորձարկումների ապացույցները ցույց են տվել, որ դա ընդհանուր օգուտ չի բերում ստանդարտ հակաբիոտիկ թերապիայի համեմատ[102]։
S. aureus-ում հակաբիոտիկ դիմադրությունը հազվադեպ էր, երբ պենիցիլինը առաջին անգամ ներդրվեց 1943 թվականին։ Իրոք, նախնական Պետրիի թասիկը, որի վրա Ալեքսանդր Ֆլեմինգը Լոնդոնի կայսերական քոլեջից դիտել էր Penicillium բորբոսի հակաբակտերիալ ակտիվությունը, աճեցնում էր S. aureus-ի կուլտուրան։ Մինչև 1950 թվականը հիվանդանոցային S. aureus մեկուսացված շտամների 40%-ը պենիցիլինի նկատմամբ կայուն էր, մինչև 1960 թվականը այն հասել էր 80%-ի[103]։
Մետիցիլինի նկատմամբ կայուն ոսկեգույն ստաֆիլոկոկը (MRSA, հաճախ արտասանվում է /ˈmɜːrsə/ կամ /ɛm ɑːr ɛs eɪ/), S. aureus-ի խիստ անհանգստացնող շտամներից մեկն է, որը կայուն է դարձել β-լակտամ հակաբիոտիկների մեծ մասի նկատմամբ։ Այդ իսկ պատճառով վանկոմիցինը` գլիկոպեպտիդային հակաբիոտիկ, սովորաբար օգտագործվում է MRSA-ի դեմ պայքարելու համար։ Վանկոմիցինը արգելակում է պեպտիդոգլիկանի սինթեզը, սակայն, ի տարբերություն β-լակտամ հակաբիոտիկների, գլիկոպեպտիդային հակաբիոտիկները թիրախավորում և կապում են բջջային պատի ամինաթթուներին՝ կանխելով պեպտիդոգլիկանի խաչաձև կապերի ձևավորումը։ MRSA շտամներն առավել հաճախ հայտնաբերվում են կապված այնպիսի հաստատությունների հետ, ինչպիսիք են հիվանդանոցները, բայց գնալով ավելի տարածված են դառնում համայնքի կողմից ձեռք բերված վարակների դեպքում։
Մաշկի մանր վարակները կարող են բուժվել եռակի հակաբիոտիկ քսուքով[104]։ Տեղական դեղամիջոցներից մեկը, որը նշանակվում է Մուպիրոսինն է՝ սպիտակուցի սինթեզի արգելակիչ, որը բնական ճանապարհով արտադրվում է Pseudomonas fluorescens-ի կողմից և հաջողություն է գրանցել S. aureus-ի ռնգային փոխանցման բուժման համար[45]։
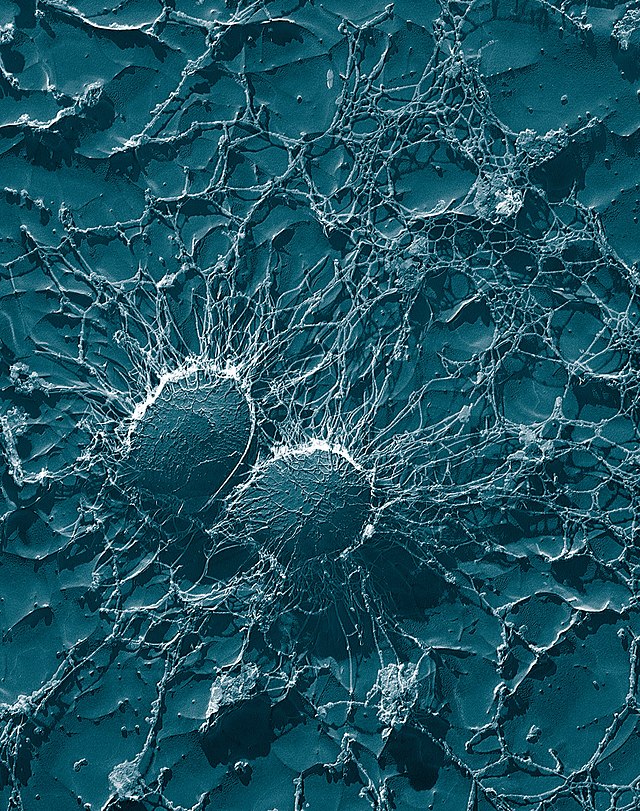
Պարզվել է, որ S. aureus-ը 2019 թվականին հակամանրէային դիմադրության հետ կապված մահերի երկրորդ առաջատար ախտահարիչն է[105]։
Պենիցիլինի նկատմամբ ստաֆիլոկոկային դիմադրությունը միջնորդվում է պենիցիլինազի (β-լակտամազի ձև) արտադրությամբ՝ ֆերմենտ, որը կտրում է պենիցիլինի մոլեկուլի β-լակտամ օղակը՝ դարձնելով հակաբիոտիկն անարդյունավետ։ Պենիցիլինազին դիմացկուն β-լակտամ հակաբիոտիկները, ինչպիսիք են մետիցիլինը, նաֆցիլինը, օքսացիլինը, կլոկսացիլինը, դիկլոքսացիլինը և ֆլուկլոքսացիլինը, կարող են դիմակայել ստաֆիլոկոկային պենիցիլինազի քայքայմանը։
մետիցիլինի նկատմամբ դիմադրողականությունը միջնորդվում է mec օպերոնի միջոցով, որը հանդիսանում է ստաֆիլոկոկային կասետային քրոմոսոմ mec-ի մի մասը (SCCmec): SCCmec-ը շարժական գենետիկ տարրերի ընտանիք է, որը հանդիսանում է բակտերիայի էվոլյուցիայի հիմնական շարժիչ ուժը[96]։ Դիմադրությունը շնորհվում է mecA գենով, որը կոդավորում է փոփոխված պենիցիլին կապող սպիտակուցը (PBP2a կամ PBP2'), որն ավելի ցածր կապ ունի β-լակտամներին (պենիցիլիններ, ցեֆալոսպորիններ և կարբապենեմներ)։ Սա թույլ է տալիս դիմադրողականություն ապահովել բոլոր β-լակտամ հակաբիոտիկների նկատմամբ և կանխում է դրանց կլինիկական օգտագործումը MRSA վարակների ժամանակ։ Ուսումնասիրությունները բացատրել են, որ այս շարժական գենետիկ տարրը ձեռք է բերվել տարբեր ընտանիքների կողմից առանձին գեների փոխանցման իրադարձությունների ժամանակ, ինչը ցույց է տալիս, որ գոյություն չունի MRSA-ի տարբեր շտամների ընդհանուր նախնի[106]։ Հետաքրքիր է, որ մի ուսումնասիրություն ենթադրում է, որ MRSA-ն զոհաբերում է վիրուլենտությունը, օրինակ՝ տոքսինների արտադրությունը և ինվազիվությունը՝ գոյատևելու և կենսաթաղանթներ ստեղծելու համար[107]։
Ամինոգլիկոզիդային հակաբիոտիկները, ինչպիսիք են կանամիցինը, գենտամիցինը, ստրեպտոմիցինը, ժամանակին արդյունավետ են եղել ստաֆիլոկոկային վարակների դեմ, քանի դեռ շտամները զարգացրել են մեխանիզմներ՝ արգելակելու ամինոգլիկոզիդների գործողությունը, որը տեղի է ունենում բակտերիալ 30S ենթամիավորի ռիբոսոմային ՌՆԹ-ի հետ պրոտոնացված ամինի և/կամ հիդրօքսիլային փոխազդեցությունների միջոցով[108]։ Ներկայումս և լայնորեն ընդունված են ամինոգլիկոզիդային դիմադրության մեխանիզմների երեք հիմնական տեսակներ. ամինոգլիկոզիդներ ձևափոխող ֆերմենտներ, ռիբոսոմային մուտացիաներ և դեղամիջոցի ակտիվ արտահոսք բակտերիայից։
Ամինոգլիկոզիդը փոփոխող ֆերմենտներն ապաակտիվացնում են ամինոգլիկոզիդը՝ կովալենտորեն միացնելով կա՛մ ֆոսֆատ, նուկլեոտիդ կա՛մ ացետիլ խումբ հակաբիոտիկի կա՛մ ամին, կա՛մ ալկոհոլային առանցքային ֆունկցիոնալ խմբին (կամ երկու խմբերին)։ Սա փոխում է լիցքը կամ խոչընդոտում է հակաբիոտիկի գործունեությունը՝ նվազեցնելով նրա ռիբոսոմային կապող ուժը։ S. aureus-ին ամենաշատը հատուկ ամինոգլիկոզիդը փոփոխող ֆերմենտը ամինոգլիկոզիդ ադենիլիլտրանսֆերազն է 4' IA (ANT(4')IA): Այս ֆերմենտը հայտնաբերվել է ռենտգենյան բյուրեղագրության միջոցով[109]։ Ֆերմենտը կարող է ադենիլային խումբ կցել բազմաթիվ ամինոգլիկոզիդների 4' հիդրօքսիլ խմբին, ներառյալ կամամիցինը և գենտամիցինը։
Գլիկոպեպտիդային դիմադրությունը միջնորդվում է vanA գենի ձեռքբերմամբ, որը ծագում է էնտերոկոկի պլազմիդի մեջ հայտնաբերված Tn1546 տրանսպոզոնից և ծածկագրում է ֆերմենտի համար, որն արտադրում է այլընտրանքային պեպտիդոգլիկան, որին վանկոմիցինը չի կապվում[110]։
Այսօր S. aureus-ը դարձել է դիմացկուն շատ հաճախ օգտագործվող հակաբիոտիկների նկատմամբ։ Մեծ Բրիտանիայում S. aureus-ի բոլոր առանձնացված գաղութների միայն 2%-ն է զգայուն պենիցիլինի նկատմամբ, մնացած աշխարհում ևս նման պատկեր կա։ β-լակտամազի նկատմամբ կայուն պենիցիլինները (մետիցիլին, օքսացիլին, կլոքսացիլին և ֆլյուկլոքսացիլին) մշակվել են պենիցիլինի նկատմամբ դիմացկուն S. aureus-ի բուժման համար և դեռ օգտագործվում են որպես առաջին գծի բուժում։ Մետիցիլինը այս դասի առաջին հակաբիոտիկն էր, որը կիրառվեց (այն ներդրվել է 1959 թվականին), բայց միայն երկու տարի անց Անգլիայում արձանագրվեց մետիցիլինի նկատմամբ կայուն Staphylococcus aureus-ի (MRSA) առաջին դեպքը[111]։
Չնայած դրան, MRSA-ն ընդհանուր առմամբ մնում էր անսովոր հայտնաբերում, նույնիսկ հիվանդանոցային պայմաններում, մինչև 1990-ականները, երբ MRSA-ի տարածվածությունը հիվանդանոցներում պայթեց, և այն այժմ էնդեմիա է[112]։ Այժմ, մետիցիլինի նկատմամբ դիմակայուն ոսկեգույն ստաֆիլոկոկըը (MRSA) ոչ միայն մարդու ախտահարիչ է, որն առաջացնում է մի շարք վարակներ, ինչպիսիք են մաշկի և փափուկ հյուսվածքների վարակը (SSTI), թոքաբորբը և սեպսիսը, այլև այն կարող է առաջացնել կենդանիների հիվանդություն, որը հայտնի է որպես անասունների հետ ասոցացված MRSA (LA-MRSA)[113]:
MRSA վարակները ինչպես հիվանդանոցում, այնպես էլ համայնքային պայմաններում սովորաբար բուժվում են ոչ β-լակտամային հակաբիոտիկներով, ինչպիսիք են կլինդամիցինը (լինկոզամին) և կո-տրիմոքսազոլը (որը նաև հայտնի է որպես տրիմետոպրիմ/սուլֆամետոքսազոլ)։ Այս հակաբիոտիկների նկատմամբ դիմադրողականությունը նաև հանգեցրել է նոր, լայն սպեկտրի հակագրամ դրական հակաբիոտիկների օգտագործմանը, ինչպիսին է լինեզոլիդը, քանի որ այն հասանելի է որպես բերանային դեղամիջոց։ MRSA-ով պայմանավորված լուրջ ինվազիվ վարակների առաջին գծի բուժումը ներկայումս գլիկոպեպտիդային հակաբիոտիկներն են (վանկոմիցին և տեյկոպլանին)։ Այս հակաբիոտիկների հետ կապված մի շարք խնդիրներ են առաջանում, ինչպիսիք են ներերակային ներարկումների անհրաժեշտությունը (բերանային պատրաստուկներ չկան), թունավորությունը և արյան անալիզների միջոցով դեղերի մակարդակը կանոնավոր վերահսկելու անհրաժեշտությունը։ Բացի այդ, գլիկոպեպտիդային հակաբիոտիկները այնքան էլ լավ չեն ներթափանցում վարակված հյուսվածքների մեջ (սա հատկապես մտահոգիչ է գլխուղեղի և մենինգների վարակների և էնդոկարդիտի դեպքում)։ Գլիկոպեպտիդները չպետք է օգտագործվեն մետիցիլինի նկատմամբ զգայուն S. aureus (MSSA) բուժման համար, քանի որ արդյունքները ցածր են։

Պենիցիլինների նկատմամբ դիմադրողականության բարձր մակարդակի և վանկոմիցինի նկատմամբ MRSA-ի կողմից դիմադրողականություն զարգացնելու հնարավորության պատճառով ԱՄՆ Հիվանդությունների վերահսկման և կանխարգելման կենտրոնը հրապարակել է վանկոմիցինի պատշաճ օգտագործման ուղեցույցներ։ Այն իրավիճակներում, երբ հայտնի է, որ MRSA վարակների հաճախականությունը բարձր է, ներկա բժիշկը կարող է ընտրել գլիկոպեպտիդային հակաբիոտիկ օգտագործել, մինչև վարակիչ օրգանիզմի ինքնությունը հայտնի չդառնա։ Այն բանից հետո, երբ հաստատվել է, որ վարակը պայմանավորված է S. aureus-ի մետիցիլինի նկատմամբ զգայուն շտամով, բուժումը կարող է փոխվել ֆլուկլոքսասիլինի կամ նույնիսկ պենիցիլինի, ըստ անհրաժեշտության։
Վանկոմիցինի նկատմամբ դիմացկուն S. aureus-ը (VRSA) այս բակտերայի շտամ է, որը կայուն է դարձել գլիկոպեպտիդների նկատմամբ։ Վանկոմիցին-միջանկյալ S. aureus-ի (VISA) առաջին դեպքը գրանցվել է Ճապոնիայում 1996 թվականին[114]; սակայն S. aureus-ի գլիկոպեպտիդ հակաբիոտիկների նկատմամբ իրոք դիմացկուն շտամի առաջին դեպքը գրանցվել է միայն 2002 թվականին[115]։ 2005 թվականի դրությամբ ԱՄՆ-ում գրանցվել է VRSA վարակի երեք դեպք։ Առնվազն մասամբ S. aureus-ի հակամանրէային դիմադրությունը կարելի է բացատրել նրա հարմարվելու ունակությամբ։ Ազդանշանի փոխանցման բազմաթիվ երկբաղադրիչ ուղիներն օգնում են S. aureus-ին արտահայտել գեներ, որոնք անհրաժեշտ են հակամանրէային սթրեսի պայմաններում գոյատևելու համար[116]։
Տարբեր մեխանիզմների շարքում, որոնք MRSA-ն ձեռք է բերում հակաբիոտիկների դիմադրությունից խուսափելու համար (օրինակ՝ դեղերի ապաակտիվացում, թիրախի փոփոխություն, թափանցելիության նվազում) կա նաև արտահոսքի պոմպերի գերարտահայտումը։ Արտահոսքի պոմպերը մեմբրանի մեջ ինտեգրված սպիտակուցներ են, որոնք ֆիզիոլոգիապես անհրաժեշտ են բջիջում՝ քսենոբիոտիկ միացությունների արտահանման համար։ Նրանք բաժանված են վեց ընտանիքի, որոնցից յուրաքանչյուրն ունի տարբեր կառուցվածք, գործառույթ և էներգիայի փոխադրում։ S. Aureus-ի հիմնական արտահոսքի պոմպերն են MFS-ը (Major Facilitator Superfamily), որը ներառում է MdeA պոմպը, ինչպես նաև NorA պոմպը և MATE-ը (Multidrug and Toxin Extrusion), որին պատկանում է MepA պոմպը։ Տրանսպորտի համար այս ընտանիքները օգտագործում են էլեկտրաքիմիական պոտենցիալ և իոնների կոնցենտրացիայի գրադիենտ, մինչդեռ ԱԵՖ կապող կասետների (ABC) ընտանիքն իր էներգիան ստանում է ԱԵՖ-ի հիդրոլիզից։
Այս պոմպերը գերարտահայտվում են MDR S. aureus-ով (Multidrug resistant S. aureus) և արդյունքը հակաբիոտիկի չափից դուրս արտանետում է բջջից դուրս, ինչն անարդյունավետ է դարձնում նրա գործողությունը։ Արտահոսքի պոմպերը նույնպես զգալիորեն նպաստում են անթափանց կենսաթաղանթերի զարգացմանը։
Ուղղակիորեն փոփոխելով արտահոսքի պոմպերի ակտիվությունը կամ նվազեցնելով դրանց արտահայտվածությունը, հնարավոր է, որ հավանական լինի փոփոխել դիմացկուն ֆենոտիպը և վերականգնել առկա հակաբիոտիկների արդյունավետությունը[117]։
ԱՄՆ-ի բնակչության մոտ 33%-ը S. aureus-ի կրողներ են, իսկ մոտ 2%-ը՝ MRSA[118]: Նույնիսկ առողջապահական ծառայություններ մատուցողները կարող են լինել MRSA գաղութարարներ[119][120]։
S. aureus-ի կրելիությունը հիվանդանոցային վարակի (նաև կոչվում է ներհիվանդանոցային) և համայնքից ձեռք բերված MRSA-ի կարևոր աղբյուր է։ Չնայած S. aureus-ը կարող է առկա լինել տիրոջ մաշկի վրա, նրա փոխադրման մեծ մասն անցնում է ռնգային անցուղիների առաջային նազերով[2] և հետագայում կարող է առկա լինել ականջներում[121]։ Ռնգային անցուղիների՝ S. aureus-ը պահելու ունակությունը պայմանավորված է տիրոջ թուլացած կամ թերի իմունիտետի և բակտերիայի՝ տիրոջ բնածին իմունիտետից խուսափելու ունակության համակցությամբ[122]։ Ստաֆիլոկոկային վարակների առաջացման մեջ ներգրավված է նաև ռնգային փոխադրումը[123]։
S. aureus-ի (ներառյալ MRSA) տարածումը հիմնականում տեղի է ունենում մարդուց մարդ շփման միջոցով, չնայած վերջերս որոշ անասնաբույժներ հայտնաբերել են, որ վարակը կարող է տարածվել ընտանի կենդանիների միջոցով[124], և շրջակա միջավայրի աղտոտումը ունի համեմատաբար ավելի անկարևոր դեր[125]։ Հետևաբար, ձեռքերի լվացման հիմնական տեխնիկայի վրա շեշտադրումը արդյունավետ է դրա փոխանցումը կանխելու համար։ Անձնակազմի կողմից մեկանգամյա օգտագործման գոգնոցների և ձեռնոցների օգտագործումը նվազեցնում է մաշկից մաշկ շփումը, ուստի ավելի է նվազեցնում փոխանցման ռիսկը։
Վերջերս ամբողջ ԱՄՆ-ի հիվանդանոցներում գրանցվել են S. aureus-ի բազմաթիվ դեպքեր։ Հարուցիչի փոխանցումը հեշտացվում է բժշկական հաստատություններում, որտեղ բուժաշխատողների հիգիենան անբավարար է։ Այն աներևակայելի դիմացկուն բակտերիա է, ինչպես ցույց է տրվել մի ուսումնասիրության մեջ, որտեղ այն գոյատևել է պոլիէսթերի վրա մոտ երեք ամսից[126]. պոլիէսթերը հիվանդանոցի վարագույրների մեջ օգտագործվող հիմնական նյութն է։
Բակտերիաները հայտնվում են են բուժաշխատողների ձեռքերին առողջ թվացող հիվանդից, որը կրում է S. aureus-ի բարորակ կամ համընդհանուր շտամ, այնուհետև փոխանցել այն հաջորդ բուժվող հիվանդին։ Բակտերիաների ներթափանցումը արյան մեջ կարող է հանգեցնել տարբեր բարդությունների, այդ թվում՝ էնդոկարդիտի, մենինգիտի և, եթե այն տարածված է, սեպսիս։
Էթանոլն արդյունավետ տեղային ախտահանիչ է MRSA-ի դեմ։ Չորրորդական ամոնիումը կարող է օգտագործվել էթանոլի հետ միասին՝ ախտահանման տևողությունը մեծացնելու համար։ Ներհիվանդանոցային վարակների կանխարգելումը ներառում է սովորական և վերջնական մաքրում։ CO2-ի համակարգերում չայրվող ալկոհոլային գոլորշները ունեն առավելություն, քանի որ դրանք չեն քայաքում բժշկական միջավայրում օգտագործվող մետաղները կամ պլաստմասսաները և չեն նպաստում հակաբակտերիալ դիմադրությանը։
Սեռկան շփումը համարվում է MRSA-ի գաղութացման և փոխանցման կարևոր և նախկինում չճանաչված միջոց[127]։
S. aureus-ը ոչնչանում է 78 °C-ում է մեկ րոպեում և 64 °C-ում՝ տաս րոպեում, բայց այն կայուն է սառեցման դեմ[128][129]։
Ոսկեգույ Ստաֆիլոկոկի մի շարք շտամներ բավականին մեծ կայունություն ունեն քլորային ախտահանման նկատմամբ[130][131]։
Մուպիրոսինի քսուքի օգտագործումը կարող է նվազեցնել S. aureus-ի քթային փոխադրման հետևանքով վարակվածության մակարդակը[132]։ Քիչ ապացույցներ կան, որ քթի ախտահանումը հակաբիոտիկների կամ հակասեպտիկ միջոցների օգտագործմամբ կարող է նվազեցնել վիրահատական տեղամասի S. aureus-ով վարակների մակարդակը[133]։
| Յուրաքանչյուր ոլորտում ամենատարածված բակտերաները | |
|---|---|
| Սննդի արդյունաբերություն | Vibrio parahaemolyticus, S. aureus, Bacillus cereus |
| Բժշկություն | Escherichia coli, S. aureus, Pseudomonas aeruginosa[134] |
2021 թվականի դրությամբ S. aureus-ի դեմ որևէ պատվաստանյութ գոյություն չունի։ Վաղ կլինիկական փորձարկումներ են իրականացվել մի քանի պատվաստանյութերի թեկնածուների համար, ինչպիսիք են Նաբիի StaphVax և PentaStaph, Ինթերսելի / Մերքսի V710, VRi's SA75 և այլն[135]։
Թեև այս պատվաստանյութերի թեկնածուներից ոմանք ցուցաբերել են իմունային ռեակցիա, մյուսները խորացրել են S. aureus-ի բորբոքումը։ Մինչ օրս այս թեկնածուներից ոչ մեկը պաշտպանություն չի ապահովում S. aureus վարակի դեմ[136]։ Ինթերսելի V710 պատվաստանյութի առաջին տարբերակը դադարեցվել է II/III փուլի ընթացքում այն բանից հետո, երբ նկատվել է ավելի բարձր մահացություն և հիվանդացություն S. aureus վարակով հիվանդների շրջանում[137]։
Նաբիի բարելավված S. aureus-ի պատվաստանյութերի թեկնածու PentaStaph-ը վաճառվել է 2011 թվականին GlaxoSmithKline Biologicals S.A.-ում[138]։ PentaStaph-ի այժմյան կարգավիճակը պարզ չէ։ Ըստ Առողջապահության համաշխարհային կազմակերպության փաստաթղթի՝ PentaStaph-ը ձախողել է փորձաշրջանի III փուլը[139]։
2010 թվականին ԳլաքսոԱմիթԿլայնը սկսեց 1-ին փուլի կույր ուսումնասիրությունը՝ գնահատելու իր GSK2392103A պատվաստանյութը։ 2016 թվականի դրությամբ, այս պատվաստանյութը այլևս ակտիվորեն չի մշակվում[140]։
2014 թվականի փետրվարին Պֆայզերի ոսկեգույն ստակիլակոկի դեմ չորս-անտիգենային պատվաստանյութ SA4Ag-ին ԱՄՆ-ի սննդի և դեղորայքի վարչությունից շնորհվել է արագ արտադրման (fast track) թույլտվություն[141]։ 2015 թվականին Պֆայզերըը սկսել է SA4Ag պատվաստանյութի 2b փուլի փորձարկումը։ 2017 թվականի փետրվարին հրապարակված 1-ին փուլի արդյունքները ցույց են տվել SA4Ag-ի շատ ամուր և անվտանգ իմունոգենություն[142]։ Պատվաստանյութը ենթարկվել է կլինիկական փորձարկման մինչև 2019 թվականի հունիսը, որի արդյունքները հրապարակվել են 2020 թվականի սեպտեմբերին, որոնք չեն ցույց տվել վիրահատությունից հետո արյան հոսքի հետվիրահատական վարակի զգալի նվազում։
2015-ին Նովարտիս Պատվաստանյութեր և Դիագնոստիկան, Նովարտիսի նախկին ստորաբաժանումը, այժմյան ԳլաքսոՍմիթԿլայնի մաս, հրապարակեց իրենց չորս բաղադրիչ ոսկեգույն ստաֆիլոկոկի պատվաստանյութի՝ 4C-staph-ի խոստումնալից նախակլինիկական արդյունքները[143]։
S. aureus-ի մի շարք ստանդարտ շտամներ (այլ անվանմամբ «կուլտուրաներ») օգտագործվում են հետազոտությունների ու լաբորատոր փորձաքննությունների համար, ինչպիսիք են՝
| Անուն | NCTC | ATCC | Ստեղծման տարի | Նշանակություն |
|---|---|---|---|---|
| Oxford H | 6571 | 9144 | 1943 | Պենիցիլինի կարողության փորձարկման ստանդարտ շտամ, որով ի սկզբանե սահմանվել է պենիցիլինի միավորը[144][145] |
| Rosenbach | 12973 | 29213 | 1884 | EUCAST հակամանրէային դիմադրության փորձերի ստանդարտ շտամ[146] |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.