Tirozin
From Wikipedia, the free encyclopedia
A tirozin (rövidítve Tyr vagy Y)[1] vagy 4-hidroxi-fenilalanin a sejtek által a fehérjék szintetizálásához használt 20 aminosav egyike. A genetikai kódban az UAC és UAU bázishármasok kódolják. Poláris oldalláncú nem esszenciális aminosav. Neve a sajtot jelentő görög türosz szóból származik,[2] mivel 1846-ban Justus von Liebig német kémikus a sajtból származó kazein nevű fehérjében fedezte fel elsőként.[3][4] Oldalláncként vagy funkciós csoportként elnevezése tirozil.
| Tirozin | |||
 Az l-izomer szerkezeti képlete | |||
 Az ikerionos l-izomer pálcikamodellje | |||
| |||
| |||
| IUPAC-név | (S)-tirozin | ||
| Más nevek | l-2-amino-3-(4-hidroxifenil)propánsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 60-18-4 | ||
| PubChem | 1153 | ||
| ChemSpider | 5833 | ||
| EINECS-szám | 200-460-4 | ||
| DrugBank | DB03839 | ||
| KEGG | D00022 | ||
| ChEBI | 58315 | ||
| SMILES | N[C@@H](Cc1ccc(O)cc1)C(O)=O | ||
| InChIKey | OUYCCCASQSFEME-QMMMGPOBSA-N | ||
| Beilstein | 392441 | ||
| Gmelin | 27744 | ||
| UNII | 42HK56048U | ||
| ChEMBL | 925 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C9H11NO3 | ||
| Moláris tömeg | 181,19 g/mol | ||
| Veszélyek | |||
| NFPA 704 | |||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Funkciói
Azon kívül, hogy proteinogén aminosav, a tirozin speciális szereppel rendelkezik fenol funkciós csoportja miatt. A sejtkommunikációs folyamatokban részt vevő fehérjék része. A fehérjekinázok (receptor-tirozinkinázok) által szállított foszfátcsoportokat fogad. A hidroxilcsoport foszforilációja megváltoztatja a fehérje aktivitását.
A tirozin fontos a fotoszintézisben. A kloroplasztiszokban (II. fotorendszer) az oxidált klorofill redukciójában vesz részt elektrondonorként. E folyamatban a fenol OH-csoportja deprotonálódik, ezt a II. fotorendszer redukálja 4 mangáncsoporttal
Tirozinforrások
A tirozin, melyet a szervezet fenilalaninból is előállíthat, számos magas fehérjetartalmú ételben megtalálható, például csirke-, pulykahúsban, halban, mogyoróban, mandulában, avokádóban, tejben, sajtban, joghurtban, túróban, Phaseolus lunatusban, tökmagban, szezámmagban, banánban és szójában.[5]
Bioszintézise
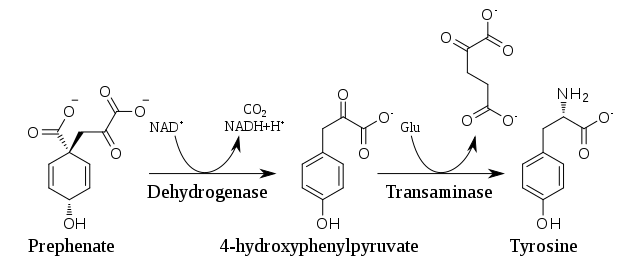
A növényekben és a mikroorganizmusok többségében a tirozin prefenáton keresztül termelődik, mely a sikimisav-útvonal köztiterméke. A prefenát oxidatív dekarboxilálása során – a hidroxilcsoport retenciójával – p-hidroxifenilpiruvát keletkezik, melyből transzaminálással – melyhez nitrogénforrásként glutamát szolgál – tirozin és α-ketoglutarát jön létre.
Az emlősök a tirozint az esszenciális aminosav fenil-alaninból (phe) szintetizálják, utóbbit a táplálékkal veszik fel. A phe–tyr átalakulást a monooxigenázok közé tartozó fenilalanin-hidroxiláz enzim katalizálja. Az enzim a fenil-alanin hat szénatomos aromás gyűrűjének végére történő hidroxiladdíciót katalizálja.
Metabolizmusa

Foszforiláció és szulfáció
Egyes helyeken a tirozint a tirozinkinázok foszforilálhatják. E foszforilált aminosav a foszfotirozin. A tirozinfoszforiláció fontos lépés a jeltranszdukcióban és az enzimaktivitás szabályzásában. A foszfotirozin adott antitestekkel észlelhető. A tirozin módosítható szulfátcsoporttal is (tirozinszulfáció).[6] Ezt a tirozilprotein-szulfotranszferáz (TPST) katalizálja. A foszfotirozin-antitestekhez hasonlóan ismertek szulfotirozint észlelő antitestek is.[7]
Neurotranszmitterek és hormonok prekurzora
A dopaminerg sejtekben a tirozint levodopává alakítja a tirozin-hidroxiláz (TH). A TH a dopamin neurotranszmitter szintézisének sebességmeghatározó enzimje. A dopamin ezután noradrenalinná és adrenalinná alakulhat.
A trijódtironin (T3) és tiroxin (T4) pajzsmirigyhormonok is tirozinszármazékok.
Alkaloidok prekurzora
A Papaver somniferum (kerti mák) váladéka a tirozint morfinná alakítja, ennek útvonalát sikerült 14C-gyel jelölt tirozin felhasználásával meghatározni az in vivo szintézis nyomonkövetéséhez.[8] A tirozin-ammónia-liáz (TAL) a természetes fenol-bioszintézisben résztvevő enzim. Ez a l-tirozint p-kumarinsavvá alakítja. Ezenkívül a tirozin a melanin prekurzora is, valamint a tirozin vagy prekurzora, a fenilalanin szükséges a koenzim Q10 benzokinonszerkezetének létrehozásához is.[9][10]
A meszkalintermelő kaktuszok tirozinból meszkalint állítanak elő annak injekciója után.[11]
Bomlása
Fordítás
Ez a szócikk részben vagy egészben a Tyrosine című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Hivatkozások
További olvasnivalók
Wikiwand - on
Seamless Wikipedia browsing. On steroids.



