Bakteriofág
baktériumokat fertőzni képes vírusok From Wikipedia, the free encyclopedia
Bakteriofágnak (a 'bacteria' és a görög φᾰγεῖν phagein „enni” szavakból) nevezzük a baktériumokat fertőzni képes vírusokat. Gyakran röviden csak fágként említik őket.
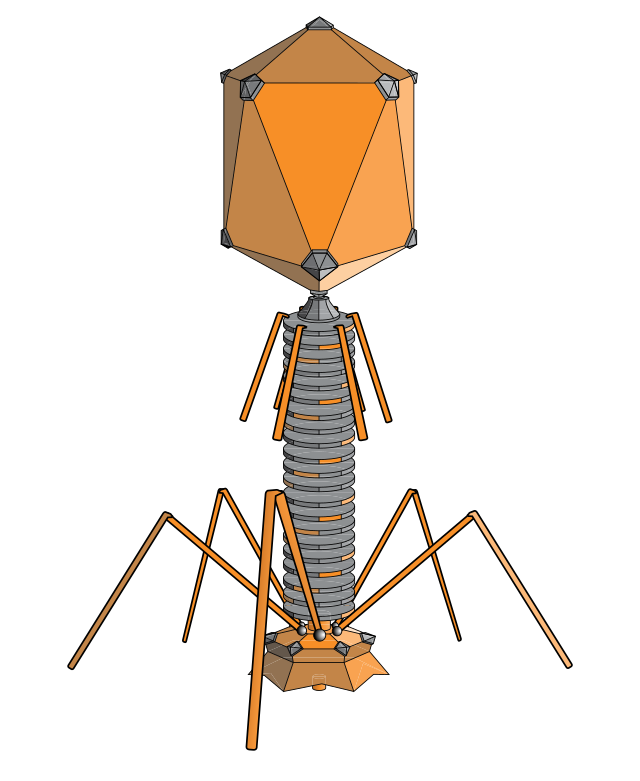
A tipikus bakteriofág egy külső, fehérjéből álló kapszidburokból, és a benne lévő örökítőanyagból áll. A genomot alkothatja RNS és DNS is – különféle formákban. A bakteriofágok sokkal kisebbek a gazdaszervezet baktériumoknál.
Becslések szerint a fágok a legszéleskörűbben elterjedt, legváltozatosabb szervezetek a földi bioszférában.[1][2][3] A mindenütt jelen lévő fágok megtalálhatók a bakteriális gazdaszervezetek által benépesített minden élőhelyen; a talajban, az állatok bélrendszerében stb. Igen nagy sűrűségben fordulnak elő a tengerben, ahol akár 9·108 virion található a felszíni baktériumszőnyeg minden milliliterében,[4] és a tengeri baktériumok akár 70%-a is fágokkal fertőzött lehet.[5]
Bár 1915-ös felfedezésük után még sokáig (1939-ig) láthatatlanok és rejtélyesek maradtak, gyógyászati felhasználásuk ötlete már a tízes évek végétől kezdve jelen volt. Több mint 60 éven keresztül használták őket az antibiotikumokkal történő gyógyítás alternatívájaként a Szovjetunióban és Kelet-Európában.[6] A fágterápia a baktériumok multirezisztens törzseivel szemben, mely utóbbi egyre komolyabb problémát jelent a sztenderd gyógyászatban és hosszú távon többek közt világméretű, tömegpusztító járványok kiújulásával fenyeget, hatásos és számba veendő terápiás eszköznek bizonyulhat.[7]
Osztályozásuk
A farokkal és kettős szálú DNS-sel rendelkező fágok (Caudovirales) adják az irodalomban megjelenő fágok mintegy 95%-át, és valószínűleg a bolygó fágainak többségét ezek adják.[3] A bioszférában azonban másfajta fágok is bőségesen előfordulnak, különböző virionokkal, genommal, életmóddal. A genomot alkothatja akár ssRNS, dsRNS, ssDNS vagy dsDNS is (az 'ss-' és 'ds-' prefixumok az egy- (single-), illetve kétszálúságra (double) utalnak), körkörös vagy lineáris elrendezésben. A fágok rendszerezésével az International Committee on Taxonomy of Viruses (ICTV) foglalkozik; a rendszerezés alapja a morfológia és a nukleinsav típusa.
| Rend | Család | Morfológia | Nukleinsav | Példa |
|---|---|---|---|---|
| Caudovirales | Myoviridae | Burok nélküli, összhúzékony farok | Lineáris dsDNS | T4 fág |
| Siphoviridae | Burok nélküli; hosszú, nem-összhúzékony farok | Lineáris dsDNS | λ fág | |
| Podoviridae | Burok nélküli; rövid, nem-összhúzékony farok | Lineáris dsDNS | T7 fág | |
| Rendbe nem sorolt | Tectiviridae | Burok nélküli, izometrikus | Lineáris dsDNS | |
| Corticoviridae | Burok nélküli, izometrikus | Körkörös dsDNS | ||
| Lipothrixviridae | Burokkal rendelkező, pálca alakú | Lineáris dsDNS | ||
| Plasmaviridae | Burokkal rendelkező, pleomorf (változatos alakú) | Körkörös dsDNS | ||
| Rudiviridae | Burok nélküli, pálca alakú | Lineáris dsDNS | ||
| Fuselloviridae | Burok nélküli, citrom alakú | Körkörös dsDNS | ||
| Inoviridae | Burok nélküli, fonalas | Körkörös ssDNS | ||
| Microviridae | Burok nélküli, izometrikus | Körkörös ssDNS | Phi X 174 | |
| Leviviridae | Burok nélküli, izometrikus | Lineáris ssRNS | ||
| Cystoviridae | Burokkal rendelkező, gömb alakú | Szegmentált dsRNS |
A bakteriofágia kutatásának története
A bakteriofágia felfedezése
Előzmények
Már az ókorban feljegyezték egyes folyóvizekről, hogy fertőző betegségeket (pl. a leprát) gyógyítanak. 1896-ban E. H. Hankin úgy találta, hogy az indiai Gangesz és Jamuna folyók vizében olyan anyag van, ami antibakteriális hatást fejt ki a kolerával szemben, és átjut a finom porcelánszűrőn.[8] Ny. F. Gamaleja, az odesszai Bakteriológiai Intézet igazgatója 1898-ban felfedezte, hogy a lépfene kórokozója (az anthrax-bacilus) bizonyos esetekben rendellenes, részlegesen elhalt telepeket fejleszt, és az ilyen tenyészetekből származó anyagmintákkal a még egészséges tenyészetek is megfertőzhetőek. A rendellenességet okozó anyagot bacteriolysinnnek („baktérium-feloldó”) nevezte el,[9] de nem feltételezte, hogy egy baktériumokon élősködő kórokozó is lehet (ekkoriban a jelenséget inkább a sejtek önfeloldásának, autolízisnek gondolták).
Az 1910-es évek közepétől kezdve sorra írták le a laboratóriumokban dolgozó kutatók az olyan megfigyeléseket, miszerint baktériumtenyészetekben részben spontán (észlelhető külső behatás nélkül), részben bizonyos anyagokkal megfertőzve, a telepek részleges (vagy teljes) elpusztulása tapasztalható, és a hatás az ilyen telepekből készült szűrlettel egészséges telepekre is átvihető. A jelenség, a transzmisszibilis bakteriolízis („átvihető/átadatható baktériumfeloldás”) rendkívül változatos magyarázatai között a baktériumokon élősködő, mikroszkóppal nem látható (szubmikroszkopikus, más néven ultramikroszkopikus) kórokozók is felmerültek.
A Twort-jelenség

Frederick W. Twort brit bakteriológusnak, a londoni Brown Institution felügyelőjének, miután 1910 környékén sikerült olyan, addig tenyészthetetlennek hitt baktériumokat, mint a leprát vagy a paratuberkulózist okozókat, táptalajon való szaporodásra bírnia (ami mintegy előfeltétele egy baktérium komoly tanulmányozásának), és ezzel a számon tartott bakteriológusok közé került, figyelme az ekkoriban még csak kevéssé ismert kórokozók, a vírusok felé fordult: ezek táptalajon való szaporítását akarta elérni. Számtalan táptalajt és fertőző-anyagot kipróbált, de baktériumszűrőn áthatolni képes virális kórokozók szaporításának - mai tudásunk szerint lehetetlen - feladatát sikeresen végrehajtani természetesen nem tudta. Végül egy olcsón és egyszerűen előállítható oltóanyag, a himlőnyirok mégis új felfedezéshez juttatta. E glicerinnel konzervált tehén-nyirokból álló pép a himlővírusok közé tartozó, de általában csak ártalmatlan, enyhe betegséget okozó Vaccinia vírust tartalmazta, amelyet Twort szaporítani akart,[10] és – minthogy az anyagot élő tehenekben tenyésztve állították elő – gyakran a Staphylococcus baktériumok különféle fajokba tartozó egyedei is előfordultak benne.[11][12]
Twort az agaros táptalajt tartalmazó, (valószínűleg rosszul megszűrt, esetleg szándékosan szűretlen) himlőnyirokkal beoltott csészékben a várt Vaccinia-telepek helyett eleinte csak néhány elburjánzó, a Staphylococcusok közé tartozó mikrokokkusz-telepet talált. Hamarosan mégis csak szokatlan és ismeretlen eredetű jelenséget figyelhetett meg: üvegszerűen átlátszóvá váló területek jelentek meg a baktériumtelepek szélén, melyek sokszor az egész telepet „felfalták”. Kevés sikerrel tudta csak továbbtenyészteni az ilyen részekből vett mintákat: a telepek vagy ki sem fejlődtek, vagy hamarosan az az anyatelepekéhez hasonló üvegszerű elváltozás, majd elhalás jelent meg rajtuk. Twort rájött, hogy ezek az átlátszóvá vált részek csak halott baktériumokat tartalmazhatnak, és a mikroszkópos vizsgálatok – amelyek csak élettelennek tűnő szemcsés törmeléket találtak a baktériumok helyén – is ezt igazolták. A himlőnyirokban tehát olyan tényezőnek kell hatnia, ami a baktériumokat elpusztítja. Ugyanilyen meglepő felfedezése volt, hogy az „üvegszerű elváltozás” bizonyos feltételek mellett a fertőzött telepekről egészségesekre volt átvihető: az elváltozás transzmisszibilis volt, mintha csak fertőző lenne.[12][13]
1915-ben – ez a bakteriofág-kutatás kezdetének hagyományosan „ünnepelt” kezdőéve – egy szaklapban közzétette tapasztalatait.[14] A cikkben legalább öt feltevést is megfogalmazott a sejtpusztulás okairól, s egyben a rejtélyes átlátszó anyag mibenlétéről, utóbbi lehet:
- a baktériumok életciklusának egy fázisa, amelyben a sejtek ultrafiltrálható formát vesznek fel, és más sejtekkel találkozva azokat is erre serkentik[12];
- a baktériumok által kibocsátott, valamilyen módon önállósult és szaporodóképes, amorf protoplazma[11] ;
- a baktériumok által termelt enzim; amely képes a felhalmozódásra vagy sokszorozódásra[11][15];
- egy ultra-mikroszkopikus vírus, ami baktériumokban tenyészik;[11]
- feltételezte továbbá, hogy maga az üvegszerű anyag a fertőző ágens, amelyet a mikrokokkuszok maguk termelnek, és felvetette: minthogy fertőzőképes és halálos hatású is lehet, megjelenése szinte már akut fertőzésés megbetegedésnek is tekinthető lenne.[11]
A lehetőségek közül a fent utolsóként felsoroltat tartotta a legvalószínűbbnek - amelyben azonban nincs határozottan szó arról, hogy az anyag maga egy vírus lenne (bár betegségnek betegség) - de nagyon kidolgozatlan formában a vírusok hipotézise is megjelenik (mint írta, ez „nem zárható ki határozottan, minthogy nem ismerjük bizonyosan egy ilyen vírus természetét”).[14] Nem jutott pénze behatóbb vizsgálatokra - amint ezt jelentéseiben sajnálkozva írta - de ideje sem, minthogy katonai kutatóorvosként részt vett az első világháborúban,[16] és ennek során sokkal inkább kellett foglalkoznia az emberek, mintsem a baktériumok betegségeivel. Cikke nem keltett érdeklődést: a húszas évek elejéig, ha nem is észrevétlenül, de gyakorlatilag visszhangtalanul maradt.[11]
A d'Hérelle-jelenség
A párizsi Pasteur Intézetben Twort felfedezéséről nem tudva dolgozó francia-kanadai mikrobiológus, Felix H. d'Hérelle 1917. szeptember 3-án „Egy láthatatlan, vérhasbaktérium-ellenes mikrobáról” (Sur un microbe invisible antagoniste des bacilles dysentériques) c. dolgozatában bejelentette, hogy vérhasból lábadozó bizonyos betegek ürülékének nedve, ha kis mennyiségben fiatal vérhasbacilus-levestenyészethez adják, akkor az feloldja a tenyészetben lévő baktériumok nagy részét, annak szemmel is jól látható feltisztulását okozva. A nedv akkor is hatásos, ha agyagszűrőn átengedik (tehát a hatás oka nem lehet mikroszkopikus baktérium, hanem csak valamely szubmikroszkopikus tényező); és bár táptalajon sem tenyészthető, de élőnek kell lennie, ugyanis elpusztult baktériumtenyészet nagyon kis mennyiségével friss és egészséges telepeket megfertőzve, az új telep baktériumai ismét csak nagy mennyiségben pusztulnak, és ezt a folyamatot untig ismételni lehet (D'Hérelle első vizsgálataiban 50 ismétlésig is elment [17]). Kézenfekvő tehát a feltételezés, hogy a hatóanyag azért nem hígul fel előbb-utóbb ártalmatlan mértékűvé, mert az újabb és újabb kísérletek során mennyisége újraképződik: vagyis szaporodik.[11][18]
A jelenséget bakteriofágiának (baktériumfalásnak)[19] nevezte el, előidézőjét pedig mikroszkóppal is láthatatlan élőlénynek, „szubmikroszkopikus, kórokozó élő csírának” tartotta, melynek nem sokkal később a bacteriophagum intestinale (bél-baktériumfaló; röviden: bakteriofág) nevet adta.[18] Feljegyzett egy drámai esetet, amikor egy vérhasban szenvedő embert a bakteriofágok teljesen meggyógyítottak.[20] Későbbi állításai szerint a bakteriofágia jelenségét nem ekkor fedezte fel, hanem 1910 és 1915 között az amerikai kontinensen tett utazása során, mely közben egy rajzó sáskafaj bélbetegségét okozó kokkoidális baktérium több évig tartó vizsgálatát végezte. Eme, sáskabaktériumokkal kapcsolatos felfedezéseiről azonban először csak az 1920-as évek elején, különböző könyveiben tett nyilvános említést.[11]
D'Hérelle volt az első – és mintegy húsz éven át az egyetlen – kutató, aki a bakteriofágokat komolyan és kitartóan azonosította a vírusokkal. E gondolat és kifejezés ugyan a témáról írt első, 1917-es cikkében nem fordul elő; azonban 1921-es könyvének („A bakteriofág: szerepe az immunitásban”) 1922-es angol kiadásában már felveti a lehetőséget,[21] és bírálói is gyakran hivatkoztak erre az elméletére már a húszas évek elején.[22][23] 1949-es, visszaemlékezéseket is tartalmazó könyvében úgy ír erről elméletéről, mint ami első pillantásra nyilvánvalóvá volt számára a sáskabaktérium-telepek „tarfoltosodásának” megpillantásakor.
D'Hérelle tevékenységét a húszas években teljesen a fágkutatásnak szentelte, melyben azok gyógyászati felhasználása is elsőrendű szerepet játszott. Már 1921-es könyve is a „A bakteriofág: szerepe az immunitásban” címet viselte, ezt 1922-ben bővített formában németül és angolul is kiadták.
A Twort-d'Hérelle jelenség és a prioritási vita
D'Hérelle egyébként nemsokára értesült Twort felfedezéséről is, de tagadta, hogy az utóbbi kutató által leírt hatás azonos lenne a bakteriofágiával. A tudományos világ azonban nem értett vele egyet. Pl. André Gratia, a későbbi neves mikrobiológus, akinek figyelmét Twort felfedezésére 1920-ban Peter Olitsky nevű kollégája hívta fel (mindketten a New York-i RIMR-ben dolgoztak), miután feltűnt neki Twort és d'Hérelle kísérletei eredményének hasonlósága, még ebben az évben bebizonyította, hogy a glicerines himlőnyirok-massza baktériumszűrőn átengedett szűrlete nemcsak lízist okoz a staphylococcusok levestenyészeteiben (vagyis „Twort anyaga hat d'Hérelle tenyészeteire”), de fordítva („d'Hérelle anyaga is hat a Twort-típusú tenyészetekre”) is igaz: vagyis a d'Hérelle-módra előállított fágfolyadékkal agaros staphylococcus-telepeket megfertőzve, a lízis szintén bekövetkezik (Gratia kísérletei azonban kezdetben Twortéhoz hasonlóan nem kaptak sok figyelmet).[24]

A húszas évek elején megindult a d'Hérelle-jelenség felé az érdeklődés, sorra jelentek meg a bakteriovírus létével szemben meglehetősen kételkedő hangvételű cikkek. Ezenkívül egy csúnya prioritási vita is kezdődött, melynek során két, a fágiával is foglalkozó kutató, Jules Bordet és Mihai Ciuca a tenyészetről tenyészetre átvihető bakteriolízis felfedezésének elsődlegességét egy cikkükben („Megjegyzések az átvihető bakteriolízis kutatásának történetéről”[25]) teljes egészében Twortnak tulajdonították.[11][23] A kérdéses cikkben a szerzők egyáltalán nem plágiumról, hanem finoman csak „a felfedezés történetének helyesbítéséről” beszéltek,[23] sőt hangsúlyozták, hogy D'Hérelle nem tudhatott Twort cikkéről, hiszen a szerzőknek maguknak is elkerülte a figyelmét,[11] továbbá azt is, hogy a francia vizsgálatai önmagukban is érdekesek; mégis a cikk miatt D'Hérelle alakjára a becstelenség vádja vetült.[26] Akadt is, aki többé-kevésbé plagizálónak tartotta (pl. az orvosi Nobel-díjas André Lwoff, aki a negyvenes években szintén a bakteriofágia neves kutatója volt),[11] vagy pedig néhány későbbi történetíró, mint pl. a bakteriofág-kutató Gunther Stent, aki szerint D'Hérelle „vagy Tworttól függetlenül fedezte fel a bakteriális vírusokat, vagy nem”.[27]
A prioritásvita érthetően rendkívül mellbevágó volt a francia kutató számára, hiszen egész szerepét és kétségtelenül óriási munkájának értelmét kérdőjelezte meg. Mikrobiológiai cikkekben nemcsak d'Hérelle-jelenség, hanem Twort–d'Hérelle-jelenség néven is emlegetni kezdték a felfedezéseket.[18][28] Lehetséges, hogy d'Hérelle e vita miatt állt elő ekkoriban a sáskabaktériumok vizsgálatának történetével (ezekről valóban többször írt, 1911-ben a francia Akadémiának, 1914-ben pedig szakcikkekben, de azt a jelenséget, melyet későbbi könyveibe foglalt, azaz a telepek „szűzfoltos” („les taches claires”) pusztulását, ami igazolta volna Tworttal szembeni elsőbbségét, egyik előbbi írás sem említi).[11] Mindazonáltal mai szemmel és a bakteriofágia szempontjából nézve, ez a vita kevéssé érdekes, ugyanis a bakteriolízis jelenségéről már Ny. F. Gamaleia és néhány más kutató is írt 1898-ban (a jelenség elnevezése is tőle származik), viszont az exogén, baktériumfaló kórokozók hipotézise, és így a jelenség valódi természetéhez legközelebbi magyarázat első publikálása kétségtelenül D'Hérelle érdeme: az ő lelkesedése, munkája tartotta életben a fogalmat a kétkedők időnként megsemmisítőnek látszó kritikája közepette, a gondolat mint komoly tudományos hipotézis kétségtelenül az övé; ami Twort esetében lényegében egy periferiális és nem tudni, mennyire komolyan vehető megjegyzés volt, D'Hérelle kutatásainak a lényegét képezte. .
Az ekkori bakteriológia egyik elterjedt (bár kizárólagosnak nem tekinthető) paradigmája volt a vírusokkal kapcsolatban, hogy azok egyfajta ultramikro-baktériumok, azokhoz hasonlóan viselkednek és élnek; csak éppen annyira aprók, hogy áthatolnak a legfinomabb szűrőkön. D'Hérelle elképzelése az „ultramikroszkopikus élő csíráról” teljesen egybevágott ezzel a feltételezéssel.[23] A még Tworttól és Kabéshimától eredő, de elsősorban a tekintélyes Bordet és Ciuca által hirdetett autolizin-elmélet volt d'Hérelle elgondolásainak legfőbb riválisa. Bordet még 1931-ben is így írt: „D'Hérelle vírusa nem létezik”. A belga immunológus már rég Nobel-díjas volt, sokan neki hittek, az autodidakta módra tudóssá lett és elméleteit sokszor túlságos rajongással és magabiztossággal hirdető d'Hérelle-lel szemben.
Az első elméletek és módszeres vizsgálatok
„„Jegyezze meg szavaimat: ez bizonyulhat a mi korszakunk legnagyobb felfedezésének””
– Oscar Bail, Jacob Furthnak, a D'Hérelle-féle bakteriális vírusokról[29]
Kezdetben egyáltalán nem volt bizonyos, hogy mi is a bakteriofágia pontos mechanizmusa: mi történik valójában. A fő problémát az okozta, hogy a fágok fénymikroszkóppal láthatatlanok maradtak (az 1931-ben felfedezett elektronmikroszkóp, melynek segítségével láthatóvá tehetők, az 1930-as évek végéig nem terjedt el).
Ennek ellenére már a korai, a kor eszközkészletének megfelelően a sztereo- és immerziós fénymikroszkópot is bevető, mégis nagyrészt makro-morfológiai szempontú kutatások valószínűsítették, hogy a bakteriofágia a baktériumok betegsége, azonban hogy e betegség pontosan hogyan is megy végbe, arról megoszlottak a vélemények. D'Hérelle nagy meggyőződéssel hirdetett elméletét, miszerint a bakteriofágia egy szubmikroszkopikus külső obligát parazita élőlény (1917), konkrétabban egy ultrafiltrálható vírus (1921) működésének eredménye, nem tartotta kizárhatónak André Gratia (1921/1922);[30] elfogadta továbbá P. C. Flu (1923) és O. Prausnitz (1928),[31] a szerzők túlnyomó többsége azonban a „endogén autolizin” elméletének híve volt,[18][31] miszerint a fág egy ún. lizin,[32] vagyis sejtoldó, fermentum természetű anyag, amely a baktériumok élettevékenysége révén a sejteken belül (endogén módon) keletkezik, illetőleg a baktériumok szaporodásával együtt szaporodik, hogy túltengő mennyiségűvé válván, megtámadja és feloldja a sejteket.[18][31]
D'Hérelle nézeteinek egyik legtekintélyesebb kritikusa az 1919-ben orvosi Nobel-díjassá lett Jules Bordet volt[23] (1925), aki a bakteriolizint a baktériumsejtek anyagcseretermékének, a bakteriofágiát pedig eleinte örökletes betegségnek tekintette,[23][33][34] majd E. Renaux közreműködésével közösen írt cikkeiben azt feltételezte, hogy a lízis a baktériumsejt életműködésének normális velejárója, vagy pedig egy normális folyamat kóros elfajulása: mindenképpen autolízis, amely például táplálékhiány esetében lép fel.[35] Valószínűleg Bordet hatása, hogy a jelenséget kezdetben „bakteriofágia” mellett „transzmisszibilis autolízisnek” (átadatható önfeloldásnak) nevezték. A vírusfertőzés feltételezésén kívül számos egyéb elmélet próbálta magyarázni a jelenséget, mint pl. hogy a fág egy proenzim, amely valamilyen módon aktiválva, autolízist okoz (T. Kabéshima, 1920, az egyik legkorábbi autolitikus elmélet);[36] hogy a fág egy mérgező gátlóanyag, amelyet az egymással versengő fajok termelnek (Lisbonne - Carrère, 1922[37][38]); vagy hogy elszabadult növekedési hormon (R. Doerr, 1922);[34][39] de többségük az endogén módon keletkező lizin gondolatára épült (O. Bail, 1925; E. Wollmann, 1927; R. Otto & H. Munter, 1927; Ph. Hadley, 1928; J. J. Bronfennbrenner, 1928).[23][34]
D'Hérelle a virális patogén látnokinak bizonyuló hipotézise mellett több egyéb, az idő próbáját ki nem álló elméletet is megfogalmazott. Kísérletei során, ha a fágot tartalmazó fertőző folyadékot nagyon felhígította, akkor a telepek pusztulása kevésbé volt látványos, kisméretű foltokban jelentkezett, melyeket „szűzfoltoknak” (magyarul: tarfoltok) nevezett el. A foltos sejtpusztulás a transzmisszibilitás mellett jó érvet szolgáltatott neki ahhoz, hogy a fágtényezőt élőlénynek feltételezze, hiszen ha egyszerű vegyi anyag lenne, akkor kis mérete (és a fertőző folyadékban való diffúziója révén) sokkal egyenletesebben kellene a hatásának eloszlania a tenyészetekben, és így a hatása nem koncentrálódhatna makroszkopikusan látható foltokba.[23] E gondolatmenet nem alaptalan, de a francia kutató még tovább ment, és feltételezte, hogy a tarfoltok a bakteriofágok telepei, és számuk megegyezik a tenyészetet eredetileg megfertőző fág-egyedek számával,[18] ami később nem bizonyult helytállónak. A jelenség egyébként az autogén lizin-elmélet alapján is magyarázható volt, ti. hogy a tarfoltok ott alakulnak ki, ahol a lizinnel szemben nem ellenálló baktériumok vannak, a telep többi része viszont ellenálló az anyaggal szemben[22].
Miután néhány kutató beszámolt egy kísérletről, melynek során tapasztalható volt, hogy bizonyos baktériumtelepek nemcsak fágfolyadákkal fertőződve, hanem más fajú baktériumtelepekkel való érintkezés után is a fágia jelenségét kezdték mutatni, és ebből levonták a következtetést, hogy a fág egy antagonista gátlóanyag, melyet a rivális fajok termelnek egymás ellen, D'Hérelle (nyilván, hogy kórokozó-hipotézisét védje), megfogalmazta azt az elméletet, miszerint egyetlen bakteriofág-faj létezik, amely azonban erősen adaptív volta révén gyakorlatilag bármilyen baktériumfajt képes fertőzni.[40]
Preisz Hugó magyar kutató így összegezte másfél éven át tartó kutatásait egy 1925-ös tanulmányában: „…nyilvánvaló, hogy a bakteriophagiának sokféle megjelenési formája van: amilyen könnyű a fölismerése akkor, amidőn a tenyészet tarfoltokat vagy a jellegzetes kimart és áttetsző szélű telepeket, mikroszkóp alatt a már említett jellegeket mutatja, épp olyan nehéz a phagia fennforgásának megállapítása oly esetekben, amikor ezek a jelek hiányoznak. Számos észlelésem és kísérletem során meggyőződtem, hogy a baktériumtenyészetek, illetőleg telepek bizonyos egyéb, sokkal kevésbé szembetűnő abnormitásai is a bakteriophagia körébe tartoznak … Ebből kiviláglik, hogy a bakteriophagia nem egyszerűen bakteriolysis és hogy a phag-tényező sem lehet egyszerűen egy lizin, a lysis, a baktériumok feloldódása csak egyik és pedig legnagyobb fokú megnyilvánulása a phagiának … Nyilvánvaló, hogy a bakteriophagia a baktériumoknak, mint egysejtű lényeknek betegsége, amely éppúgy, mint szerves lények betegségei általában, sokféle formában nyilvánulhat meg. Ennek a betegségnek kell, hogy előidéző oka legyen, ez az ok külső, exogén természetű … Ez az oki tényező (a bakteriophag vagy phag), bárminő természetű is legyen, nyilván belekerül a baktériumok testébe és ingerként hatva az élő sejt protoplasmájára, ennek működését többé-kevésbé mélyrehatóan módosítja.”[18]
A lizin-elméletet erősítette azonban ekkoriban az ún. spontán bakteriofágia felfedezése. A német mikrobiológusokkal ellentétben magyar kutatók, mint Preisz Hugó vagy Manninger Rezső, a spontán bakteriofágia jelenségét már ebben az időben is kétségbe vonták, és óvatosan ugyan, de feltételezték a fágok kórokozó, élő természetét. Preisz fentebb már idézett tanulmányában beszámolt egy kísérletről, melynek során egy 50 milliószoros higítású fágfolyadékkal való fertőzési próba látszólag ártalmatlannak bizonyult ugyan, de kétszeri átoltásos újratenyésztés után az egyiken a számtalan utódtelep közül mégis megjelent egy tarfolt, amiből újabb átoltással sikerült egy aktív fágiát mutató tenyészetet létrehozni. „Ez a kísérlet világosan mutatja, hogy valamely baktériumtenyészetben a phag lappangva jelen lehet és ismételt továbboltások ellenére is lappangva maradhat, míg egy újabb továbboltáskor egyszerre és váratlanul jelentkezik, ami alkalmas azt a látszatot kelteni, hogy a phag a baktériumok terméke.”[18] Manninger Rezső részletesebb vizsgálatokkal igazolta, hogy a jelenség helyes értelmezése valóban az, hogy a litikus anyag kórokozója lappang, és nem pedig, hogy spontán keletkezik.[41]
Fágterápiás kutatások
A bakteriofágia néhány év alatt az orvosi kutatások egyik kiemelt irányává fejlődött, aminek okait nem nehéz kitalálni: „…D'Hérelle első közleményeire az orvosi laboratóriumokban világszerte foglalkoztak ezzel a biológiai jelenséggel, úgy, hogy a bakteriophagiának ma már terjedelmes irodalma van. Ezt nemcsak azzal lehet értelmezni, hogy maga a jelenség mint természeti tünemény fölötte érdekes s a [természet]búvárt serkentő, hanem hogy jelentős gyakorlati távlatot is nyit meg az orvos előtt: mert – bárminemű természetű legyen is a bakteriophagia oka – ha a bakteriumokat nemcsak in vitro, hanem a baktériumokkal fertőzött emberi vagy állati szervezetben is képes elölni, akkor a fertőző betegségek gyógyításának új lehetősége nyílik meg az orvoslás tudományában.”[18] Ezt a lehetőséget később fágterápiának nevezték, kidolgozására már D'Hérelle is tett kísérleteket. 1926-ban a Nobel-díjas amerikai író, Sinclair Lewis Pulitzer-díjas regényében, az Arrowsmithben megörökítette a bakteriofágok gyógyítási célú használatát (a regény részben D’Hérelle életén alapult); Az 1920-as években Tbilisziben megnyílt a bakteriofág-terápiát kutató Eliava Institute, amit az 1990-es évek elején a grúziai polgárháború pusztításai súlyosan érintettek.
A korai fágterápiás kutatások azonban a bakteriofágokról való hiányos ismeretek és az antibiotikumok felfedezése miatt zsákutcába jutottak, nyugaton a negyvenes évekre gyakorlatilag megszűntek, a Szovjetunióbeli kutatások anyaga pedig elszigetelt maradt. A kezdeti kísérletek színvonaltalanok, sok esetben tudományosan értékelhetetlenek voltak, többek közt azért is, mert a kutatók előtt nem volt még világos a fágok pontos mibenléte; sok kísérletben teljesen oda nem illő betegségeket, pl. vírusfertőzéseket és allergiákat próbáltak vele kúrálni. Így a fágterápiát hamarosan megbízhatatlannak ítélték és elvetették. A néhány évvel később felfedezett antibiotikumok hamar népszerűvé váltak, széles hatásspektrumuk, könnyebb tömeggyártásuk, tárolásuk, felírásuk miatt. Ettől kezdve a Nyugaton felhagytak a fágterápiával.
A kutatások az 1940-es évektől a Szovjetunióban folytak tovább; széles körben alkalmazták, többek közt a Vörös Hadsereg katonái bakteriális fertőzéseinek kezelésére. A kutatási eredményeket oroszul és grúz nyelven publikálták, és nyugaton hosszú ideig hozzáférhetetlenek voltak. Grúziában és más kelet-európai országokban a hidegháború éveiben továbbra is alkalmazták a fágterápiát.[42] Nina Chanishvili 2009-ben, Tbilisziben jelentetett meg monográfiát a témában: A Literature Review of the Practical Application of Bacteriophage Research.[43] A monográfia a témában megjelent szovjet tudományos publikációk részletes elemzését adja.
Hosszú idő után az első nyugat-európai, szabályozott klinikai kísérlet (a fülfertőzést okozó Pseudomonas aeruginosa-val szemben) leírása 2009 augusztusában jelent meg, a Clinical Otolaryngology c. kiadványban.[44] A nyugati kutatók a multirezisztens baktériumokkal szemben biotechnológiai úton megtervezett vírusok bevetésén is dolgoznak.[45]
A szerkezeti kutatás
Az első bakteriofág-egyedet teljes valójában 1939-ben látta meg először Helmut Ruska elektronmikroszkóp alatt. Ezzel bebizonyosodott, hogy a bakteriofágok a vírusok közé tartoznak.
A fágkutatás új korszaka 1938-ban indult el E. L. Ellis, Max Delbrück és S. Luria hatására,[46] akik körül hamarosan egész csoport alakult ki. A kutatás célja immár nem a terápiás célú felhasználás, hanem a fágok szerkezetének és genetikájának feltárása volt,[8] ami végül hozzájárult a molekuláris biológia és a genetika forradalmához. Alfred Hershey és Martha Chase 1952-ben T2 fággal végzett kísérleteikben bizonyították, hogy a DNS az egyedüli és elégséges genetikai kódhordozó.[8] A T típusú bakteriofágok azon szervezetek közé tartoznak, melyek molekuláris biológiáját elsőként sikerült alaposabban feltárni. Kevéssé ismert, hogy a molekuláris genetika több kiemelkedő felfedezője fiatalkorában fágkutatással foglalkozott: közöttük volt Francis Jacob vagy Jaques Monod. James D. Watson, a „kettős spirál” társ-felfedezője, doktori címét a Delbrück-Lurija-féle fágcsoport laboratóriumában szerezte, amely a röntgensugárzással inaktivált bakteriofágok kutatásához kapcsolódott.
A bakteriofágia természetének végső megértését csak ezek a vizsgálatok hozták el.
1969-ben Max Delbrück, Alfred Hershey és Salvador Luria Orvosi Nobel-díjat kaptak a vírusok replikációjával és genetikai szerkezetükkel kapcsolatos felfedezéseikért.
A bakteriofágia folyamata
A bakteriofágia makro-morfológiája
A korai fénymikroszkópos és tenyésztési vizsgálatok a jelenség többféle változatát is feltárták. Tömény baktériumtenyészet és tömény fágfolyadék alkalmazásával a táptalajon pl. 15-20 óra alatt megjelennek a baktériumtelepek, de csak szórványosan, a folyadékkal megkent terület szélén, és a telepek széle rendellenesen csipkés és áttetsző. Ezeket a telepeket a német mikrobiológusok Flatterform-oknak nevezték el. Ritkábban a kenési terület közepén is megjelennek hasonló telepek, ami arra utal, hogy rezisztencia alakult ki a fágfolyadékkal szemben (vagy pedig a folyadék fertőzőképessége valamilyen ok miatt tönkrement). Az áttetsző helyeken a baktériumok egyneműbb, fényáteresztő anyaggá olvadnak össze, az ennek következtében előálló rendellenességek leginkább akkor szembetűnőek, ha a táptalaj ritkásabban lett baktériumokkal behintve, úgyhogy a telepek nem olvadnak össze nagyon korán. Az áttetsző telepek vagy helyek egyszersmind lelapultak, összetöpedtek, fénytelen és gyakran színjátszó felületűek, kisebb nagyítású mikroszkóppal tekintve finoman és sugaras mintázatban ráncoltak, vagy szemcsézettek (jegecesek). A ráncoltság és jegecesedés a phagia igen megbízható jele, még abban az esetben is, ha a lízis nem nyilvánvaló.
A fágfolyadék higítását fokozatosan csökkentve, a kísérletek ilyen változata az ún. tarfoltos fágia megjelenéséhez vezet:[47] a baktériumok sűrű lepedéket képeznek, de ebben tűszúrásnyi, 1–2 mm-es átmérőjű kerekded áttetsző foltok mutatkoznak, a higítási arány a foltok sűrűségét befolyásolja, bár az összefüggés nem .
Erős nagyítással és sejtfestéssel mindkét esetben megfigyelhető nemcsak a baktériumok pusztulása, de a fertőzött sejtek elváltozása is: egyes festett baktériumok a normálisnál sokkal duzzadtabbak, rendes átlagtérfogatuk 10-20-szorosára is megnőhetnek, sokszor vacuola- vagy spóraszerű képződményekkel a belsejükben, amik vagy maguk a sejtek is, erősen fénylővé és fénytörővé válhatnak; alakjuk pedig gömbszerűből megnyúlttá és hurkaszerűen görbévé, illetve agancsosan elágazóvá deformálódhat. A sejtek festődési tulajdonságai és a telepek szerkezete is megváltozhat, a vérhasbaktériumok például a lépfenebaciluséra emlékeztető fonalas telepeket kezdenek létrehozni, a kólibacilusok telepei pedig rendellenes módon nyálkássá válnak.
Előfordulhat azonban, hogy a bakteriofágiának nyilvánvaló makroszkópos és mikroszkópos jele nincs, és a részletesebb vizsgálat is csak a baktériumok alakjának és méretének némi megváltozását konstatálja. Előfordulhat, hogy a fágia csak mikroszkóppal látható jeleket mutat: tűszúrásnyi méretű besüppedések, durvább szerkezetű ráncok vagy szemcsék a telepeken, a telepek áttetsző, sugaras pontokból kiinduló repedései.[18]
A bakteriofágia sejtbiológiai osztályzása és leírása
A bakteriofágok szaporodhatnak litikus ciklus vagy lizogén ciklus útján, néhány vírus pedig mindkettőre képes. A litikus fágok, mint a T4 fág esetében a virion sokszorozódása során a baktériumsejtek felbomlanak (lízis) és elpusztulnak. Ahogy a sejt elpusztul, az új fágok új gazdaszervezetet kereshetnek. A litikus fágok alkalmazhatók fágterápiás kezelésre.
Ezzel kontrasztban a lizogén ciklus nem eredményezi a gazda-baktériumsejt azonnali pusztulását. A lizogéniára képes fágokat mérsékelt fágoknak (temperált fágok) nevezzük. Ezek virális genomja integrálódik a gazda DNS-ébe, és viszonylag ártalmatlan módon, azzal együtt replikálja magát, vagy akár végül a baktérium plazmidjává válik. A vírus szunnyadó állapotban van jelen, amíg a gazdaszervezetben a körülmények meg nem romlanak, például a tápanyagok megfogyatkozása miatt; ekkor az endogén fágok (profág) aktivizálódnak. Beindítják a reprodukciós ciklust, ami a gazdasejt lízisét okozza. Mivel a lizogén ciklus lehetővé teszi a gazdabaktérium számára a túlélést és a szaporodást, a vírus jelen van a sejt valamennyi leszármazottjában.
Néha a profágok jótékony hatásúak a baktérium számára, szunnyadó állapotukban új funkciókat adva a baktérium genomjához. Ezt a jelenséget lizogén konverziónak nevezik. Legismertebb példája, amikor a Vibrio cholerae egy ártalmatlan törzsét egy fág virulenssé, így a kolerabetegség kórokozójává teszi. Ez az ok, amiért a mérsékelt fágokat nem alkalmazzák a fágterápiában.
Megtapadás és penetráció
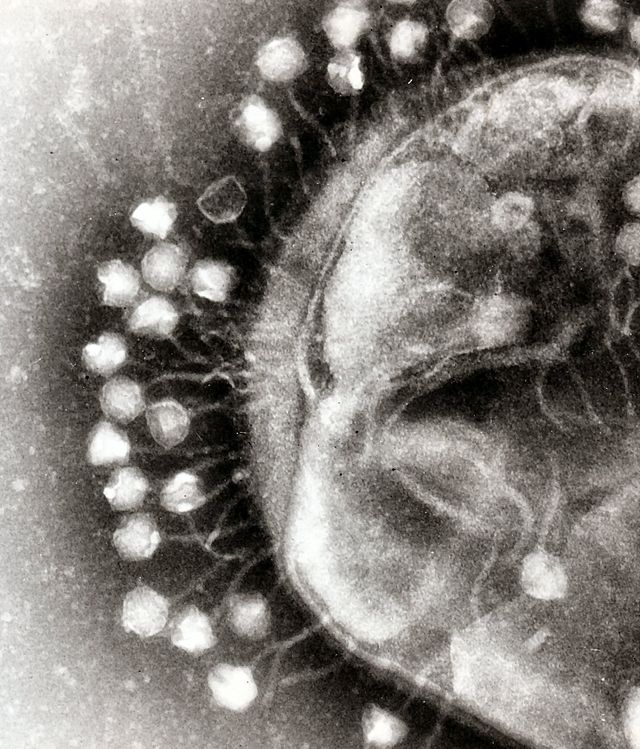
A gazdasejtbe való behatoláshoz a bakteriofágoknak a baktérium felszínén található specifikus receptorokhoz kell tapadniuk – ezek lehetnek lipopoliszacharidek, lipo-teichoinsavak, fehérjék vagy akár az ostorok. A bakteriofág specificitása azt jelenti, hogy a fág csak azokat a baktériumokat képes fertőzni, amik hordozzák a receptorokat, amikhez kötődni képes. A szélesebb gazdaspektrumú bakteriofágokat polivalens vagy WHR („Wide Host Range”) bakteriofágoknak nevezik.[48] A gazdasejt növekedési feltételei is befolyásolják a fágok képességét a megtapadásra és a penetrációra.[49] Mivel a fág virionjai önálló mozgásra nem képesek, így rá vannak utalva arra, hogy a vizes oldatban (vér-, nyirokkeringés, öntözés, talajvíz stb.) véletlenszerűen találkozzanak épp a nekik megfelelő receptorral.
A komplex bakteriofágok az örökítő anyag baktériumba fecskendezéséhez hipodermális injekciós tű-szerű módszert alkalmaznak. Miután kapcsolódtak a megfelelő receptorhoz, a farokrész fehérjeszálai az alaplemezt közelebb hozzák a sejtfelszínhez. Miután teljesen megtapadtak, a farok összehúzódik, talán a farokban található ATP segítségével,[5] a bakteriális membránon keresztül injektálva az örökítő anyagot a sejtbe.
Fehérje- és nukleinsav-szintézis
A penetráció megtörténte után a baktérium riboszómái perceken belül megkezdik a vírus mRNS-e alapján a fehérjegyártást. Az RNS-alapú fágoknál a folyamat korai szakaszában megtörténik az RNS-replikáz szintézise. A fehérjék úgy módosítják a bakteriális RNS-polimerázt, hogy az előnyben részesítse a vírus mRNS-ének átírását. A gazdaszervezet fehérje- és nukleinsav-szintézise felborul, a normál üzem helyett virális termékek gyártására kényszerül. Ezekből a termékekből új, a sejten belüli virionok alkotóelemei, az új virionok gyártását segítő fehérjék, vagy a baktérium lízisét elősegítő fehérjék (helper protein) lesznek. Walter Fiers, a belgiumi Ghenti Egyetem kutatója volt az első, aki megállapította egy gén komplett nukleotidsorrendjét (1972), és az MS2 fág teljes genomjáét (1976).[50]
Virionok „összeszerelése”
A T4 fág esetében az új vírusrészecskék összeszereléséhez helper fehérjék közreműködése szükséges. Először az alaplemezek szerelődnek össze, a farokrész csak ez után. A külön összeszerelt feji kapszidrészek spontán módon összeépül a farokrészekkel. A DNS hatékonyan összecsomagolt állapotban található a fejen belül. Az egész folyamat mintegy 15 percet vesz igénybe.

Az érett virionok kiszabadulása
A fágok a baktériumból kiszabadulhatnak lízis, kilökődés, vagy egyes esetekben bimbózás (a gazdasejt membránját használva burokként) útján. A farokkal rendelkező fágok egy endolizin nevű enzimmel végzik a sejt lízisét, ami megtámadja és feloldja a peptidoglikán sejtfalat. Egy másik fágtípus, a fonalas fág a sejtet folyamatosan új vírusrészecskék kiválasztására készteti. A bimbózás egyes Mycoplasma-fágok jellemzője. A lizogén életciklusú fágok nem pusztítják el a gazdaszervezetet, hanem profágként hosszabb együttélésre rendezkednek be.
Környezeti előfordulásuk
A metagenomika lehetővé tette a bakteriofágok vízből történő kimutatását olyan helyeken is, ahol eddig nem volt lehetséges. A kutatások megmutatták, hogy az édesvízi és tengeri élőhelyek vízoszlopaiban sokkal elterjedtebbek a fágok, mint korábban gondolták, és a bakteriális plankton mortalitásának jelentős részéért felelősek. A bakteriofágok nem csak a legnagyobb számban előforduló, de valószínűleg a legváltozatosabb biológiai entitások is egyben.[3]
Kifejlesztették a fágok közösségi ökológiájának vizsgálati módszereit, hogy megbecsüljék a fágok által kiváltott bakterioplankton-mortalitást, a fágok szerepét a táplálékhálózatban és a biogeokémiai ciklusokban, levegyék egyes fágpopulációk vagy -közösségek genetikai ujjlenyomatát, és metagenomikai módszerekkel megbecsüljék a vírusok biodiverzitását. A baktériumok fágok által kiváltott lízise az addig kötött formában (sejtekben) jelen levő szenet felszabadítja, az a többi élőlény számára könnyebben felvehető, vízben oldott formába kerül. A fágközösségekből szekvenált adatok többsége új, addig nem fordult elő az adatbázisokban. Ezek az adatok, és más kutatások eredményei arra utalnak, hogy a fágspecifikus gének és ökológiai jellemzők sűrűbben fordulnak elő, mint korábban gondolták. Ennek a genetikai és ökológiai sokrétűségnek a megértéséhez kutatásokat kell folytatni a fágközösségekkel, méghozzá a mikroorganizmusok kontextusában alkalmas térbeli és időbeli skálán.[3]
A fágok felhasználása
Szerepük az élelmiszer-előállításban
Sok élelmiszeripari termék, vegyi áru és biotechnológiai termék előállításában hasznosítanak a fermentálásra különböző, szerves szubsztrátokon ipari méretekben szaporított baktériumokat. Mivel hatalmas baktériummennyiség jön létre nap mint nap a fermentáló kádakban, egy bakteriofág-fertőzés végzetes hatású lenne a termelésre. Az így bekövetkező termeléskiesés komoly gazdasági kockázatot jelent ezekben az iparágakban. Az élelmiszer-előállítás szempontjából igen lényeges a bakteriofágok és a gazdabaktériumok kapcsolata; vizsgálni és kontrollálni kell a fertőződési lehetőségeket, a terjedési útvonalakat, biotechnológia védekezési stratégiákkal visszafogni a szóba jövő fágok terjedését. A tejágazat nyíltan elismerte a fágok problémájának létezését, és évtizedek óta együttműködik a kutatóintézetekkel a fágok elleni védekezésben.[3]
2006 augusztusában az USA Élelmiszer- és Gyógyszerellenőrző Hivatala (United States Food and Drug Administration, FDA) engedélyezte a bakteriofágok használatát a sajton tenyésző Listeria monocytogenes baktériummal szemben, biztonságosnak tekintve azt (GRAS státus, Generally Recognized As Safe).[51] 2007 júliusában az engedélyt kiterjesztették az összes élelmiszeripari termékre.[52]
Modern fágterápiás és köztisztasági alkalmazások
Az amerikai kutatócsoportok is számos előrelépést jelentettek. Létezik már spray alapú felhasználás növények és zöldségek rothadása és a bakteriális betegség terjedése ellen. Más felhasználási módjuk felületek fertőtlenítése (biocid anyagként) pl. kórházakban, orvosi eszközök előzetes fertőtlenítésére, vagy katéterek fertőzésének megelőzésére. A technológia most már alkalmas száraz felületeken (munkaruhák, függönyök, varratok) való alkalmazásra is. A Lancetben folyó klinikai vizsgálatok eredményesnek mutatják kutyák középfülgyulladásának (otitis) kezelésében is.[53]
Felhasználásuk hidrológiai jelölőanyagként
A bakteriofágokat felhasználják hidrológiai modellezésekben is, főleg, ahol felszíni és felszín alatti vizek interakcióját is nyomon kell követni. A fágok jobb jelölőnek bizonyultak, mint a hagyományos festékek, mivel jóval kevésbé hajlamosak felszívódni a felszín alatti vizekben, és mert nagyon alacsony koncentrációban is kimutathatók.[54]
Egyéb felhasználásuk
Nyugati kormányzati szervek évek óta próbálnak Grúziától és a volt Szovjetunió államaitól segítséghez jutni egyes biológiai fegyverek és toxinok, mint az anthrax és a botulizmus fágokkal való leküzdésében.[55] Az epidemiológiában (járványtan) 1938-tól kezdve megindult a fertőző baktériumok bakteriofágokkal való azonosításának, az ún. fágtípus-meghatározásnak sikeres módszertani kidolgozása, melyet 1948-tól kezdve Magyarországon is bevezettek (a módszert eredetileg a hastífuszt okozó szalmonellabaktérium ellen fejlesztették ki).[56] E vizsgálati módszer azon alapul, hogy csak azok a baktériumok érzékenyek az adott fág(ok)gal szemben, amelyek a fágadszorpcióhoz megfelelő fágreceptorral rendelkeznek. A fágtípus-meghatározáshoz használt fágok, az ún. típusfágok a tipizálandó baktériumtörzseket azok érzékenysége esetén feloldják (lízis). A típusfágokkal kapott oldások alapján állapítható meg a fágtípus/fágkép, melyet többnyire fágtípus-séma(ák) alapján szám vagy betűjellel történt kódolás után adnak meg.[57][58]
Jegyzetek
Források
További információk
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
