
Malonitril
From Wikipedia, the free encyclopedia
A malonitril (más néven malonsavdinitril) a nitrilek közé tartozó szerves vegyület, képlete CH2(CN)2. Vízben, alkoholban és éterben oldódik.[2]
További információk Kémiai azonosítók, SMILES ...
| Malonitril | |||
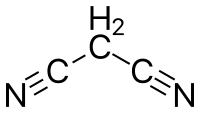 A malonitril szerkezeti képlete | |||
 A malonitril pálcikamodellje |  A malonitril kalottamodellje | ||
| IUPAC-név | propándinitril | ||
| Más nevek | cianoacetonitril, dicianometán, malononitril | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 109-77-3 | ||
| PubChem | 8010 | ||
| ChemSpider | 13884495 | ||
| EINECS-szám | 203-703-2 | ||
| MeSH | dicyanmethane | ||
| ChEBI | 33186 | ||
| RTECS szám | OO3150000 | ||
| |||
| InChIKey | CUONGYYJJVDODC-UHFFFAOYSA-N | ||
| Beilstein | 773697 | ||
| Gmelin | 1303 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C3H2N2 | ||
| Moláris tömeg | 66,06 g/mol | ||
| Megjelenés | színtelen kristályok vagy fehér por[1] | ||
| Sűrűség | 1,049 g ml−1 | ||
| Olvadáspont | 32 °C | ||
| Forráspont | 220,05 °C | ||
| Oldhatóság (vízben) | 13% (20 °C)[1] | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH | 187,7–188.1 kJ mol−1 | ||
| Égés standard- entalpiája ΔcH | −1,6540–−1,6544 MJ mol−1 | ||
| Standard moláris entrópia S | 130,96 J K−1 mol−1 | ||
| Hőkapacitás, C | 110,29 J K−1 mol−1 | ||
| Veszélyek | |||
| PEL | nincs[1] | ||
| LD50 | 19 mg kg−1 (egér, szájon át) 350 mg kg−1 (patkány, bőrön át) | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
Bezárás
Viszonylag savas vegyület – pKa értéke vízben 11[3] –, ami lehetővé teszi felhasználását a Knoevenagel-kondenzációs reakcióban, például a CS gáz előállítására:

Kiindulási anyagként használható a Gewald-reakcióban is, melynek során a nitril elemi kén és bázis jelenlétében ketonnal vagy aldehiddel kondenzációs reakcióba lépve 2-aminotiofén terméket eredményez.[4]