
Kénsav
szervetlen vegyület, erős sav / From Wikipedia, the free encyclopedia
A kénsav (H2SO4) színtelen, nagy sűrűségű folyadék, kétértékű, erős ásványi sav. Vízzel korlátlanul elegyedik. A kénsav a kémiai ipar egyik legfontosabb vegyülete, a legnagyobb mennyiségben előállított anyag. 2001-ben 165 millió tonnát gyártottak belőle. Legnagyobb arányban a műtrágyaipar hasznosítja, de szinte minden vegyipari ágazat alapanyagként használja.
| Ez a szócikk a kénsavról szól. Hasonló címmel lásd még: kénessav. |
| Kénsav | |||
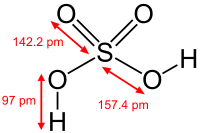 | |||
 | |||
 | |||
| IUPAC-név | kénsav | ||
| Más nevek | vitriol, óleum, akkumulátorsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 7664-93-9 | ||
| ChemSpider | 1086 | ||
| EINECS-szám | 231-639-5 | ||
| KEGG | D05963 | ||
| ChEBI | 26836 | ||
| RTECS szám | WS5600000 | ||
| |||
| |||
| InChIKey | QAOWNCQODCNURD-UHFFFAOYSA-N | ||
| UNII | O40UQP6WCF | ||
| ChEMBL | 572964 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | H2SO4 | ||
| Moláris tömeg | 98,079 g/mol | ||
| Megjelenés | tiszta, színtelen, szagtalan, olajszerű viszkózus folyadék | ||
| Sűrűség | 1,84 g/cm³ (folyadék) | ||
| Olvadáspont | 10 °C | ||
| Forráspont | 337 °C (300 °C felett lassan bomlik) | ||
| Oldhatóság (vízben) | korlátlanul elegyedik exoterm reakció | ||
| Savasság (pKa) | −3, 1,99 | ||
| Viszkozitás | 26,7 cP (20 °C) | ||
| Termokémia | |||
| Std. képződési entalpia ΔfH | −814 kJ·mol−1[1] | ||
| Standard moláris entrópia S | 157 J·mol−1·K−1[1] | ||
| Hőkapacitás, C | 131 J/(mol·K) | ||
| Veszélyek | |||
| MSDS | ICSC 0362 | ||
| EU osztályozás | |||
| EU Index | 016-020-00-8 | ||
| NFPA 704 | |||
| R mondatok | R35 | ||
| S mondatok | (S1/2) S26 S30 S45 | ||
| Lobbanáspont | nem gyúlékony | ||
| LD50 | 2140 mg/kg (patkány, szájon át), LC50 = 25 mg/m³ (patkány, belélegezve) | ||
| Rokon vegyületek | |||
| Azonos anion | szulfátok | ||
| Rokon vegyületek | kénessav | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A tömény kénsav erélyes vízelvonószer. Noha előállítható a 100%-os töménységű, úgynevezett füstölgő kénsav (más néven: óleum) is, a gyakorlatban 98,3%-nál töményebb savat a kén-trioxid (SO3) párolgása miatt nem használnak. Az ólomakkumulátorok celláit 33,5%-os kénsavval töltik fel.
A kénsav előfordul a természetben is, de csak kis mennyiségben, például egyes vulkáni vidékek folyóiban, vagy a kénvegyületek oxidációjaként kén-hidrogént tartalmazó barlangokban. Az iparban a kén-trioxid kénsavban való elnyeletésével, majd az így keletkezett óleum vízzel való hígításával állítják elő.
- H2SO4 + SO3 → H2S2O7
- H2S2O7 + H2O → 2 H2SO4
