Repetición rica en leucina
From Wikipedia, the free encyclopedia
Unha repetición rica en leucina (LRR) é un motivo estrutural de proteína que forma un pregamento en ferradura α/β.[1][2] Está composta de tramos de 20 a 30 aminoácidos repetidos que son inhabitualmente ricos no aminoácido hidrofóbico leucina. Estas repeticións xeralmente préganse xuntas para formar un dominio proteico de solenoide, denominado dominio de repeticións ricas en leucina. Normalmente, cada unidade repetida ten unha estrutura de febra beta-xiro-hélice alfa, e o dominio ensamblado, composto de moitas desas repeticións, ten forma de ferradura cunha folla beta paralela interior e un conxunto exterior de hélices. Unha face da folla beta e un lado do conxunto de hélices están expostos ao solvente e están, por tanto, dominados por residuos hidrófilos. A rexión entre as hélices e follas é o núcleo hidrofóbico da proteína e está estreitamente empaquetado estericamente con residuos de leucina.
| Repetición rica en leucina | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 Exemplo dunha proteína de repetición rica en leucina, un inhibidor da ribonuclease porcina | |||||||||||
| Identificadores | |||||||||||
| Símbolo | LRR_1 | ||||||||||
| Pfam | PF00560 | ||||||||||
| Pfam clan | CL0022 | ||||||||||
| InterPro | IPR001611 | ||||||||||
| SCOPe | 2bnh / SUPFAM | ||||||||||
| OPM protein | 1xwd | ||||||||||
| |||||||||||
| Repetición rica en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
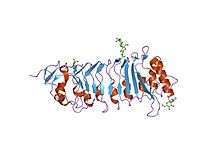 A estrutura cristalina de pgip (proteína inhibidora da poligalacturonase), unha proteína de repetición rica en leucina implicada na defensa das plantas | |||||||||
| Identificadores | |||||||||
| Símbolo | LRRNT_2 | ||||||||
| Pfam | PF08263 | ||||||||
| InterPro | IPR013210 | ||||||||
| SMART | LRRNT | ||||||||
| SCOPe | 1m10 / SUPFAM | ||||||||
| |||||||||
| Repetición rica en leucina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Unha variante de repetición rica en leucina cun motivo estrutural repetitivo de proteína novo | |||||||||
| Identificadores | |||||||||
| Símbolo | ? | ||||||||
| Pfam | PF05484 | ||||||||
| Pfam clan | CL0020 | ||||||||
| InterPro | IPR008665 | ||||||||
| SCOPe | 1lrv / SUPFAM | ||||||||
| |||||||||
As repeticións ricas en leucina están implicadas frecuentemente na formación de interaccións proteína-proteína.[3][4]
Exemplos
Os motivos de repeticións ricas en leucina foron identificados en gran número de proteínas funcionais non relacionadas.[5] O exemplo mellor coñecido é o inhibidor da ribonuclease, pero outras proteínas como o regulador da tropomiosina chamado tropomodulina e o receptor de tipo Toll tamén comparten o motivo. De feito, o receptor de tipo Toll posúe 10 motivos LRR sucesivos, que serven para unirse a padróns moleculares asociados a patóxenos ou outros perigos.
Aínda que a proteína LRR canónica contén aproximadamente unha hélice par cada febra beta, as variantes que forman os pregamentos de superhélice beta-alfa ás veces teñen longos bucles en vez de hélices que se unen a sucesivas febras beta.
Un dominio variante de repetición rica en leucina (LRV) ten un novo motivo estrutural repetitivo consistente en hélices alternantes de tipo alfa e de tipo 310 dispostas nunha superhélice dextroxira, con ausencia das febras beta presentes noutras repeticións ricas en leucina.[6]
Dominios asociados
As repeticións ricas en leucina xeralmente están flanqueadas por dominios ricos en cisteína N-terminais e C-terminais, pero non sempre, como no caso de C5orf36.
Tamén aparecen xunto con dominios "adxacentes a LRR". Estes son pequenos dominios feitos enteiramente de febras beta, que foron descritos estruturalmente para a proteína internalina (InlA) e as proteínas relacionadas InlB, InlE, InlH da bacteria patóxena Listeria monocytogenes. A súa función parece ser principalmente estrutural. Están fusionadas ao extremo C-terminal das repeticións ricas en leucina, estabilizando significativamente o LRR, e formando unha entidade ríxida común co LRR. Non están implicadas por si mesmas en interaccións proteína-proteína, pero axudan a presentar o dominio adxacente a LRR para que estableza ditas interaccións. Estes dominios pertencen á familia dos dominios de tipo inmunoglobulina, xa que constan de dúas follas beta en sándwich que seguen a conectividade clásica dos dominios Ig. As febras beta dunha das follas son, non obstante, moito menores que as da maioría dos dominios de tipo Ig estándar, polo que en certa medida son un caso á parte.[7][8][9]
Un clúster de ferro-xofre encóntrase no N-terminal dalgunhas proteínas que conteñen o "dominio variante de repeticións ricas en leucina" (LRV). Estas proteínas teñen unha estrutura en dous dominios, composta por un dominio N-terminal que contén un grupo de catro residuos de cisteína que alberga o clúster 4Fe:4S, e un dominio C-terminal maior que contén as repeticións LRV.[6] Os estudos bioquímicos revelaron que o clúster 4Fe:4S é sensible ao oxíxeno, mais non parece ter actividade redox reversible.
Notas
Véxase tamén
Wikiwand - on
Seamless Wikipedia browsing. On steroids.



