Loading AI tools
composé chimique, herbicide De Wikipédia, l'encyclopédie libre
Le paraquat, également appelé gramoxone, est un herbicide produit à des fins commerciales à partir de 1961 par Imperial Chemical Industries (devenu Syngenta). Il appartient à la famille chimique des pyridines, qui comprend d'autres produits phytosanitaires possédant des propriétés similaires.
| Paraquat | ||

| ||
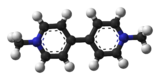 | ||
| Représentation 3D de la molécule | ||
| Identification | ||
|---|---|---|
| Nom UICPA | 1,1’–diméthyl-4,4’-bipyridinium | |
| Synonymes |
Gramoxone |
|
| No CAS | ||
| No ECHA | 100.016.015 | |
| No CE | 225-141-7 | |
| SMILES | ||
| InChI | ||
| Apparence | poudre blanche | |
| Propriétés chimiques | ||
| Formule | C12H14N2 [Isomères] |
|
| Masse molaire[1] | 186,253 ± 0,011 g/mol C 77,38 %, H 7,58 %, N 15,04 %, |
|
| Propriétés physiques | ||
| T° fusion | 175 à 180 °C | |
| T° ébullition | décomposition >300 °C | |
| Solubilité | soluble dans l'eau | |
| Masse volumique | 1,25 liquide | |
| Pression de vapeur saturante | 700 g·L-1 à 20 °C | |
| Précautions | ||
| SGH | ||
| H301, H311, H315, H319, H330, H335, H372 et H410 |
||
| Directive 67/548/EEC | ||
| Inhalation | Irritation des muqueuses respiratoires. Fibrose pulmonaire aiguë. |
|
| Peau | Irritation | |
| Yeux | Irritation des muqueuses oculaires |
|
| Ingestion | Brûlures du système digestif. Dommages aux reins. |
|
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
| Dichlorure de paraquat | |
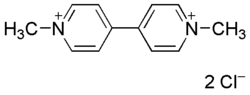
| |
| Identification | |
|---|---|
| Nom UICPA | Dichlorure de 1,1’-Diméthyl-4,4’-bipyridinium |
| No CAS | |
| No ECHA | 100.016.015 |
| No CE | 217-615-7 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C12H14Cl2N2 |
| Masse molaire[2] | 257,159 ± 0,015 g/mol C 56,05 %, H 5,49 %, Cl 27,57 %, N 10,89 %, |
| Précautions | |
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
| Paraquat méthylsulfate | |
| Identification | |
|---|---|
| Nom UICPA | di(méthylsulfate) de 1,1’-Diméthyl-4,4’-bipyridinium |
| No CAS | |
| No ECHA | 100.016.015 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C14H20N2O8S2 |
| Masse molaire[3] | 408,447 ± 0,025 g/mol C 41,17 %, H 4,94 %, N 6,86 %, O 31,34 %, S 15,7 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le paraquat est hautement toxique à l'ingestion et présenterait des effets indésirables sur la santé lors de contacts prolongés.
| No CAS | Nom commun | Nom chimique |
|---|---|---|
| Paraquat | 1,1’-Diméthyl-4,4’-bipyridinium | |
| Paraquat chlorure | Dichlorure de 1,1’-Diméthyl-4,4’-bipyridinium | |
| Paraquat méthylsulfate | di(méthylsulfate) de 1,1’-Diméthyl-4,4’-bipyridinium |
Le paraquat est l’un des herbicides les plus utilisés au monde, vendu dans plus de 120 pays (selon son fabricant).[réf. nécessaire] Bien que très toxique, pour son faible coût et sa facilité d'utilisation, il sert en agriculture, floriculture et dans certains boisements à désherber ou préparer le sol pour une centaine de cultures de céréales (maïs, blé, orge, seigle, riz...), de soja, pomme de terre, fruits (pomme, orange, banane), de plantes destinées à la fabrication de boissons (café, thé, cacao) et des cultures traitées (coton, huile de palme, canne à sucre et caoutchouc). Il vise à protéger les semis contre la concurrence d'un large éventail de plantes pluriannuelles, les adventices, qui réduisent le rendement et la qualité de la récolte par compétition pour l'espace, l'eau, les nutriments, et la lumière. Il est aussi de plus en plus utilisé pour préparer le semis direct, notamment là où les adventices sont devenues résistantes au glyphosate (mais avec le risque de générer de nouvelles résistances au paraquat, cette fois).[réf. nécessaire]
Le paraquat-chlorure se présente sous la forme de cristaux incolores et inodores. Il n’est pas volatil. Très soluble dans l’eau, il l'est légèrement dans l’éthanol et l’acétone ; il est insoluble dans les hydrocarbures. Les sels de paraquat et leurs solutions aqueuses ne sont pas inflammables.
Il se décompose au-dessus de 300 °C, produisant des fumées toxiques.
Il attaque les métaux, notamment le fer.
Quelques caractéristiques le distinguent d'autres substances actives d'herbicides de contact :
Les préparations légales les plus utilisées en France étaient des solutions aqueuses contenant au maximum 40 g·L-1 de paraquat sous forme de dichlorure. Des spécialités contenant en plus du paraquat d’autres matières actives (simazine, diuron ou diquat) existaient aussi. Ces préparations étaient colorées en bleu et dénaturées par adjonction d’une substance odorante, répulsive et émétique. Cependant, la firme ICI fabricant le Paraquat est suspectée d'avoir limité la quantité d'émétique pour des raisons de coût dans certains produits, à une dose insuffisante pour protéger du risque d'ingestion[4]. Le produit était pulvérisé après dilution dans l’eau.
Le professeur de toxicologie clinique à l’université d’Edimbourg Michael Eddleston estime en 2021 que probablement plus de 100 000 personnes sont mortes empoisonnées au Paraquat depuis sa mise sur le marché dans les années 1960[4].
Le paraquat est dangereux par sa forte toxicité aiguë par ingestion, même à faible dose[5]. Il est à l'origine de controverses, notamment aux Antilles[6].
Essentiellement effet irritant de la peau, des muqueuses oculaires et respiratoires.
Dans les années , l'ONG nicaraguayenne Fundacion Nica Global a alerté sur l'effet potentiel que pourrait avoir le paraquat sur une épidémie d'insuffisance rénale chronique qui concernerait les planteurs de canne à sucre et atteindrait directement plus de 2 500 travailleurs. Si cette alerte fut relayée dans certains médias, elle donna lieu à une controverse sur l'implication des pesticides et notamment le paraquat[10],[11]. Une étude récente indique que l'exposition au glyphosate, lorsqu'elle est associée au paraquat, aurait un effet synergique et pourrait effectivement conduire à l'apparition d'insuffisance rénale chronique[12].
Expérimentalement :
La valeur limite d'exposition professionnelle (VLE) est fixée à 0,1 mg·m-3.
L'intérêt pour le paraquat provient de sa similarité structurale avec le MPP+, un produit issu du catabolisme du MPTP (1-méthyle-4-phényl-1,2,3,6-tétrahydropyridine)[14]. Le MPTP est utilisé dans l'industrie comme intermédiaire de synthèse. Le chlorure de MPP+ a notamment été utilisé pour produire le Cyperquat, un herbicide, dans les années [15] ; substance structurellement proche du paraquat, elle a été suspectée d’avoir la même toxicité, bien que les études épidémiologiques, à l'époque, ne semblaient pas en apporter la preuve[16].
Des études épidémiologiques plus récentes indiquent un excès de risque - deux fois plus élevé - de développer la maladie de Parkinson lors d'une exposition à des pesticides causant un stress oxydatif et notamment le paraquat[17],[18]. Il a par ailleurs été montré que le paraquat avait un effet synergique lorsqu'il était associé au manèbe et au zirame ; dans le cas d'une exposition à ces trois pesticides, le risque de développer la maladie de Parkinson est multiplié par trois[19],[20].
Le MPTP est une neurotoxine qui peut être produite au cours de la synthèse de MPPP (1-methyl-4-phenyl-4-propionoxypiperidine) (en), c'est pour cette raison que son rôle inducteur d'un syndrome Parkinsonien a été découvert dans les années [21]. Sa neurotoxicité avait déjà été suspectée en lorsque Barry Kidston, un étudiant en chimie du Maryland âgé de 23 ans, s’était injecté du MPPP qu’il avait synthétisé de manière incorrecte en générant des impuretés, le MPTP. Le MPPP est un opioïde de synthèse, analogue de la péthidine, utilisé par les toxicomanes comme drogue récréative et qui a des effets similaires à ceux de l’héroïne et de la morphine. Il a été ainsi été lésé par le MPTP, et à l’issue d’un délai de trois jours, il a commencé à développer les symptômes de la maladie de Parkinson, symptômes éliminés avec succès par un traitement à la levodopa ; il décédera 18 mois plus tard d'une overdose de cocaïne. Lors de l'autopsie, on a découvert une destruction des neurones dopaminergiques de la substance noire[22].
Le MPTP lui-même n'est pas toxique et comme tout composé liposoluble, il peut traverser la barrière hémato-encéphalique. Une fois à l'intérieur du cerveau, le MPTP est métabolisé en une substance toxique le 1-méthyl-4-phenylpyridinium (MPP +) par la monoamine oxydase (MAO-B), une enzyme présente dans les cellules gliales. Le MPP+ est transporté dans les neurones dopaminergiques par le transporteur de la dopamine (en). Il détruit essentiellement les neurones dopaminergiques dans une partie du cerveau appelée la substance noire. Le MPP+ interfère avec le complexe I de la chaîne respiratoire, un élément du métabolisme des mitochondries, ce qui conduit à la mort cellulaire et provoque l'accumulation de radicaux libres, des molécules toxiques qui contribuent ultérieurement à la destruction des cellules.
Langston et al. (1984) ont constaté que l'injection de MPTP, chez le singe Saïmiri, entraînait également un syndrome Parkinsonien[23]. Les symptômes induits pouvaient être atténués par la lévodopa, un précurseur de la dopamine, principal traitement de la maladie de Parkinson. Les structures cérébrales affectées et les manifestations pathologiques générées par l'injection de MPTP récapitulent presque parfaitement celles de la maladie de Parkinson, hormis la formation des corps de Lewy. Le MPTP est ainsi utilisé pour modéliser la maladie de Parkinson, chez l'animal, en vue d'étudier la physiopathologie de cette maladie et d’évaluer des traitements potentiels. Des études sur la souris ont montré que la sensibilité au MPTP augmentait avec l'âge.
Il a été postulé que la maladie de Parkinson pourrait être provoquée par l’accumulation de faibles quantités de MPP+ composées d’un apport exogène par ingestion ou par le biais d'expositions répétées, et que ces substances sont en concentration trop minime pour être détectées de manière significative par des études épidémiologiques[24].
La connaissance du MPTP et son utilisation pour recréer un modèle expérimental fiable de la maladie de Parkinson a incité les scientifiques à étudier les possibilités d'une intervention chirurgicale remplaçant la perte des neurones par des implants de tissus fœtaux et de cellule souche ou la stimulation électrique cérébrale sous-thalamique, recherches[25], qui toutes initialement ont fait preuve d’une réussite provisoire.
En 2000, un autre modèle animal de la maladie de Parkinson a été découvert[26]. Les auteurs de l'étude ont mis en évidence que la roténone, un insecticide, provoquait un syndrome Parkinsonien chez le rat en détruisant les neurones dopaminergiques de la substance noire. Comme le MPP+, la roténone interfère avec le complexe I de la chaîne respiratoire des mitochondries[27].
S'il présente des analogies structurales avec le MPP+, le paraquat agit sur la physiologie cellulaire différemment. C'est une molécule chargée ne pouvant pas passer la barrière hémato-encéphalique ; elle utilise pour cela les transporteurs des acides aminés neutres[28]. Un mécanisme de transport dépendant du sodium () lui permettrait ensuite de pénétrer dans les neurones[28]. Au niveau cytosolique, le paraquat génère un stress oxydatif important en inhibant, notamment, le recyclage du glutathion[15]. De plus, lors d'une exposition chronique, l'exposition initiale au paraquat déclencherait une réponse de la microglie prédisposant les cellules dopaminergiques à la neurodégénérescence lors des expositions suivantes[29]. La microglie est un type de cellule gliale macrophagique participant à la défense immunitaire et protégeant le système nerveux central. Ces cellules ont la capacité de déclencher une explosion oxydative visant à produire des dérivés réactifs de l’oxygène afin de dégrader les corps étrangers qu'elles phagocytent. Parmi ces dérivés oxydatifs, il y a l'ion superoxyde (O2•–) généré à partir du coenzyme NADPH par la NADPH oxydase. Le paraquat génère un stress oxydant toxique en activant la NADPH oxydase[30]. Le paraquat agirait également en induisant un phénomène d'apoptose via l'activation de Bax et Bak (en), deux protéines de la famille Bcl-2[31].
Chez la souris, l'injection systémique de paraquat permet de modéliser la maladie de Parkinson en induisant une diminution du nombre de neurones dopaminergiques dans la substance noire ainsi qu'une altération de l'activité ambulatoire[32]. Par ailleurs, ce composé augmente l'expression de l'alpha-synucléine, ainsi que son taux d’agrégation, dans les neurones de la substance noire[33]. L'agrégation de l'α-synucléine sous forme de structures appelées corps de Lewy étant une des caractéristiques de la maladie de Parkinson, ces résultats suggèrent une influence de ce pesticide dans la physiopathologie de la maladie. Enfin, la sensibilité au paraquat augmente avec l'age[34].
Bien que le mode d'exposition et les doses utilisées dans les modèles expérimentaux soient, à juste titre, discutés, la recherche s'oriente de plus en plus vers l'effet que pourraient avoir de faibles doses lorsque différents composés chimiques sont mélangés (effet "cocktail")[35] ou lors de périodes de vulnérabilité accrue comme le développement[36] ; conditions qui, en définitive, sont plus proches de la réalité de l'exposition vécue par l’être humain. Il a été ainsi mis en évidence que l'effet du paraquat pouvait être exacerbé lorsqu'il était combiné avec un dithiocarbamate, composé utilisé comme additif pour les pesticides[37]. Paraquat et manèbe ont ainsi un effet synergique sur les atteintes du système dopaminergique et sur l'activité motrice. Par ailleurs, il a été mis en évidence que l'exposition néo-natale, chez la souris, à de faibles doses de paraquat conduisait chez l'adulte à des altérations de la motricité et du métabolisme dopaminergique, spécifiquement dans le striatum. De plus, les atteintes de la motricité s'aggravaient avec le vieillissement[38].
L'exposition au paraquat a permis de mettre au point d'autres modèles animaux de la maladie de Parkinson induits par un facteur environnemental. Chez la mouche, l'ingestion orale de paraquat induit des déficits moteurs, un diminution de l'espérance de vie et une perte des neurones dopaminergiques, de manière spécifique. Ces troubles peuvent être atténués, tout comme chez l'humain, par l'ingestion de L-DOPA[39].
L’Union européenne avait - à la demande notamment de la France, qui l'utilisait dans les bananeraies et sur luzerne, et du Royaume-Uni où il est fabriqué - autorisé le paraquat en 2003 en l'inscrivant à l’annexe I de la directive 91/414/CEE par la directive 2003/112/CE. Cette autorisation de mise sur le marché a été décidée en dépit de sa toxicité pour l'Homme et l'environnement.
La Suède, soutenue par le Danemark, l’Autriche, et la Finlande, a alors saisi la commission européenne. Après trois ans d'investigations complémentaires, le verdict devait être annoncé au printemps 2007. Ce n'est que le que le Tribunal de première instance des Communautés européennes, par l'arrêt arrêt T-229/04, a finalement annulé[40] la directive 2003/112/CE autorisant l'usage du paraquat dans les États-membres, considérant qu’il n’avait pas suffisamment été tenu compte du lien entre le paraquat et la maladie de Parkinson, ainsi que d'autres effets de la substance sur la santé des travailleurs et des animaux sauvages. Un nouvel effet délétère de faibles doses a été publié en 2007, sur les cellules souches du système nerveux central (de même que de faibles doses de plomb, de mercure)[13].
Sur le plan de la réglementation des produits phytopharmaceutiques :
Bien que son usage soit interdit dans l'Union européenne, sa production se poursuit et les populations européennes pourraient continuer à y être exposées de manière indirecte. En effet, différentes entreprises localisées en Europe vendent chaque année plusieurs centaines de tonnes de paraquat aux entreprises agricoles brésiliennes. Ces dernières renvoient ensuite leur production agricole, potentiellement contaminée par ce même pesticide, vers les pays européens[41],[42]. En 2017, la France et la Suisse furent épinglées pour leur exportation de ce pesticide interdit sur leurs territoires vers des tiers[43].
Face à la recrudescence des empoisonnements mortels, l'Agence de protection de l’environnement des États-Unis (EPA) envisage dans les années 1970 de retirer l'autorisation. Pour régler ce problème, Imperial Chemical Industries ajoute, en 1976 un vomitif (PP796), au paraquat. Cependant, le coût du PP796 étant élevé, l'entreprise fausse les résultats de ses recherches pour introduire une dose cinq à dix fois inférieure à celle nécessaire pour générer les vomissements à même d'éviter l'empoisonnement. Les empoisonnements demeurent (1200 morts au Japon pour la seule année 1986) et dans les pays où la réglementation veut interdire le paraquat (Suède, Grande Bretagne, Japon), ICI introduit des versions avec un ratio plus élevé de PP796. Elle choisit délibérément de ne pas généraliser ces mesures pour protéger les bénéfices (le pesticide représente 30 % du profit en 1987). ICI devient Zeneca en 1993, puis Syngenta en 2000 fournit les données faussées à la Commission européenne pour obtenir son autorisation sur le marché unique. Jon Heylings qui a travaillé pour ICI entre 1986 et 2008 lance l'alerte auprès de l'EPA en 2019 pour dénoncer les choix de l'entreprise qui aurait selon lui privilégié sciemment les bénéfices économiques à la santé et à la vie de milliers de personnes[4].
.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.