La synapse (du grec σύναψις / súnapsis, « contact, point de jonction », dérivé de συνάπτω / sunáptô, « joindre, connecter ») est une zone de contact fonctionnelle qui s'établit entre deux neurones, ou entre un neurone et une autre cellule (cellules musculaires, récepteurs sensoriels…). Elle assure la conversion d'un potentiel d'action déclenché dans le neurone présynaptique en un signal dans la cellule postsynaptique. On estime, pour certains types cellulaires (par exemple cellule pyramidale, cellule de Purkinje…), qu'environ 40 % de la surface membranaire est couverte de synapses.

On distingue habituellement deux types de synapses :
- la synapse chimique, très majoritaire, qui utilise des neurotransmetteurs pour transmettre l'information ;
- la synapse électrique où le signal est transmis électriquement par l'intermédiaire d'une jonction communicante (en anglais gap-junction).
On les distingue au microscope électronique par la taille de la fente synaptique ; de l'ordre de 2 nanomètres pour les synapses électriques, entre 10 et 40 nm pour les synapses chimiques. On peut également, dans le cas des synapses électriques, observer les jonctions communicantes. Au niveau d'une synapse, il s'agit toujours d'un contact entre deux membranes plasmiques, il n'y a jamais fusion en un syncytium.
Historique
Le mot « neurone » est utilisé pour la première fois par Waldeyer pour désigner les cellules nerveuses et un premier pas vers la compréhension de leur mode de fonctionnement a lieu à la fin du XIXe siècle lorsque Camillo Golgi met au point une technique de coloration par imprégnation argentique permettant une visualisation optimale du neurone et de ses prolongements.
Par la suite, Santiago Ramón y Cajal utilise la méthode de coloration de Golgi pour étayer la théorie du neurone. Le terme de « synapse », quant à lui, est proposé en 1897 par le physiologiste et Prix Nobel britannique Sir Charles Scott Sherrington pour désigner le point de contact entre deux neurones. Toutefois, Golgi est lui-même opposé à l'hypothèse selon laquelle le système nerveux pouvait être composé d'unités discontinues. En 1906 Golgi et Cajal reçoivent conjointement le Prix Nobel de médecine et physiologie, pour deux théories de l'organisation du tissu neuronal (neuronisme et réticularisme). Les travaux de Bernard Katz sur la théorie chimique de la neurotransmission au niveau de la plaque motrice et ceux de John Carew Eccles au niveau du système nerveux central des mammifères en 1951 ont démontré par la suite que les synapses électriques sont très rares et l'on admet aujourd'hui que le système nerveux est constitué majoritairement d'unités contiguës (thèse neuroniste)[1].
Synapse chimique
La synapse chimique est la plus fréquente des synapses du système nerveux. Ce type de synapse transmet le signal nerveux d'un neurone à un autre en utilisant un neurotransmetteur qui est émis par le neurone afférent, diffuse dans la fente synaptique et se lie aux récepteurs postsynaptiques.
Dans certaines synapses les cellules gliales jouent un rôle particulièrement actif, notamment en effectuant la recapture du neurotransmetteur (ex. : glutamate). Dans les synapses motrices, une enzyme, la cholinestérase, dégrade le neurotransmetteur dans la fente synaptique.
Morphologie
Il existe deux morphologies de synapses chimiques : la synapse en bouton et la synapse « en passant ». Toutes deux fonctionnent de la même façon et on y retrouve les mêmes composants. La synapse en bouton se situe à l'extrémité de la fibre nerveuse alors que les synapses en passant sont réparties régulièrement le long de l'axone.
Il existe un grand « bestiaire » de synapses chimiques selon le type de neurone, la localisation, etc. Le calice de Held dans le tronc cérébral auditif, par exemple, est un cas de synapse géante qui entoure quasi complètement la cellule postsynaptique.
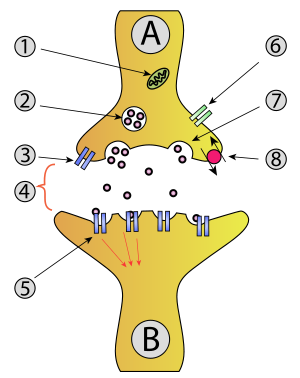
La synapse est constituée de trois parties : l'élément présynaptique, l'élément postsynaptique, séparés par l'espace intersynaptique.
- L'élément présynaptique se présente sous forme d'un renflement de l'axone, rempli de vésicules de forme variée (les vésicules synaptiques) contenant le neurotransmetteur. On y trouve aussi un appareil de Golgi très développé et de nombreuses mitochondries, signe d'une activité de synthèse intense. En effet, les neurotransmetteurs sont en partie synthétisés sur place.
- L'élément postsynaptique, lui, est totalement dépourvu de ce type de vésicule, mais il contient quelques mitochondries nécessaires au fonctionnement de la synapse. Dans certains cas la membrane est plus épaisse (densité postsynaptique), ce qui caractérise les synapses asymétriques, généralement glutamatergiques.
- L'espace intersynaptique (ou fente synaptique) est la zone qui sépare les membranes des deux neurones. Elle est de petite dimension (quelques dizaines de nanomètres) et dépourvue de lame basale (contrairement à la plaque motrice).
Transmission de l'influx nerveux
L'influx nerveux est transmis le long de l'axone sous la forme d'une séquence de potentiel d'action. Au niveau d'une synapse chimique, l'information change de nature : elle est transmise par une libération de neurotransmetteurs dans l'espace synaptique. Les trains d'onde de dépolarisation supportés par des courants électrochimiques (les potentiels d'action), sont codés par concentration de neurotransmetteur dans la fente synaptique.
Pendant longtemps, le credo a fait force de loi : un neurone, un neurotransmetteur. On sait aujourd'hui qu'un neurone peut libérer plusieurs neurotransmetteurs au niveau de la synapse, en général un transmetteur principal associé à un ou plusieurs neuropeptides [2]. Le transmetteur principal peut même évoluer. Certains neurones orthosympathiques (noradrénergiques), par exemple, peuvent libérer de la sérotonine à la suite d'une lésion.
Évènements présynaptiques : la libération des neurotransmetteurs
Il faut d'emblée différencier les neurotransmetteurs peptidiques et non peptidiques. Les neurotransmetteurs peptidiques sont produits par le neurone à partir d'acides aminés précurseurs présents dans le sang. Une grande partie de leur synthèse a lieu dans le péricaryon, en suivant le schéma classique de toute production protéique (Transcription de l'ADN en ARNm, lecture et traduction de l'ARNm par un ribosome sur le réticulum endoplasmique) puis transport antérograde rapide le long du cytosquelette de l'axone dans des vésicules provenant du bourgeonnement de l'appareil de Golgi. Une étape de maturation a lieu dans les vésicules golgiennes (clivages des extrémités N-ter et C-ter par des exopeptidases, clivage dans le peptide par des endopeptidases, amidation sur des acides aminés glycine, acétylation…). Les vésicules sont ensuite accumulées près de l'extrémité présynaptique, dans l'attente d'une dépolarisation.
Les neurotransmetteurs non peptidiques sont produits à partir d'acides aminés (catécholamines comme l'adrénaline ou la noradrénaline à partir de la tyrosine, le GABA (Gamma AminoButyric Acid)…), de lipides (THC pour TetraHydroCannabinol), etc. Ils sont produits dans le cytoplasme du neurone ou de la cellule excitable et sont activement pompés (par des enzymes utilisant l'ATP ou ATPases) dans des vésicules issues des endosomes ou d'une endocytose.
Le changement de polarité de membrane provoqué par l'arrivée d'un potentiel d'action (PA) au niveau d'une synapse déclenche l'ouverture de canaux calcium membranaires dépendants du voltage (VOC = Voltage Operated Channels). L'augmentation de la concentration en calcium intracellulaire qui en résulte provoque la fusion de la membrane vésiculaire avec la membrane plasmique et la libération des neuromédiateurs. Ce phénomène s'appelle l'exocytose. La biologie cellulaire a montré que cette exocytose était assurée par un complexe appelé SNARE composé principalement de 3 protéines :
- VAMP (aussi appelée synaptobrévine), insérée dans la membrane plasmique de la vésicule ;
- la syntaxine arrimée à la membrane plasmique de la cellule ;
- SNAP 25 arrimée dans la membrane plasmique.
Lors d'une dépolarisation ouvrant des VOC au calcium (VOC Ca++), une brusque entrée de calcium précipite la fusion de VAMP avec SNAP 25 et la syntaxine, ce qui arrime la vésicule à la membrane plasmique. La modification tridimensionnelle de ce complexe ternaire conduit à la fusion de la vésicule avec la membrane et à la libération du neurotransmetteur dans la fente synaptique. La fusion opérée par les SNAREs est considérablement accélérée par la présence dans la membrane des vésicules synaptiques de la synaptotagmine, qui est aujourd'hui considérée comme le détecteur de l'influx calcique grâce à ces deux domaines liant le calcium (C2A et C2B).
Trois mécanismes peuvent arrêter l'exocytose et donc faire cesser la libération de neurotransmetteur dans la fente synaptique :
- l'ouverture de canaux potassium, qui ramènent le potentiel de membrane à sa valeur d'origine et inhibent ainsi les canaux dépendants du potentiel ;
- des pompes calciques, situées sur le réticulum et la mitochondrie, qui captent les ions calcium entrés dans la cellule, ce qui fait cesser le signal calcique ;
- disparition des vésicules synaptiques chargées en neurotransmetteur capable de fusionner avec la membrane (fatigue synaptique).
Ces trois mécanismes expliquent en partie l'existence de la plasticité synaptique à plus ou moins long terme, mise en évidence par des chercheurs comme le britannique Geoffrey Raisman en particulier.
Diffusion des neurotransmetteurs dans la fente synaptique
Les neurotransmetteurs libérés dans la fente synaptique atteignent la membrane postsynaptique par simple diffusion. Avec le délai nécessaire pour provoquer l'exocytose, c'est l'étape qui nécessite le plus de temps dans la transmission synaptique. Dans le cas de la plaque motrice, la concentration en acétylcholine dans la fente atteint une concentration de 100 mmol/l 10 µs après sa libération. Elle mettra environ 100 µs pour revenir à une concentration proche de zéro. Cette disparition du neurotransmetteur de la fente synaptique peut impliquer un recaptage ou une hydrolyse par une enzyme spécialisée. Le codage de l'information étant fréquentiel, il est important de faire cesser l'excitation le plus vite possible.
Évènements postsynaptiques : l'activation des récepteurs membranaires
Les neurotransmetteurs se fixent sur des récepteurs de la membrane postsynaptique. Il en existe deux sortes :
- les récepteurs ionotropes qui sont des protéines-canal s'ouvrant pour générer un courant ionique ;
- les récepteurs métabotropes sont couplés aux protéines G et sont des transducteurs de signal régulant des seconds messagers dans le cytoplasme. Les seconds messagers peuvent s'associer à une protéine-canal ou bien provoquer une cascade de réactions. Parmi les voies métaboliques activées par ces seconds messagers, des facteurs de traduction de l'ADN sont impliqués, ce qui influence le pool de gènes exprimé par la cellule, et donc pourraient être impliqués dans le phénomène de plasticité synaptique à long-terme (LTP) et la mémorisation. Cette voie est beaucoup plus lente que la première.
On assiste alors à une réponse physiologique locale appelée potentiel générateur, potentiel gradué (PG) ou potentiel postsynaptique. On caractérise deux types de potentiel postsynaptique :
- le potentiel postsynaptique excitateur (ou PPSE) diminue la différence de potentiel entre les deux côtés de la membrane plasmique. Autrement dit le PPSE dépolarise localement la membrane ;
- le potentiel postsynaptique inhibiteur (ou PPSI) augmente la différence de potentiel. Elle hyperpolarise la membrane.
Si la membrane dépasse le seuil critique de dépolarisation, un potentiel d'action est initié. Les PPSI empêchent le déclenchement d'un potentiel d'action alors que les PPSE le favorisent.
En général, un neurone est couvert de synapses excitatrices et de synapses inhibitrices. Il se produit alors une sommation à la fois temporelle et spatiale des entrées synaptiques pour « décider » du déclenchement ou non d'un potentiel d'action. En fait les dendrites ont peu de canaux sodiques dépendants du voltage, responsables du déclenchement du potentiel d'action. Il est donc rare qu'un potentiel d'action y soit déclenché. Les potentiels postsynaptiques se propagent le long des dendrites jusqu'au péricaryon. À la jonction du péricaryon et de l'axone se trouve une région particulièrement riche en canaux sodiques dépendants du voltage, il s'agit du cône d'initiation. C'est au niveau du cône d'initiation que sont générés le plus souvent les potentiels d'actions qui se propageront ensuite le long de l'axone vers d'autres synapses…
Le potentiel d'action, une fois initié, a toujours la même amplitude et le même décours temporel. Sa valeur informative ne dépend pas de l'importance de la dépolarisation qui l'a initié. C'est cela qu'on appelle la loi du tout ou rien. Si la dépolarisation continue suffisamment longtemps après le déclenchement du potentiel d'action, un autre potentiel d'action peut être initié. Les potentiels d'action codent l'information en fréquence.
Plusieurs molécules étant libérées lors de la transmission synaptique et plusieurs types de récepteurs pour le même neurotransmetteur pouvant être présents sur la même membrane postsynaptique, plusieurs effets peuvent avoir lieu simultanément. C'est par exemple le cas de nombreuses synapses GABAergiques qui présentent un PPSI rapide dû aux récepteurs ionotropes GABAA et un PPSI lent dû aux récepteurs métabotropes GABAB.
Arrêt de la stimulation nerveuse
Pour éviter que la stimulation du neurone postsynaptique ne se prolonge, deux systèmes éliminent la molécule de l'espace intersynaptique :
- la dégradation, qui met en jeu des enzymes spécifiques qui vont métaboliser le neurotransmetteur, mettant fin à son effet sur le neurone postsynaptique exemple la MAO issue des synthèses mitochondriales ;
- la recapture, pendant laquelle le neurotransmetteur ou ses précurseurs issus de la dégradation enzymatique est récupéré par le neurone présynaptique, ou par la cellule gliale avoisinante, pour être réutilisé ou détruit.
En général les deux sont associés. Dans le cas de l'acétylcholine, une dégradation limitée est suivie d'une recapture de la choline qui sera utilisée pour resynthétiser l'acétylcholine.
Influence des substances psychoactives
Les substances psychoactives sont des drogues, des médicaments, etc., qui modifient les perceptions sensorielles, les sensations, l'humeur… Elles ont comme principal mode d'action de modifier le passage des neurotransmetteurs.
Comme pour les neurotransmetteurs, il existe plusieurs modes d'action possibles à ces drogues, dont :
- se lier aux récepteurs sans entraîner d'effet (effet antagoniste). Les récepteurs ne sont alors plus disponibles pour lier l'agoniste (neurotransmetteur) ;
- empêcher ou limiter la sortie ou la destruction de neurotransmetteurs, qui active davantage et plus longtemps le récepteur (exemple de la fluoxétine).
Les conséquences à long terme sont de modifier la réceptivité de la synapse, par exemple en modifiant le nombre de récepteurs, en réaction de défense, ce qui entraîne l'accoutumance et la dépendance.
Jonction neuromusculaire
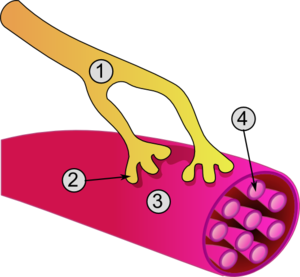
Lors du réflexe myotatique CF réflexe de flexion, l'élément présynaptique rencontre la plaque motrice de la fibre musculaire qui est composée d'une membrane plasmique appelée sarcolemme faisant office d'élément postsynaptique et contenant plusieurs centaines de myofibrilles. La jonction neuromusculaire est historiquement très importante puisque ce sont les observations sur le muscle extenseur de la patte de grenouille qui ont donné naissance à l'électrobiologie qui eut un retentissement rapide auprès du grand public, comme en témoigne l'engouement de l'époque pour les phénomènes électriques.
 | 
|
Vue détaillée d'une jonction |
L'acétylcholine intervient dans la contraction musculaire lors des réflexes de flexion ou d'extension au niveau de la jonction neuromusculaire. Les neurones la produisant s'appellent neurones cholinergiques. Ses précurseurs sont la choline d'origine alimentaire qui est captée par la terminaison présynaptique dans le sang et l'acétylcoenzyme A d'origine mitochondriale. Ils sont synthétisés par l'enzyme choline-acétyltransférase (CAT) qui les transforment en acétylcholine. Ces neuromédiateurs sont alors enveloppés par des vésicules provenant du bourgeonnement de l'appareil de Golgi et sont transportés jusqu'au renflement (ou bouton) synaptique. Au niveau présynaptique il y a non pas un seul renflement mais des centaines afin d'assurer une surface de contact plus large, on parle d'arborisation terminale.
Sous l'effet du calcium, les vésicules chargées de neuromédiateurs fusionnent avec la membrane plasmique, déversant leur contenu dans la fente synaptique (exocytose). Les neuromédiateurs se fixent alors sur des récepteurs spécifiques de la plaque motrice du muscle squelettique ce qui a pour conséquence de provoquer sa contraction. L'excès de neuromédiateur est ensuite dégradé par une enzyme : acétylcholinestérase (ACHE) qui libère de l'acide acétique et de la choline qui pourra être ensuite recapturée par les récepteurs de l'axone présynaptique et recyclé.
Synapse électrique
Dans la synapse électrique, les membranes des deux neurones sont reliées par des jonctions communicantes, parfois appelées également nexus (GAP junctions). Les ions se transmettent donc d'une cellule à une autre, ainsi que la dépolarisation membranaire associée. L'influx nerveux se transmet sans intervention de neurotransmetteur. Ce type de synapse, qui joue un rôle important dans le système nerveux immature, est ensuite relativement rare au stade adulte et est majoritairement retrouvé chez les invertébrés. Ce type de communication est très fréquent dans les épithéliums.
Classification
Au niveau du soma (le soma ou « corps cellulaire » ou péricaryon, est la partie centrale d'un neurone)
- Synapse axo–somatique simple
- Synapse axo–somatique invaginée
- Synapse axo–somatique épineuse
- Synapse axo–dendritique simple, (accolement des 2 membranes)
- Synapse axo–dendritique épineuse (synapse sur le bourgeon des épines dendritiques)
- Synapse à crête (sur le côté du bourgeon dendritique)
- Synapse épineuse ramifiée
- Synapse axo–dendritique « en passant »
- Synapse axo–dendritique réciproque
- Terminaison poly–synaptique
- Synapse épineuse interdigité
Au niveau du cône d’implantation et de l’axone
- Synapse axo–axonique proximale
- Synapse axo–axonique inhibitrice
- Synapse axo–axonique distale
- Synapse axo–axonique « en passant »
Les terminaisons dendritiques sont super mobiles.
Intégration du signal : zoom sur l'élément postsynaptique


Les synapses sont regroupées selon deux catégories selon les effets qu'elles engendrent : excitatrices ou inhibitrices. Le principal neuromédiateur inhibiteur du cerveau est le GABA qui se fixe sur les canaux récepteurs GABAA dont l'ouverture provoque un influx d'ions chlorure et donc une hyperpolarisation de la membrane. Il existe une plus grande diversité de récepteurs ionotropes excitateurs, par exemple les récepteurs au glutamate ou à l’acétylcholine. L'élément postsynaptique possède en général ces deux catégories de récepteurs ainsi que des canaux sodium ou calcium activés par dépolarisation. Il réalise une sommation temporelle des signaux excitateurs (PPSE, potentiel postsynaptique excitateur) et inhibiteurs (PPSI, potentiel postsynaptique inhibiteur). Il propagera le potentiel d'action à la condition que la somme des excitations soit supérieure à la somme des inhibitions et si un seuil de dépolarisation est atteint. Ce seuil correspond au voltage auquel un nombre suffisant de canaux sodium sont activés.
La sommation spatiale se réfère aux différentes synapses afférentes à l'élément postsynaptique. Un neurone peut en effet recevoir plus d'un millier d'afférences différentes mais il ne peut réagir que d'une seule manière : conduction ou absence de conduction. Si le résultat de la somme algébrique de tous les éléments afférents est supérieure à une valeur seuil, aux environs de -15 mV dans le schéma ci-contre, le neurone intégrateur sera le siège d’un potentiel d’action.
Une sommation dite temporelle a aussi lieu au niveau de l’élément postsynaptique. Elle est due à la vitesse d'entrée des ions à l'intérieur de la cellule. Si beaucoup de PPSE sont rapprochés dans le temps, ils s'ajoutent et peuvent également atteindre le seuil de dépolarisation et donner lieu à un potentiel d’action.
Un dernier élément d’intégration est dû à l’existence de la période réfractaire du neurone. Si deux signaux afférents excitateurs sont espacés de moins d'une milliseconde, le second ne donnera naissance à aucun PPSE et sera donc silencieux.
Pathologie
L'anomalie de fonctionnement de la synapse neuro-musculaire est responsable d'une maladie neuromusculaire nommée myasthénie.
Synapses, génétique, fonctionnement du cerveau et autisme
Il existe de nombreuses formes d'autisme, longtemps considérées comme d'origine non-organique, souvent multifactorielles et pour partie environnementale, mais toujours liées à une organisation et un fonctionnement atypique du cerveau. On connait aussi de nombreuses formes de déficience mentale (DM), associées ou non à des anomalies physiologiques du cerveau. Assez souvent l'autisme peut être associé à une déficience mentale, mais aussi à des capacités intellectuelles accrues dans certains domaines (cas du syndrome d'Asperger)[3].
Les données épidémiologiques ont peu à peu suggéré l'implication de causes génétiques directes et indirectes, ainsi que de facteurs génétiques et épigénétiques dans l'apparition des TSA, au moins dans un grand nombre de cas[4]. Il en va de même pour divers types de retard mental[4]. Depuis 2003, la présence de mutations génétiques (se transmettant selon le modèle mendélien) affectant la formation, la maturation et le fonctionnement des synapses en lien avec l’étiologie de l’autisme est avérée. Ces gènes mutés concernent au moins la synapse glutamatergique et probablement l'astrocyte qui lui est associé[3].
Certains des gènes identifiés codent des protéines particulièrement impliquées dans la structure de connexion des neurones (synapses)[3]. Parmi les premiers gènes trouvés impliqué dans des anomalies, chez des personnes avec autisme ou syndrome d’Asperger, des synthèses et fonctions de certaines protéines synaptiques, selon le consortium international Autism Genome Project[5], figurent NLGN3 et NLGN4, situés sur le chromosome X et codant les Neuroligines 3 et 4 et ; mais aussi SHANK3 et NRXN1 codant des neurexines[6],[7], protéines associées à l'autisme au début des années 2000[8],[9],[10],[11],[12]. Le rôle spécifique et précis de ces gènes dans le dysfonctionnement du cerveau apparait complexe et encore mal compris, de même pour les interactions gène-environnement, car les TSA montrent une variabilité phénotypique et une hétérogénéité génétique très élevées[13] ; certaines neurexines peuvent aussi être impliqués dans la schizophrénie (parfois associée au Syndrome d'Asperger ou à d'autres TSA)[14].
On sait aussi que la glie contribue à la physiopathologie des TSA. Non seulement le cellules gliales « collent » les neurones entre eux, mais elles participent activement à la neurogenèse, à la myélinisation, à la synaptogenèse, au contrôle de l'inflammation et à la gestion du glutamate, entre autres choses[15]. Gzielo et Nikiforuk (2021) plaident pour que le rôle des cellules astrogliales et les interactions mutuelles entre neurones et astrocytes soient mieux étudié, car il semble que « les signes de dysfonctionnement astroglial, mais aussi oligodendroglial et microglial observés dans le cerveau autistique montrent que la gliopathologie peut être une cause de survenue de TSA »[16].
Ayant observé qu'un même dysfonctionnement de certaines synapse du cerveau correspond à plusieurs types de déficience mentale (DM) d’origine génétique, des chercheurs ont recherché d'éventuelles causes génétiques communes entre DM et autisme ; ils ont trouvé que plusieurs gènes semblent indifféremment être des gènes « d’autisme » ou de « DM » (ex. : gène NLGN4X, l'un des 5 gènes codant pour la Neuroligine et qui est retrouvé muté dans les cas de syndrome d’Asperger, mais aussi chez les autistes non retardés ou retardés, ainsi que chez des sujets retardés sans troubles du spectre autistique)[3].
Selon Perche & al (2010), « il existe donc un continuum génétique entre autisme et troubles apparentés, d’une part, et avec les DM d’autre part »[3].
Depuis les années 2010, plusieurs études et revues de la littérature montrent ou confirment qu'il existe aussi des facteurs épigénétiques[17],[18],[19],[20], affectant notamment les liaisons synaptiques[21]. La régulation épigénétique est un mécanisme moléculaire, notamment basé sur la méthylation, connu pour être sources de troubles neurodéveloppementaux. Ses liens avec l'environnement pourraient expliquer l'apparente augmentation des TSA, via des polluants et/ou médicaments affectant la génétique des spermatozoïdes, des ovules ou de l'embryon ou du jeune enfant en développement[22]. L'alimentation de la mère pourrait à la fois être source de molécules épigénétiquement délétères et de molécules susceptibles d'avoir des effets épigénétiques positifs liées aux TSA[22] (acide folique par exemple).
Niveau synaptique
La structure des organismes biologiques qui constituent la biosphère peut être décomposée en plusieurs niveaux d'organisation : atomique, moléculaire, cellulaire, tissulaire, organique, des appareils, et enfin celui de l'organisme dans sa totalité fonctionnelle.
L'étude scientifique du vivant se fait par des recherches sur les éléments de chacun de ces niveaux, puis par la compréhension des interactions entre ces différents niveaux (voir l'article « Méthode scientifique »).
L'étude du niveau synaptique permet de comprendre les caractéristiques de la transmission des signaux bioélectriques et chimiques, entre les neurones eux-mêmes ou entre les neurones et certains éléments de l'organisme (cellule sensorielle, muscle lisse ou strié…). La compréhension de la transmission des signaux neuraux est une nécessité incontournable car ce mécanisme est fondamental dans le fonctionnement du système nerveux.
Recherche et développement, prospective
Des travaux de recherche portent sur la création de synapses artificielles bioinspirées (neuroinspirées plus précisément)[23].
Notes et références
Annexes
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.