Loading AI tools
type de liaison chimique De Wikipédia, l'encyclopédie libre
Une liaison σ (prononcé sigma) est une liaison chimique covalente formée par le recouvrement axial de deux orbitales atomiques[1]. Dans une molécule diatomique homonucléaire, la densité électronique est maximum le long de l'axe internucléaire, lequel n'est intersecté par aucun plan nodal. De telles liaisons peuvent résulter du recouvrement d'orbitales s + s, pz + pz, s + pz ou dz2 + dz2, où z est l'axe internucléaire[2]. Dans ces molécules, le concept de liaison σ est équivalent à celui d'orbitale moléculaire σ. Dans cette dernière, la densité électronique est distribuée selon une symétrie circulaire autour de l'axe interatomique. Plus généralement, les liaisons σ se forment par recouvrement axial d'orbitales atomiques, ce qui fait qu'une molécule d'alcane comme le propane C3H8 est unie par dix liaisons σ, à savoir huit liaisons C–H et deux liaisons C–C.
| —— | ———————————————— | ————— |
Orbitales atomiques | 
| |
| Liaisons σ entre orbitales atomiques s–s et p–p | Liaison π pour comparaison | |
| —— | ———————————————— | ————— |
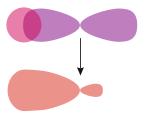 Fluorure d'hydrogène HF | 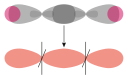 Acétylène HC≡CH | |
Les liaisons σ sont les liaisons covalentes les plus fortes car le recouvrement axial est plus important que le recouvrement latéral d'une liaison π ou d'une liaison δ. Il ne peut exister qu'une seule liaison σ entre deux atomes. Une liaison simple est généralement une liaison σ, tandis qu'une double liaison est généralement formée d'une liaison σ et d'une liaison π et qu'une triple liaison est typiquement constituée d'une liaison σ et de deux liaisons π. L'énergie de dissociation de la liaison C–C de l'éthane H3C–CH3 vaut 347 à 377 kJ/mol, tandis que celle de l'éthylène H2C=CH2 vaut 710 kJ/mol et celle de l'acétylène HC≡CH vaut 960 kJ/mol[3], illustrant qu'une liaison σ est plus forte que des liaisons π.
Les complexes de métaux de transition qui présentent des liaisons multiples, comme les complexes de dihydrogène, ont des liaisons σ entre les atomes unis par des liaisons multiples. Ces liaisons σ peuvent être complétées par d'autres interactions telles que des rétrocoordinations π, comme dans le cas de W(CO)3(PCy3 (en))2(H2) ou encore des liaisons δ, comme dans le cas de l'acétate de chrome(II) Cr2(CH3CO2)4(H2O)2[4].
Les molécules organiques présentent souvent des combinaisons de liaisons σ et de liaisons π dans des composés qui peuvent être cycliques ou à chaîne ouverte. Le nombre Nσ de liaisons σ de telles molécules peut être déduit par analogie avec la caractéristique d'Euler en considérant que les atomes sont des sommets, les liaisons σ des arêtes, et les cycles des faces :
Cette formule fonctionne bien pour les molécules qui peuvent être représentées de manière bidimensionnelle : le méthane CH4 contient ainsi quatre liaisons σ, l'éthane C2H6 en contient sept (six liaisons C–H et une liaison C–C), l'hexane C6H14 en contient 19, le cyclohexane C6H12 en contient 18, le benzène C6H6 en contient 12, le naphtalène C10H8 en contient 19, etc. Dans certains cas, il peut s'agir d'une liaison σ virtuelle, comme pour le carbone diatomique C2 uni seulement par deux liaisons π mais qui contient également une liaison σ annulée par une orbitale σ* antiliante.
Cette formule atteint ses limites avec des composés plus complexes dont la géométrie ne peut être représentée simplement dans un plan, ce qui modifie la caractéristique d'Euler. C'est par exemple le cas du buckminsterfullerène C60, qui contient 60 atomes, 32 cycles et 90 liaisons σ ; la formule donnerait, quant à elle, 60 + 32 – 1 = 91 liaisons σ.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.