Loading AI tools
acide aminé contenant du soufre De Wikipédia, l'encyclopédie libre
La cystéine (abréviations IUPAC-IUBMB : Cys et C), du grec ancien κύστις (« vessie »[5])[6], est un acide α-aminé dont l'énantiomère L est l'un des 22 acides aminés protéinogènes, encodé sur les ARN messagers par les codons UGU et UGC. Elle n'est pas considérée comme essentielle pour l'homme mais peut être produite en quantité insuffisante par l'organisme selon l'état de santé des individus — notamment dans le cas de certaines maladies métaboliques et de syndromes de malabsorption — ainsi que chez les enfants et les personnes âgées.
| Cystéine | |
 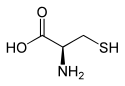 L ou R(+)-cystéine et D ou S(-)-cystéine |
|
| Identification | |
|---|---|
| Nom UICPA | acide 2-amino- 3-mercapto-propanoïque |
| Synonymes |
C, Cys |
| No CAS | (racémique) L ou R(+) D ou S(–) |
| No ECHA | 100.000.145 |
| No CE | 200-158-2 L 213-062-0 D |
| No E | E920 L |
| FEMA | 3263 L |
| Propriétés chimiques | |
| Formule | C3H7NO2S [Isomères] |
| Masse molaire[1] | 121,158 ± 0,009 g/mol C 29,74 %, H 5,82 %, N 11,56 %, O 26,41 %, S 26,47 %, |
| pKa | 1,91 8,14 10,28 |
| Propriétés physiques | |
| T° fusion | 240 °C |
| Solubilité | 280 g·L-1 dans l'eau (25 °C) |
| Propriétés biochimiques | |
| Codons | UGU, UGC |
| pH isoélectrique | 5,07[2] |
| Acide aminé essentiel | selon les cas |
| Occurrence chez les vertébrés | 3,3 %[3] |
| Précautions | |
| SIMDUT[4] | |
Produit non contrôlé |
|
| Directive 67/548/EEC | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Il s'agit d'un acide α-aminé naturel caractérisé par la présence d'un groupe sulfhydryle –SH formant un thiol ; la sélénocystéine et la tellurocystéine en sont des analogues dont l'atome de soufre est remplacé respectivement par un atome de sélénium et de tellure.
La cystéine est présente en petites quantités dans la plupart des protéines. Sa présence dans les protéines est très importante, notamment parce qu'elle permet la formation de ponts disulfure. Le groupe thiol est très fragile car il s'oxyde facilement. Son oxydation conduit à la cystine, qui consiste en deux molécules de cystéine unies par un pont disulfure. Un oxydant plus énergique peut oxyder la cystéine sur son soufre en donnant l'acide cystéique HO3S–CH2–CH(NH2)COOH, à l'origine de la taurine, produit de décarboxylation présent dans la bile sous forme de taurocholate.
Différentes réactions sont utilisées pour « protéger » les thiols des cystéines, ou pour réduire les ponts disulfures, en particulier :
Le blocage par alkylation est couramment utilisé lors de l'étude des protéines. Il utilise en particulier l'iodoacétamide conduisant à une carboxyamidométhylation :
La cystéine peut être prise comme complément alimentaire sous forme de N-acétylcystéine (NAC).
Elle a pu jouer un rôle important dans le développement de la vie sur terre[7].
La cystéine est autorisée comme additif alimentaire et porte le numéro E920.
L'acide L-cystéique et la L-cystéine peuvent être produits en quantités industrielles à partir de certains OGM, notamment Escherichia coli à partir de glucose et de sels minéraux[8], de plumes dissoutes dans de l’acide chlorhydrique ainsi que de cheveux humains, qui en contiennent davantage. Ce dernier mode de production a été interdit en France par un avis du Conseil supérieur d'hygiène publique de France par un avis daté du 8 juin 1999[9] « étant donné la recommandation générale du Comité scientifique de l’alimentation humaine s’opposant au recyclage intra-espèce » ; cette décision est cependant difficilement applicable car l'origine de la cystéine distribuée ne peut être facilement déterminée.
L'Autorité européenne de sécurité des aliments (EFSA) a autorisé, par une directive d'[10], l'emploi de L-cystéine dans les biscuits pour nourrissons et enfants en bas âge afin de prévenir les risques d'étouffement par émiettement des biscuits à faible teneur en matières grasses. Plus généralement, la cystéine permet aux pâtes de mieux retenir les gaz et de conserver durablement des formes volumineuses, ce qui favorise l'écoulement de ces produits chez les pâtissiers.
La cystéine intervient dans la synthèse de la mélanine, le pigment naturel de la peau et des cheveux.
Elle intervient aussi dans la synthèse du coenzyme A qui joue de nombreux rôles dans le métabolisme humain.
Et parce que ses résidus fixent les cations métalliques, elle semble impliquée dans certains processus de contamination[11], bioconcentration, et détoxication naturelle de l'organisme (chélation de métaux lourds ou métalloïdes toxiques[12])[12].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.