Loading AI tools
virus n'infectant que des bactéries De Wikipédia, l'encyclopédie libre
Les bactériophages, ou phages (mot formé des éléments bactério-, « bactérie », et -phage, « qui mange »), ou, plus rarement, virus bactériens, sont des virus qui n'infectent que des bactéries. Ils sont présents dans toute la biosphère. Ils sont particulièrement abondants dans les milieux riches en bactéries, et donc notamment dans les excréments, le sol et les eaux d'égout. Dans un millilitre d'eau de mer, on compte près de 50 millions de bactériophages[1]. Le support de l'information génétique (génome) des bactériophages peut être un ADN ou un ARN[2]. Parce que leur génome est entouré d’une capside, les phages font partie des virus dits complexes.

L'activité des bactériophages est découverte en 1897 par le biologiste français Félix D'Hérelle qui remarque des “trous” dans les cultures de bactéries qu’il développe pour lutter contre les essaims de sauterelles en Amérique centrale. Il n’en comprend le sens qu'en 1917, lorsqu'il fait la même observation dans des selles de malades atteints de dysenterie bacillaire (maladie du côlon). Il isole alors les premiers phages, puis développe les premières applications phagothérapeutiques[1].
En 1915, Frederick W. Twort, à Londres, remarque aussi que des colonies de microcoques prennent parfois un aspect vitreux, dû à la destruction des cellules bactériennes, et que cette caractéristique est transmissible à des colonies normales par simple contact.
Les phages sont des outils fondamentaux de recherche et d'étude en génétique moléculaire[1]. Ils servent notamment de vecteurs de clonage et de transfert de gènes (on parle aussi de transduction). Dans les années 1940-1960, les travaux effectués sur les bactériophages ont permis de nombreuses avancées dans le domaine de la biologie moléculaire (avancées portées par Max Delbrück, dans le cadre du « groupe phage ») et ont permis de découvrir que les acides nucléiques constituent le support de l'information génétique (expérience de Hershey-Chase, en 1952[3],[1]).
Les bactériophages sont utilisés en France à des fins thérapeutiques de 1920 à 1977 et le sont toujours dans certains pays de l'ex-bloc de l'Est, où l'on peut acheter des préparations bactériophagiques en pharmacie sans ordonnance[4]. Ils connaissent un retour en grâce depuis les années 2000, ce dont témoignent des publications désormais nombreuses et la création du Réseau Bactériophage France en 2016[5].
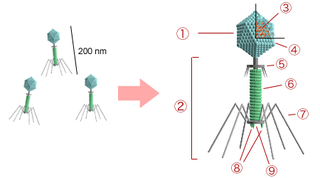
Comme les virus qui infectent les eucaryotes, un phage possède du matériel génétique encapsidé dans une structure protéique complexe constituée le plus souvent d'une tête et d'une queue. Pour plus de 95 % des phages connus, ce matériel est une molécule d'ADN double-brin d'une longueur de 5 à 650 kpb (kilo paire de bases) et leur dimension varie de 24 à 200 nm[réf. nécessaire]. Les bactériophages ayant un génome de plus de 200 kpb sont appelés « phages jumbo »[6].
On caractérise les phages par la présence de « plages de lyse ». L'infection d'une cellule bactérienne par un seul phage peut provoquer sa lyse au bout d'une vingtaine de minutes avec libération de quelques dizaines voire centaines de particules phagiques. En laboratoire, chaque particule ainsi libérée va infecter une nouvelle bactérie et recommencer le cycle lytique. Conséquence de ces lyses microscopiques en cascade, des « plages de lyse » se forment dans le tapis bactérien à la surface des géloses, permettant la lecture à l'œil nu des résultats de test. La taille et l'aspect de ces plages de lyse constituent un phénotype contribuant à caractériser les phages.
Les bactériophages, incapables de se reproduire par leurs propres moyens, injectent leur matériel génétique dans des bactéries hôtes. Grâce aux enzymes et aux ribosomes de l'hôte (et à certaines protéines virales selon les cas), le génome viral peut être répliqué et traduit pour former de nombreuses copies du virus qui sont libérés avec la lyse de la bactérie-hôte : on parle de cycle lytique ou cycle de production.
Certains bactériophages se comportent autrement, leur matériel génétique est répliqué et s'intègre au chromosome de la bactérie (ou existe sous forme de plasmide), mais n'est pas exprimé pour former des virions. Le virus est alors désigné sous le terme de prophage, lequel est transmis à la descendance de la bactérie infectée (lignée lysogénique) et on parle de lysogénie ou de cycle lysogénique. En réponse à une induction (ex. : stress de la bactérie), l'infection lysogénique bascule vers un cycle lytique.
D'une espèce à l'autre, le cycle de réplication des phages dans la cellule peut suivre plusieurs schémas :
Les phages, comme d'autres virus, sont vulnérables aux UV solaires, connus pour contribuer à détruire les virus, au moins dans le haut de la colonne d'eau, et plus ou moins profondément selon la turbidité de l'eau[8].
Dans les eaux plus eutrophes voire dystrophes, une autre cause de destruction virale (encore mal comprise) semble être la présence de molécules antivirales dissoutes, thermolabiles et de haut poids moléculaire (plus de 30 kDa), de type protéases ou autres enzymes bactériennes probablement[8] qui, lors d'expériences conduites par Noble & al. en 1997, semblent responsables d'environ 1/5 de la désintégration maximale des virus ; en complément du rayonnement solaire qui en élimine au maximum de 1/3 à 2/3 (quand il s'agit de virus non-natifs) et de 1/4 à 1/3 quand il s'agit de virus natifs) suggérant des phénomènes de co-évolution adaptation évolutive entre bactéries et virus, et en fonction du taux d'UV solaires pénétrant la colonne d'eau[8].
L’organisme responsable de la nomenclature et de la taxonomie des virus s’appelle l’International Committee on Taxonomy of Viruses (ICTV). On dénombre une vingtaine de morphologies différentes chez les virus bactériens actuellement reconnus par l'ICTV[1]. En 2000, plus de 5 000 bactériophages différents avaient été observés et décrits. Plus de 95 % d'entre eux possédaient une queue impliquée dans l'entrée de l'ADN du phage dans la cellule bactérienne (famille des Caudovirales). On distingue trois morphologies de queues différentes :
Depuis 2022, cette subdivision morphologique n'est plus à la base de la classification[9].
Comme les phages peuvent porter dans leur génome des gènes accessoires à leur cycle de vie, ils participent aux transferts horizontaux de gènes entre populations bactériennes. C'est la transduction. Lorsque ces gènes accessoires codent des facteurs de virulence, la bactérie infectée voit son pouvoir pathogène augmenté – c’est le phénomène de « conversion lysogénique ».
Un exemple bien connu est celui des gènes des toxines Stx des Escherichia coli entérohémorragiques (EHEC). Ces gènes stx sont localisés dans des séquences de bactériophages lambdoïdes intégrés dans le chromosome. Les EHEC auraient donc émergé par conversion lysogénique. On connaît de nombreux autres exemples de ce type, comme la toxine cholérique de Vibrio cholerae qui est portée par le phage CTX.
Les bactériophages lysogènes sont souvent intégrés dans le chromosome au niveau de locus codant des ARN de transfert (ARNt). Par exemple, le phage PhiR73 de Escherichia coli est inséré au niveau du locus selC. L'acquisition de gènes étrangers par transfert horizontal, grâce à des bactériophages s’intégrant au niveau de tels « points chauds » est plausible, puisque les séquences codant les ARNt sont hautement conservées entre les différentes espèces bactériennes. Enfin, la persistance des gènes de virulence dans les génomes phagiques suggère qu’ils confèrent un avantage sélectif, peut-être dû à la plus grande multiplication et diffusion de la bactérie hôte.

Dans les années 1960, les recherches menées sur les interactions hôte–phage par les biologistes américains Max Delbrück, Alfred Hershey et Salvador Luria valurent à ces chercheurs le prix Nobel de médecine-physiologie en 1969.
Les phages ont permis différentes découvertes :
L'étude des phages a des implications importantes en médecine et en génétique, en particulier pour la compréhension des infections virales, des anomalies génétiques, de l'embryologie humaine, des causes du cancer et de la résistance des bactéries aux antibiotiques.
Les phages sont utilisés de multiples manières en biologie moléculaire. Ils sont utilisés comme vecteurs de clonage pour insérer de l'ADN dans les bactéries. La méthode du phage display est une méthode qui permet la sélection d'un peptide grâce à sa présentation sur la surface de phages. Le phage display est une technique permettant la construction de banques d'ADN ou d'ADN complémentaire. Les 2 principaux phages utilisés dans cette technique sont les phages M13 (phage filamenteux) et lambda qui infectent tous les deux E. Coli. Prenons l'exemple du phage M13 qui est un phage filamenteux capable d'infecter uniquement les bactéries gram (-) ayant incorporé le facteur F et dont l'infection conduit à la lysogénie. Sa capside contient, entre autres, les protéines P8 et P3 nécessaires pour la liaison du bactériophage à la bactérie via les pilus sexuels. Ces 2 protéines vont être utilisées pour présenter à la surface des phages des molécules d'intérêt (peptide, fragment d'anticorps ou protéine entière): la molécule d'intérêt est fusionnée avec les protéines P8 et P3, par l'insertion du gène codant la molécule d'intérêt à proximité de l'extrémité 5' des gènes P3 et P8 en respectant le cadre de lecture. On utilise l'une ou l'autre des protéines selon le type de molécule et la quantité de molécules à exposer à la surface du phage. On distingue les phages polyvalents/homogènes, où toutes les protéines P3 et P8 sont fusionnées, des phages monovalents/hétérogènes où seulement une partie des protéines le sont. La technique permet d'obtenir des banques d'ADN que l'on peut facilement conserver et les clones sélectionnés sont multipliés à faible coût. Cette technique va permettre de produire des anticorps sans devoir passer par l'immunisation d'un animal. Limite de la technique: certaines molécules ne peuvent pas être exprimées comme les molécules toxiques pour la cellule hôte. Il y a donc une capacité limitée à transformer E. Coli.
Le séquençage d'un génome ne se fait pas d'un seul coup, mais petit à petit sur des fragments de génomes. Pour cela ces fragments d'ADN peuvent être stockés et multipliés dans des organismes servant de banque d'ADN. Les phages en tant que vecteurs de clonage le permettent.
Principalement utilisés dans l'agroalimentaire puis en médecine vétérinaire, les phages sont aussi étudiés en médecine comme alternative à la résistance aux antibiotiques[1]. En Hollande est également commercialisé un cocktail de phages pour lutter contre les contaminations de Listeria dans les produits alimentaires[11].
En 2006, aux États-Unis, une préparation bactériophagique à base de six virus bactériophages a été autorisée comme conservateur alimentaire, notamment pour lutter contre la listériose[12],[1].
Plus de la moitié des antibiotiques produits sont utilisés dans les élevages[13]. Les préparations à base de phages offrent une intéressante alternative de contrôle et de prévention des infections. En Norvège, en 2016, des essais cliniques sont menés en aquaculture[14].
Les phages lytiques sont utilisés pour combattre des infections bactériennes sous la forme de phagothérapies ou de traitement bactériophagique. Ces derniers sont utilisés en France, en Allemagne, en Géorgie, en URSS puis en Russie, en Pologne, aux États-Unis, et finalement partout dans le monde[15],[16], avec ou sans adjonction de traitement antibiotique.
En France, leur utilisation et commercialisation disparaît au début des années 1980 (on les trouve dans le Vidal jusqu'en 1978 et on les utilise encore pendant des années dans certains centres hospitaliers comme à Montpellier[17]). Leur efficacité n'est pas remise en question mais leur utilisation est moins pratique que celle des antibiotiques et demeure assez empirique (pas d'évaluation de la spécificité des phages, pas de titration des solutions...)[18]. L'entreprise américaine Eli Lilly cesse la commercialisation des phagiques aux États-Unis avec le développement des antibiotiques[19]. L'emploi des médicaments bactériophagiques se maintient dans les pays de l'ex-bloc soviétique. Les médicaments bactériophagiques sont employés en Russie pour traiter certaines infections telles que la shigellose[20]. En 2017, la consommation en Russie s'élève à plus d'un milliard de boîtes de phagiques par an[21].
La phagothérapie fait actuellement l'objet d'un regain d'intérêt car elle présente une solution pour traiter les infections par des souches bactériennes résistantes aux antibiotiques[15].
En France l'entreprise Pherecydes Pharma développe des « cocktails de phages » pour traiter et prévenir les infections de grandes plaies exposées (brûlure notamment) et les infections pulmonaires[22].
La phagothérapie est possible en France dans le cadre d'une Autorisation temporaire d'utilisation nominative, c'est-à-dire au cas par cas, et dans les limites prévues par l'ANSM[23] : un pronostic vital engagé ou pronostic fonctionnel menacé ; une impasse thérapeutique ; une infection mono-microbienne. S'y ajoutent les restrictions suivantes : la nécessité d’un groupe de validation issu du Comité scientifique spécialisé temporaire sur la phagothérapie de l'ANSM pour toute demande d’ATUn de bactériophages afin d’obtenir un avis collégial ; la nécessité de disposer des résultats d’un phagogramme avant la décision d’une mise sous traitement.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.