Loading AI tools
composé chimique De Wikipédia, l'encyclopédie libre
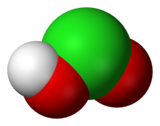
L'acide chloreux est un composé inorganique de formule brute HClO2. C'est un acide faible. L'atome de chlore y est au degré d’oxydation +III. Ce composé est instable sous forme pure.
| Acide chloreux | ||

| ||
 | ||
| Identification | ||
|---|---|---|
| Nom UICPA | acide chloreux chlorite d'hydrogène |
|
| Synonymes |
acide hypochlorique |
|
| No CAS | ||
| PubChem | 24453 | |
| ChEBI | 29219 | |
| SMILES | ||
| InChI | ||
| Propriétés chimiques | ||
| Formule | HClO2 [Isomères] |
|
| Masse molaire[1] | 68,46 ± 0,003 g/mol H 1,47 %, Cl 51,79 %, O 46,74 %, |
|
| pKa | 1,93-1.97[2],[3],[4] | |
| Unités du SI et CNTP, sauf indication contraire. | ||
| modifier |
||
Ce composé est instable sous forme pure, il se dismute en acide hypochloreux HClO, dont l'état d'oxydation du chlore est +1, et en acide chlorique, HClO3 (état d'oxydation du chlore +5) :
En solution aqueuse froide et diluée, l'acide chloreux est en équilibre avec du dioxyde de chlore et de l'acide chlorhydrique, la forme acide chloreux étant minoritaire[4] :
En revanche, les anions chlorite, base conjuguée de cet acide, forment des sels, tels que le chlorite de sodium, qui sont stables même à l'état pur.
Une solution d'acide chloreux peut être préparée en faisant réagir du chlorite de baryum avec de l'acide sulfurique dilué :
Le sulfate de baryum précipite et laisse une solution d'acide chloreux.
Le chlore est le seul halogène pour lequel un oxoacide de formule HXO2 peut être isolé[5]. Le fluor ne possède pas d'état d'oxydation supérieur à +1 et ni l'acide bromeux, ni l'acide iodeux n'ont été isolés. D'autre part, si quelques rares sels de l'acide bromeux, les bromites, sont connus, aucun iodite ne l'est[5].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.