Azida
From Wikipedia, the free encyclopedia
Azida N3- formulako anioia da. Azido hidrazoikoaren base konjugatua da eta, aldi berean, kimika organikoan funtzio-taldea da[1]. Azida nukleozalea da, baina alkilazida (RN3) elekroizaiea da.

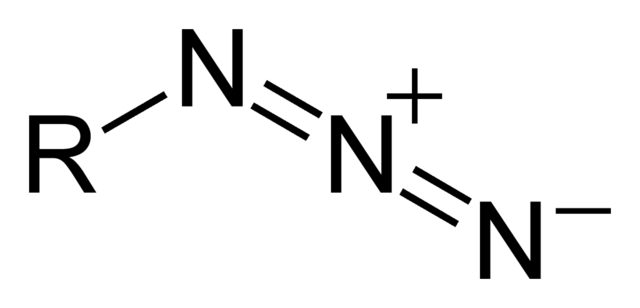
Azida anioiak karbona dioxidoarekin ( CO2) eta oxido nitrosoarekin ( N2O) isoelektronikoa da. Balentzia-loturaren teoriaren arabera azidak egitura erresonante bat baino gehiago izan ditzake, inportanteena N-=N+=N- delarik
Azida inorgarnikoak
Azidek lotura kobalenteak edo ioinikoak era ditzakete metalekin. Horietako batzuk erabilera handia dute. Sodio azida (NaN3) adibidez; berau gatz bat da nitrogeno gaseosoaren iturri gisa usatzen dena airbagetan[2].
Metal astunen azidak oso lehergarriak dira.
Azida organikoak
Sintesi organikoan erabilera zabala dute azidek. Hiru erreakziobide nagusiri zor zaio aziden erreaktibitatea irudian ikus daitekeen legez.

- N1 nitrogenoan zehar eraso nukleozale egitea elektroizale bati (A).
- Nukleozale batek N3 nitrogenoari erasotzea (B).
- Zikloadizioa non azida taldeak dipolo baten moduan jokatzen duen alkenoen eta alkinoen moduko dipolozaleen aurrean (C).
Hain zuzen azken erreakziobide hori dago 2022ko Kimikako Nobel sariaren atzean. Izan ere, Morten Meldal-ek eta K. Barry Sharpless-ek, bakoitzak bere aldetik, kobreak katalizatutako azida-alkino zikloadizioak lortu zituzten, klik kimikan garapen erabakigarria izan dena[3][4].
Toxikotasuna
Azida anioia toxikoa da eta zitokromo eta oxidasa entzimen lana inhibitzeko gai da. Adibidez hemo kofaktorearekin lortura itzulezina eratzen du karbono monoxidoak egiten duen modu berean.
Sodio azida ere toxikoa da irentsita eta azalean zehar absorbatuta[5].
Edonola ere azidekin tentuz lan egin behar da jokaera toxikoa izan dezaketelako.
Erreferentziak
Kanpo estekak
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
