
Γαλακτικό οξύ
From Wikipedia, the free encyclopedia
Το γαλακτικό οξύ[1] (αγγλικά: lactic acid) είναι οργανική χημική ένωση, με μοριακό τύπο C3H6O3, αν και συνηθέστερα παριστάνεται ως CH3Cλαλα. Το χημικά καθαρό γαλακτικό οξύ, στις κανονικές συνθήκες περιβάλλοντος, είναι λευκό στερεό, αναμείξιμο με το νερό.[2] Όταν διαλύεται στο τελευταίο (νερό) σχηματίζει ένα άχρωμο διάλυμα. Η παραγωγή του συμπεριλαμβάνει τόσο φυσικές όσο και τεχνητές μεθόδους. Το γαλακτικό οξύ είναι ένα α-υδροξυοξύ (AHA, A-HydroxyAcid), λόγω της παρουσίας υδροξυομάδας δίπλα ακριβώς από την καρβοξυλομάδα του. Χρησιμοποιήθηκε βιομηχανικά ως ενδιάμεσο συνθετικό σύνθεσης διαφόρων οργανικών και βιοχημικών προϊόντων. Η συζυγής βάση του γαλακτικού οξέος είναι το γαλακτικό ανιόν [CH3C(OH)CO2–].
| Γαλακτικό οξύ | |
|---|---|
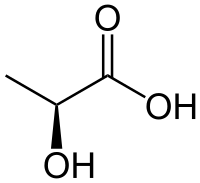 | |
 | |
 | |
| Γενικά | |
| Όνομα IUPAC | 2-υδροξυπροπανικό οξύ |
| Άλλες ονομασίες | Γαλακτικό οξύ α-υδροξυπροπανικό οξύ |
| Χημικά αναγνωριστικά | |
| Χημικός τύπος | C3H6O3 |
| Μοριακή μάζα | 90,08 amu |
| Σύντομος συντακτικός τύπος | CH3CH(OH)COOH |
| Συντομογραφίες | MeCH(OH)COOH |
| Αριθμός CAS | 50-21-5, 79-33-4 (L) 10326-41-7 (D) 598-82-3 (DL) |
| SMILES | CC(O)C(=O)O |
| ChemSpider ID | 96860 |
| Κωδικός προσθέτου τροφίμων | E270 |
| Ισομέρεια | |
| Ισομερή θέσης | 65 |
| Οπτικά ισομερή | 2 |
| Φυσικές ιδιότητες | |
| Σημείο τήξης | 53°C (D) 53°C (L) 16,8°C (DL) |
| Σημείο βρασμού | 122°C (12 mmHg) |
| Πυκνότητα | 1.210 kg/m³ |
| Τάση ατμών | 10 Pa |
| Γωνία στροφής πολωμένου φωτός | [α]D20 = -2,6 (D, H2O) [α]D15 = +3,82 (L, H2O) |
| Χημικές ιδιότητες | |
| pKa | 3,86 |
| Εκτός αν σημειώνεται διαφορετικά, τα δεδομένα αφορούν υλικά υπό κανονικές συνθήκες περιβάλλοντος (25°C, 100 kPa). | |
Το γαλακτικό οξύ σε υδατικό διάλυμα διίσταται, σχηματίζοντας γαλακτικό ανιόν και υδροξώνιο (Η3Ο+). Σε σύγκριση με το οξικό οξύ, το γαλακτικό οξύ έχει pKa = 3,86 έναντι 4,756 του πρώτου (δηλαδή του οξικού οξέος), γεγονός που σημαίνει ότι το γαλακτικό οξύ είναι περίπου κατά 10 φορές ισχυρότερο οξύ από αυτό (δηλαδή το οξικό οξύ). Η υψηλότερη οξύτητά του είναι συνέπεια του ενδομοριακού δεσμού υδρογόνου μεταξύ του ατόμου υδρογόνου του υδροξυλίου και του ενός ατόμου οξυγόνου του καρβοξυλίου.
Το γαλακτικό οξύ είναι χειρόμορφο, αποτελούμενο από δυο εναντιομερή. Το ένα είναι γνωστό ως L-(+)- ή S- γαλακτικό οξύ, ενώ το άλλο, που όμοιο με κατοπτρική εικόνα του πρώτου, είναι γνωστό ως D-(-)- ή R- γαλακτικό οξύ. Ένα ισομοριακό μείγμα των δυο εναντιομερών ονομάζεται DL- ή ρακεμεικό γαλακτικό οξύ. Το DL-γαλακτικό οξύ είναι υγροσκοπικό και αναμείξιμο με το νερό, αλλά και με την αιθανόλη, πάνω από την κανονική θερμοκρασία τήξης του, που είναι 16,8 °C. Τα διαχωρισμένα εναντιομερή έχουν αρκετά υψηλότερη θερμοκρασία τήξης (53°C). Το γαλακτικό οξύ που παράγεται με ζύμωση γάλακτος είναι συχνά ρακεμεικό, παρόλο που υπάρχουν κάποια συγκεκριμένα είδη βακτηριδίων που παράγουν μόνο D-γαλακτικό οξύ. Από την άλλη, το γαλακτικό οξύ που παράγεται με αναερόβεια αναπνοή των ζωικών μυών είναι το L-γαλακτικό οξύ και γι' αυτόν το λόγο ενίοτε το εναντιομερές αυτό ονομάζεται «σαρκογαλακτικό οξύ», δηλαδή με πρόθεμα που προέρχεται από την ελληνική λέξη «σάρξ» (δηλαδή σάρκα).
Στα ζώα, το L-γαλακτικό οξύ παράγεται σταθερά από το πυροσταφυλικό οξύ, μέσω ενός ενζύμου που ονομάζεται γαλακτική δεϋδρογονάση (LDH, Lactate DeHydrogenase), σε μια διεργασία ζύμωσης που συμβαίνει κατά τον κανονικό μεταβολισμό και την άσκηση. Η συγκέντρωση του L-γαλακτικού οξέος δεν αυξάνεται, παρά μόνο αν ο ρυθμός παραγωγής του ξεπεράσει το ρυθμό αποσύνθεσής του, που ρυθμίζεται από έναν αριθμό παραμέτρων, που συμπεριλαμβάνουν μεταφορείς μονοκαρβοξυλικών, τη συγκέντρωση και τον ισοφορμισμό της LDH, καθώς και την οξειδωτική χωρητικότητα των ιστών.
Η συγκέντρωση του L-γαλακτικού οξέος στο αίμα είναι συνήθως 1-2 mM σε ηρεμία, αλλά μπορεί να ξεπεράσει τα 20 mM, κατά τη διάρκεια έντονης άσκησης, καθώς και τα 25 mM μετά την άσκηση.
Απομονώθηκε για πρώτη φορά το 1780, από το Σουηδό χημικό Καρλ Βίλχελμ Σέελε (Carl Wilhelm Scheele).
Στη βιομηχανία, η γαλακτική ζύμωση πραγματοποιείται από τα βακτήρια γαλακτικού οξέος (LAB), που μετατρέπουν γλυκόζη και σουκρόζη σε γαλακτικό οξύ. Αυτά τα βακτήρια μπορούν επίσης να αναπτυχθούν στο στόμα: Το γαλακτικό οξύ που παράγουν είναι υπεύθυνο για τη φθορά των δοντιών[3][4][5][6].
Στην ιατρική, το γαλακτικό οξύ είναι ένα από τα κύρια συστατικά του γαλακτικού διαλύματος Ρίνγκερ (lactated Ringer's solution) και του γαλακτικού διαλύματος Χάρτμανν (lactated Hartmann's solution). Αυτά τα ενδοφλέβια διαλύματα περιέχουν γαλακτικό οξύ, χλωριούχο νάτριο (NaCl) και χλωριούχο κάλιο (KCl) σε αποσταγμένο νερό, σε ισοτονικές με το ανθρώπινο αίμα συγκεντρώσεις, Η πιο συνηθισμένη χρήση αυτών των διαλυμάτων είναι η αντικατάσταση απωλειών σε υγρά του αίματος, μετά από αιμορραγία από τραύμα, εγχείρηση ή έγκαυμα.