Μια σταθερά διάστασης οξέος, Ka, (γνωστή επίσης και ως σταθερά οξύτητας, ή σταθερά ιοντισμού οξέος) είναι μια ποσοτική μέτρηση της ισχύος ενός οξέος σε διάλυμα. Κάθε οξύ έχει διαφορετικό pKa. Είναι η σταθερά ισορροπίας μιας χημικής αντίδρασης γνωστής ως διάσταση στο περιβάλλον των αντιδράσεων οξέος-βάσης. Όσο μεγαλύτερη η τιμή του Ka, τόσο μεγαλύτερη η διάσταση των μορίων στο διάλυμα και συνεπώς πιο ισχυρό το οξύ. Άρα, ένα ισχυρό οξύ «θέλει» να απαλλαγεί από το πρωτόνιο [υδρογονοϊόν (H+)] πολύ περισσότερο από ένα ασθενές οξύ.

Να μη συγχέεται με το pH, που είναι το μέτρο του πόσο όξινο (ή αλκαλικό) είναι ένα διάλυμα. Μια μικρή ποσότητα ισχυρού οξέος στο νερό θα οδηγήσει σε ένα χαμηλό pH (π.χ. 2), ενώ η ίδια συγκέντρωση ασθενούς οξέος δεν οδηγήσει σε ένα τέτοιο χαμηλό pH (π.χ. 5).
Η ισορροπία της διάστασης του οξέος μπορεί να γραφτεί συμβολικά ως:
όπου HA είναι ένα γενικό οξύ που διίσταται διαιρούμενο σε A−, γνωστό ως η συζυγής βάση του οξέος και το υδρογονοϊόν ή πρωτόνιο, H+, που, στην περίπτωση των υδατικών διαλυμάτων, υπάρχει ως υδροξώνιο—με άλλα λόγια, ένα επιδιαλυτωμένο πρωτόνιο. Στο παράδειγμα του σχήματος, το HA αντιπροσωπεύει το αιθανικό οξύ, και το A− αντιπροσωπεύει το οξικό ιόν, τη συζυγή βάση. Τα HA, A− and H+ λέγεται ότι είναι σε ισορροπία όταν οι συγκεντρώσεις τους δεν μεταβάλλονται με την πάροδο του χρόνου. Η σταθερά διάστασης συνήθως γράφεται ως ένα πηλίκο των συγκεντρώσεων ισορροπίας (σε mol/L), που συμβολίζονται με [HA], [A−] και [H+]:
Λόγω των πολλών τάξεων μεγέθους που καλύπτονται από τις τιμές Ka, χρησιμοποιείται συνήθως στην πράξη μια λογαριθμική μέτρηση της σταθεράς διάστασης του οξέος. Η λογαριθμική σταθερά, pKa, που είναι ίση με −log10 Ka, αναφέρεται μερικές φορές (αλλά λαθεμένα) ως μια σταθερά διάστασης του οξέος:
Όσο πιο μεγάλη η τιμή του pKa, τόσο πιο μικρή η έκταση της διάστασης σε οποιοδήποτε δεδομένο pH (δείτε εξίσωση Χέντερσον-Χάσελμπαχ ([Henderson–Hasselbalch))—που σημαίνει τόσο πιο ασθενές το οξύ. Ένα ασθενές οξύ έχει μια τιμή pKa περίπου −2 έως 12 στο νερό. Οξέα με τιμή pKa μικρότερη από περίπου −2 θεωρούνται ως ισχυρά οξέα· ένα ισχυρό οξύ διίσταται σχεδόν πλήρως σε υδατικό διάλυμα, σε βαθμό που η συγκέντρωση του αδιάστατου οξέος δεν ανιχνεύεται. Οι τιμές του pKa για ισχυρά οξέα μπορούν, όμως, να εκτιμηθούν θεωρητικά ή με παρεκβολή από μετρήσεις σε μη υδατικούς διαλύτες στους οποίους η σταθερά διάστασης είναι πιο μικρή, όπως στο αιθανονιτρίλιο και το διμεθυλοσουλφοξείδιο.
Η σταθερά διάστασης του οξέος για ένα οξύ είναι άμεση συνέπεια της υποκείμενης χημικής θερμοδυναμικής της αντίδρασης διάστασης· η τιμή pKa είναι ευθέως ανάλογη με την πρότυπη ελεύθερη ενέργεια Gibbs της αντίδρασης. Η τιμή του pKa αλλάζει με τη θερμοκρασία και μπορεί να κατανοηθεί ποιοτικά με βάση την αρχή του Le Chatelier: όταν η αντίδραση είναι ενδόθερμη, η pKa μειώνεται με αύξηση της θερμοκρασίας· το αντίθετο αληθεύει για εξώθερμες αντιδράσεις.
Η τιμή του pKa εξαρτάται επίσης από τη μοριακή δομή κατά πολλούς τρόπους. Παραδείγματος χάρη, ο Λάινους Πόλινγκ (Linus Pauling) πρότεινε δύο κανόνες: έναν για διαδοχικά pKa των πολυπρωτικών οξέων (δείτε «πολυπρωτικά οξέα» παρακάτω) και έναν για την εκτίμηση του pKa των οξυοξέων με βάση των αριθμό των =Ο και των ομάδων −OH (δείτε παρακάτω «Παράγοντες που επηρεάζουν τις τιμές pKa»). Άλλοι δομικοί παράγοντες που επηρεάζουν το μέγεθος της σταθεράς διάστασης του οξέος περιλαμβάνουν επαγωγικά φαινόμενα, μεσομερικά φαινόμενα και δεσμούς υδρογόνου.
Η ποσοτική συμπεριφορά των οξέων και των βάσεων σε διάλυμα μπορεί να κατανοηθεί μόνο αν οι τιμές pKa τους είναι γνωστές. Ειδικά, το pH ενός διαλύματος μπορεί να προβλεφθεί, όταν η αναλυτική συγκέντρωση και οι τιμές pKa όλων των οξέων και των βάσεων είναι γνωστές· αντίθετα, είναι δυνατός ο υπολογισμός της συγκέντρωσης ισορροπίας των οξέων και των βάσεων σε διάλυμα όταν το pH είναι γνωστό. Αυτοί οι υπολογισμοί βρίσκουν εφαρμογή σε πολλούς διαφορετικούς τομείς της χημείας, της βιολογίας, της ιατρικής και της βιολογίας. Παραδείγματος χάρη, πολλές ενώσεις που χρησιμοποιούνται ως φάρμακα είναι ασθενή οξέα ή βάσεις και η γνώση των τιμών pKa, μαζί με τον συντελεστή κατανομής νερού-οκτανόλης, μπορούν να χρησιμοποιηθούν για την εκτίμηση της έκτασης στην οποία εισέρχεται η ένωση στη ροή του αίματος. Οι σταθερές διάστασης του οξέος είναι επίσης βασικές στην υδατική χημεία και στην χημική ωκεανογραφία, όπου η οξύτητα του νερού παίζει θεμελιακό ρόλο. Στους ζώντες οργανισμούς, η οξεοβασική ισορροπία και η ενζυμική κινητική εξαρτώνται από τις τιμές pKa των πολλών οξέων και βάσεων που υπάρχουν στα κύτταρα και το σώμα. Στη χημεία, η γνώση των τιμών pKa είναι απαραίτητη για την προετοιμασία των ρυθμιστικών διαλυμάτων και είναι επίσης προϋπόθεση για την ποσοτική κατανόηση της αλληλεπίδρασης μεταξύ οξέων ή βάσεων και μεταλλικών ιόντων στο σχηματισμό συμπλόκων. Πειραματικά, οι τιμές pKa μπορούν να προσδιοριστούν με ποτενσιομετρική τιτλοδότηση (pH), αλλά για τιμές του pKa μικρότερες από περίπου 2 ή μεγαλύτερες από περίπου 11, μπορεί να απαιτούνται μετρήσεις φασματοφωτομετρίας ή πυρηνικού μαγνητικού συντονισμού (NMR) λόγω των πρακτικών δυσκολιών με μετρήσεις pH.
Σύμφωνα με τον αρχικό ορισμό του Αρρένιους, ένα οξύ είναι μια ουσία που διίσταται σε υδατικό διάλυμα, ελευθερώνοντας το ιόν υδρογόνου H+ (ένα πρωτόνιο):[1]
- HA
 A− + H+.
A− + H+.
Η σταθερά ισορροπίας για αυτή την αντίδραση διάστασης είναι γνωστή ως σταθερά διάστασης. Το απελευθερωμένο πρωτόνιο συνδυάζεται με ένα μόριο νερού για να δώσει ένα ιόν οξωνίου ή υδροξωνίου H3O+ (γυμνά πρωτόνια δεν υπάρχουν σε διάλυμα) και έτσι ο Αρρένιους πρότεινε αργότερα ότι η διάσταση πρέπει να γραφτεί ως μια αντίδραση οξέος-βάσης:
- HA + H2Ο
 A− + H3O+.
A− + H3O+.
Οι Μπρόνστεντ-Λόρι (Brønsted - Lowry) γενίκευσαν αυτό παραπέρα σε μια αντίδραση ανταλλαγής πρωτονίου:[2][3][4]
- οξύ + βάση
 συζυγής βάση + συζυγές οξύ.
συζυγής βάση + συζυγές οξύ.
Το οξύ χάνει ένα πρωτόνιο, αφήνοντας μια συζυγή βάση· το πρωτόνιο μεταφέρεται στη βάση, δημιουργώντας ένα συζυγές οξύ. Για τα υδατικά διαλύματα ενός οξέος HA, η βάση είναι το νερό· η συζυγής βάση είναι A− και το συζυγές οξύ είναι το ιόν οξωνίου. Ο ορισμός Μπρόνστεντ-Λόρι εφαρμόζεται και σε άλλους διαλύτες, όπως διμεθυλοσουλφοξείδιο: ο διαλύτης S δρα ως βάση, αποδεχόμενος ένα πρωτόνιο και σχηματίζει το συζυγές οξύ SH+.
- HA + S
 A− + SH+.
A− + SH+.
Στη χημεία των διαλυμάτων, είναι συνηθισμένη η χρήση του H+ ως μιας συντόμευσης για το επιδιαλυτωμένο υδογονοϊόν, ανεξάρτητα από τον διαλύτη. Σε υδατικά διαλύματα το H+ υποδηλώνει ένα επιδιαλυτωμένο οξώνιο παρά ένα πρωτόνιο.[5][6]
Ο ορισμός ενός οξέος ή μιας βάσης ως «συζυγούς» εξαρτάται από το περιεχόμενο. Το συζυγές οξύ BH+ μιας βάσης B διίσταται σύμφωνα με την
- BH+ + OH−
 B + H2O
B + H2O
που είναι η αντίστροφη της ισορροπίας
- H2Ο (οξύ) + B (βάση)
 OH− (συζυγής βάση) + BH+ (συζυγές οξύ).
OH− (συζυγής βάση) + BH+ (συζυγές οξύ).
Το υδροξείδιο OH−, μια καλά γνωστή βάση, δρα εδώ ως συζυγής βάση του οξέος νερό. Τα οξέα και οι βάσεις θεωρούνται συνεπώς απλώς ως δότες και δέκτες πρωτονίων, αντίστοιχα.
Ένας πιο ευρύς ορισμός της διάστασης του οξέος περιλαμβάνει την υδρόλυση, στην οποία παράγονται πρωτόνια από τη διαίρεση των μορίων του νερού. Παραδείγματος χάρη, το βορικό οξύ (B(OH)3) παράγει H3O+ σαν να ήταν δότης πρωτονίου,[7] αλλά έχει επιβεβαιωθεί από τη Φασματοσκοπία Ράμαν ότι αυτό οφείλεται στην ισορροπία της υδρόλυσης:[8]
- B(OH)3 + 2 H2Ο
 B(OH)4− + H3O+.
B(OH)4− + H3O+.
Παρόμοια, η υδρόλυση μεταλλικού ιόντος προκαλεί ιόντα όπως το[Al(H2O)6]3+ να συμπεριφέρονται ως ασθενή οξέα:[9]
- [Al(H2O)6]3+ +H2Ο
 [Al(H2O)5(OH)]2+ + H3O+.
[Al(H2O)5(OH)]2+ + H3O+.
Σύμφωνα με τον αρχικό ορισμό του Λιούις, ένα οξύ είναι μια ουσία που δέχεται ένα ζεύγος ηλεκτρονίων για να σχηματίσει ημιπολικό δεσμό.[10]
Μια σταθερά διάστασης οξέος είναι ένα συγκεκριμένο παράδειγμα μιας σταθεράς ισορροπίας. Για τη συγκεκριμένη ισορροπία μεταξύ ενός μονοπρωτικού οξέος, HA και της συζυγούς του βάσης A−,στο νερό,
- HA + H2Ο
 A− + H3O+
A− + H3O+
η θερμοδυναμική σταθερά ισορροπίας, K![]() μπορεί να οριστεί από[11]
μπορεί να οριστεί από[11]
όπου {A} είναι η χημική ενεργότητα του χημικού είδους A κλπ. Το K![]() είναι αδιάστατο αφού η ενεργότητα είναι αδιάστατη. Οι ενεργότητες των προϊόντων της διάστασης τοποθετούνται στον αριθμητή και οι ενεργότητες των αντιδρώντων της αντίδρασης τοποθετούνται στον παρανομαστή. Δείτε τον συντελεστή ενεργότητας για την προέλευση της έκφρασης.
είναι αδιάστατο αφού η ενεργότητα είναι αδιάστατη. Οι ενεργότητες των προϊόντων της διάστασης τοποθετούνται στον αριθμητή και οι ενεργότητες των αντιδρώντων της αντίδρασης τοποθετούνται στον παρανομαστή. Δείτε τον συντελεστή ενεργότητας για την προέλευση της έκφρασης.

Επειδή η ενεργότητα είναι το γινόμενο της συγκέντρωσης και του συντελεστή ενεργότητας (γ) ο ορισμός μπορεί επίσης να γραφεί ως
όπου [HA] αντιπροσωπεύει τη συγκέντρωση του HA και το είναι ο λόγος των συντελεστών ενεργότητας.
Προς αποφυγή των προβλημάτων που σχετίζονται με τη χρήση ενεργοτήτων, οι σταθερές διάστασης προσδιορίζονται, όπου είναι δυνατό, σε ένα μέσο με υψηλή ιοντική ισχύ, δηλαδή, κάτω από συνθήκες στις οποίες το μπορεί να θεωρηθεί ότι είναι πάντα σταθερό.[11] Παραδείγματος χάρη, το μέσο μπορεί να είναι ένα διάλυμα των 0.1 M νιτρικού νατρίου ή 3 M υπερχλωρικού καλίου (1 M = 1 mol·dm−3, μια μονάδα της μοριακής συγκέντρωσης). Επιπλέον, σε όλα εκτός τα πάρα πολύ πυκνά διαλύματα μπορεί να θεωρηθεί ότι η συγκέντρωση του νερού, [H2O], είναι σταθερή, περίπου 55 mol·dm−3. Διαιρώντας το K![]() με τους σταθερούς όρους και γράφοντας [H+] για τη συγκέντρωση του οξωνίου λαμβάνεται η παράσταση.
με τους σταθερούς όρους και γράφοντας [H+] για τη συγκέντρωση του οξωνίου λαμβάνεται η παράσταση.
Αυτός είναι ο ορισμός σε κοινή χρήση.[12] Το pKa ορίζεται ως ο −log10 Ka.
Σημειώστε, όμως, ότι όλες οι δημοσιευόμενες τιμές σταθερών διάστασης αναφέρονται στο συγκεκριμένο χρησιμοποιούμενο ιοντικό μέσο στον προσδιορισμό τους και ότι διαφορετικές τιμές λαμβάνονται σε διαφορετικές συνθήκες, όπως φαίνεται για το αιθανικό οξύ στο παραπάνω διάγραμμα. Όταν οι δημοσιευόμενες σταθερές αναφέρονται σε μια ιοντική ισχύ άλλη από την απαιτούμενη για τη συγκεκριμένη εφαρμογή, μπορούν να προσαρμοστούν μέσα από την ειδική ιονική θεωρία (SIT) και άλλες θεωρίες.[13]
Αν και το Ka εμφανίζεται να έχει τις διαστάσεις της συγκέντρωσης, ο ακριβής ορισμός χρησιμοποιεί χημικές ενεργότητες, που είναι αδιάστατες. Συνεπώς, το Ka, όταν ορίζεται σωστά, είναι επίσης αδιάστατο· αν και δεν είναι ασυνήθιστο, ιδιαίτερα σε κείμενα που σχετίζονται με βιοχημικές ισορροπίες, να εμφανίζεται μια παρατιθέμενη τιμή με διαστάσεις όπως, παραδείγματος χάρη, Ka = 300 M.
Μονοπρωτικά οξέα
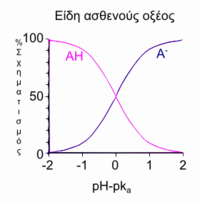
Μετά την αναδιάταξη της παράστασης που ορίζει το Ka και βάζοντας pH = −log10[H+], παίρνουμε[14]
Αυτή είναι μια μορφή της εξίσωσης Χέντερσον-Χάσελμπαχ (Henderson–Hasselbalch)], από την οποία μπορούν να εξαχθούν τα παρακάτω συμπεράσματα.
- Στην ημιεξουδετέρωση [A−]/[HA] = 1; επειδή log(1) =0, το pH της ημιεξουδετέρωσης είναι αριθμητικά ίσο με το pKa. Αντίθετα, όταν το pH = pKa, η συγκέντρωση του HA είναι ίση με τη συγκέντρωση του A−.
- Η ρυθμιστική περιοχή εκτείνεται στο προσεγγιστικό εύρος pKa ± 2, αν και το ρυθμιστικό είναι ασθενές έξω από το εύρος pKa ± 1. Στο pKa ± 1, [A−]/[HA] = 10 ή 1/10.
- Αν το pH είναι γνωστό, μπορεί να υπολογιστεί ο λόγος. Αυτός ο λόγος είναι ανεξάρτητος από την αναλυτική συγκέντρωση του οξέος.
Στο νερό, το εύρος των μετρήσιμων τιμών pKa είναι από περίπου −2 για ένα ισχυρό οξύ μέχρι περίπου 2 για ένα πολύ ασθενές οξύ (ή ισχυρή βάση). Όλα τα οξέα με τιμή pKa μικρότερη από −2 είναι σε ποσοστό πάνω από 99% σε διάσταση σε pH 0 (1 M οξέος). Αυτό είναι γνωστό ως εξισωτικό φαινόμενο, επειδή όλα αυτά τα οξέα φέρονται στο ίδιο επίπεδο να είναι ισχυρά οξέα, ανεξάρτητα από τις τιμές του pKa. Παρομοίως, όλες οι βάσεις με τιμή pKa μεγαλύτερη από το άνω όριο είναι πρωτονιωμένες σε ποσοστό περισσότερο από 99% σε όλες τις εφικτές τιμές pH και ταξινομούνται ως ισχυρές βάσεις.[3]
Ένα παράδειγμα ισχυρού οξέος είναι το υδροχλωρικό οξύ, HCl, που έχει μια τιμή pKa, που εκτιμάται από θερμοδυναμικά δεδομένα σε −9,3 στο νερό.[15] Η συγκέντρωση του αδιάστατου οξέος σε ένα διάλυμα mol·dm−3 θα είναι μικρότερη από 0,01% των συγκεντρώσεων των προϊόντων της διάστασης. Τότε, το υδροχλωρικό οξύ λέγεται ότι είναι «πλήρως διιστάμενο» σε υδατικό διάλυμα, επειδή το ποσοστό του αδιάστατου οξέος είναι ανεπαίσθητο. Όταν το pKa και η αναλυτική συγκέντρωση του οξέος είναι γνωστά, η έκταση διάστασης και το pH ενός διαλύματος μονοπρωτικού οξέος μπορεί εύκολα να υπολογιστεί χρησιμοποιώντας έναν πίνακα ICE.
Ένα ρυθμιστικό διάλυμα επιθυμητού pH μπορεί να προετοιμαστεί ως μείγμα ενός ασθενούς οξέος και της συζυγούς του βάσης. Στην πράξη το μείγμα μπορεί να δημιουργηθεί διαλύοντας το οξύ σε νερό και προσθέτοντας την αναγκαία ποσότητα ισχυρού οξέος ή βάσης.Το pKa του οξέος πρέπει να έχει μια μονάδα διαφορά από το επιθυμητό pH (pH-1< pKa < pH+1) .
Πολυπρωτικά οξέα

Τα πολυπρωτικά οξέα είναι οξέα που μπορούν να χάσουν περισσότερα από ένα πρωτόνιο. Η σταθερά διάστασης για το πρώτο πρωτόνιο μπορεί να δηλωθεί ως Ka1 και οι σταθερές διάστασης για τα επόμενα πρωτόνια ως Ka2, κλπ. Το φωσφορικό οξύ, H3PO4, είναι ένα παράδειγμα ενός πολυπρωτικού οξέος επειδή μπορεί να χάσει τρία πρωτόνια.
| Ισορροπία | Τιμή pKa[16] |
|---|---|
| H3PO4 |
pKa1 = 2,14 |
| H2PO4− |
pKa2 = 7,20 |
| HPO42− |
pKa3 = 12,37 |
Όταν η διαφορά μεταξύ των διαδοχικών τιμών pK είναι περίπου τέσσερα ή περισσότερο, όπως σε αυτό το παράδειγμα, κάθε είδος μπορεί να θεωρηθεί ως ένα οξύ από μόνο του·[17] Στην πραγματικότητα τα άλατα του H2PO4− μπορούν να κρυσταλλωθούν από διάλυμα με ρύθμιση του pH σε περίπου 5,5 και άλατα του HPO42− μπορούν να κρυσταλλωθούν από διάλυμα με ρύθμιση του pH σε περίπου 10. Το διάγραμμα κατανομής των ειδών εμφανίζει ότι οι συγκεντρώσεις των δύο ιόντων είναι μέγιστες σε pH 5,5 και 10.

Όταν η διαφορά μεταξύ των διαδοχικών τιμών pK είναι μικρότερη από περίπου τέσσερα υπάρχει επικάλυψη μεταξύ του εύρους ύπαρξης του pH των ειδών σε ισορροπία. Όσο πιο μικρή η διαφορά, τόσο μεγαλύτερη η επικάλυψη. Η περίπτωση του κιτρικού οξέος εμφανίζεται στα δεξιά· διαλύματα του κιτρικού οξέος ρυθμίζονται σε όλο το εύρος του pH από 2,5 έως 7,5.
Σύμφωνα με τον πρώτο κανόνα του Πόλινγκ, οι διαδοχικές τιμές pK ενός δεδομένου οξέος αυξάνονται (pKa2 > pKa1).[18] Για οξυοξέα με περισσότερα από ένα ιονιζόμενο υδρογόνο στο ίδιο άτομο, οι τιμές pKa αυξάνονται συχνά κατά περίπου 5 μονάδες για κάθε αφαιρούμενο πρωτόνιο,[19][20] όπως στο παραπάνω παράδειγμα του φωσφορικού οξέος.
Στην περίπτωση ενός διπρωτικού οξέος, H2A, οι δύο ισορροπίες είναι
- H2A
 HA− + H+
HA− + H+ - HA−
 A2− + H+
A2− + H+
και μπορεί να φανεί ότι το δεύτερο πρωτόνιο αφαιρείται από ένα αρνητικά φορτισμένο είδος. Επειδή το πρωτόνιο φέρει ένα θετικό φορτίο απαιτείται πρόσθετο έργο για την αφαίρεσή του· αυτή είναι η αιτία της παραπάνω προαναφερθείσας τάσης. Οι παραπάνω τιμές του φωσφορικού οξέος επιβεβαιώνουν αυτόν τον κανόνα, όπως κάνουν και οι τιμές του βαναδικού οξέος, H3VO4. Όταν βρίσκεται κάποια εξαίρεση στον κανόνα, σημαίνει ότι μια σημαντική αλλαγή έχει συμβεί στη δομή. Στην περίπτωση του of VO2+ (aq), το βανάδιο έχει οκταεδρική γεωμετρία, ενώ το βαναδικό οξύ έχει τετραεδρική γεωμετρία. Αυτή είναι η βάση που εξηγεί γιατί το pKa1 > pKa2 για τα οξυοξέα του βαναδίου(V).
| Ισορροπία | Τιμή pKa |
|---|---|
| [VO2(H2O)4]+ |
pKa1 = 4,2 |
| H3VO4 |
pKa2 = 2,60 |
| H2VO4− |
pKa3 = 7,92 |
| HVO42− |
pKa4 = 13,27 |
Ισοηλεκτρικό σημείο
Για ουσίες σε διάλυμα, το ισοηλεκτρικό σημείο (pI) ορίζεται ως το pH στο οποίο το άθροισμα, σταθμισμένο κατά τιμή φορτίου, των συγκεντρώσεων των θετικά φορτισμένων ειδών είναι ίσο με το σταθμισμένο άθροισμα των συγκεντρώσεων των αρνητικά φορτισμένων ειδών. Στην περίπτωση που υπάρχει από ένα είδος κάθε τύπου, το ισοηλεκτρικό σημείο μπορεί να ληφθεί άμεσα από τις τιμές pK. Παραδείγματος χάρη, το παράδειγμα της γλυκίνης, που ορίζεται ως AH. Υπάρχουν δύο ισορροπίες διάστασης για εξέταση.
- AH2+
 AH + H+; [AH][H+] = K1[AH2+]
AH + H+; [AH][H+] = K1[AH2+] - AH
 A− + H+; [A−][H+] = K2[AH]
A− + H+; [A−][H+] = K2[AH]
Αντικαθιστώντας την παράσταση για το [AH] στην πρώτη εξίσωση
- [A−][H+]2 = K1K2[AH2+]
Στο ισοηλεκτρικό σημείο η συγκέντρωση των θετικά φορτισμένων ειδών, AH2+, ισούται με τη συγκέντρωση των αρνητικά φορτισμένων ειδών, A−, έτσι
- [H+]2 = K1K2
Συνεπώς, λαμβάνοντας τους συλλογάριθμους, έχουμε
Οι τιμές pI για τα αμινοξέα είναι καταχωρισμένες στα πρωτεϊνογενετικά αμινοξέα. Όταν περισσότερα από δύο φορτισμένα είδη είναι σε ισορροπία μεταξύ τους ένας πλήρης υπολογισμός των ειδών μπορεί να χρειαστεί.
Αυτοϊονισμός του νερού
Το νερό κατέχει και όξινες και βασικές ιδιότητες. Είναι αμφιπρωτικό. Η σταθερά ισορροπίας για την ισορροπία
- 2 H2Ο
 OH− + H3O+
OH− + H3O+
δίνεται από την:
Όταν, όπως συνήθως συμβαίνει, η συγκέντρωση του νερού μπορεί να θεωρηθεί σταθερή, αυτή η παράσταση μπορεί να αντικατασταθεί από:
Η σταθερά αυτοϊοντισμού του νερού, Kw, είναι συνεπώς απλά μια ειδική περίπτωση της σταθεράς διάστασης ενός οξέος.
| T/°C | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 | 50 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| pKw | 14,943 | 14,734 | 14,535 | 14,346 | 14,167 | 13,997 | 13,830 | 13,680 | 13,535 | 13,396 | 13,262 |
Από αυτά τα δεδομένα μπορούμε να συμπεράνουμε ότι Kw = 10−14 στους 24,87 °C. Σε αυτή τη θερμοκρασία και τα υδρογονοϊόντα και τα ιόντα υδροξειδίου έχουν συγκέντρωση 10−7 mol dm−3.
Επαμφοτερίζουσες ουσίες
Μια επαμφοτερίζουσα ουσία είναι μια ουσία που μπορεί να δράσει είτε ως οξύ, είτε ως βάση, ανάλογα με το pH. Το νερό είναι επαμφοτερίζουσα ουσία. Ένα άλλο παράδειγμα επαμφοτερίζοντος μορίου είναι το όξινο ανθρακικό ιόν HCO3− που είναι η συζυγής βάση του ανθρακικού οξέος H2CO3 στην ισορροπία
- H2CO3 + H2Ο
 HCO3− + H3O+
HCO3− + H3O+
αλλά επίσης το συζυγές οξύ του ανθρακικού ιόντος CO32− στην αντίστροφη της ισορροπίας
- HCO3− + OH−
 CO32− + H2O.
CO32− + H2O.
Οι ισορροπίες του ανθρακικού οξέος είναι σημαντικές για την οξεοβασική ισορροπία στο ανθρώπινο σώμα.
Ένα αμινοξύ είναι επίσης επαμφοτερίζον με την πρόσθετη περιπλοκή ότι το ουδέτερο μόριο υπόκειται σε μια εσωτερική ισορροπία οξέος-βάσης στην οποία η βασική αμινομάδα έλκει και συνδέει το πρωτόνιο από την όξινη καρβοξυλομάδα, σχηματίζοντας ένα αμφιτεριόν.
- NH2CHRCO2Η
 NH3+CHRCO2−
NH3+CHRCO2−
Σε pH μικρότερο από περίπου 5 και η καρβοξυλομάδα και η αμινομάδα είναι πρωτονιωμένες. Με την αύξηση του pH το οξύ διίσταται σύμφωνα με την
- NH3+CHRCO2Η
 NH3+CHRCO2− + H+
NH3+CHRCO2− + H+
Σε υψηλά pH μια δεύτερη διάσταση μπορεί να λάβει χώρα.
- NH3+CHRCO2−
 NH2CHRCO2− + H+
NH2CHRCO2− + H+
Συνεπώς το αμφιτεριόν, NH3+CHRCO2−, είναι επαμφοτερίζον επειδή μπορεί μπορεί είτε να πρωτονιωθεί, είτε να αποπρωτονιωθεί.
Βάσεις και βασικότητα
Ιστορικά, η σταθερά ισορροπίας Kb για μια βάση έχει οριστεί ως η σταθερά σύζευξης για την πρωτονίωση της βάσης, B, ώστε να σχηματίσει το συζυγές οξύ, HB+.
- B + H2Ο
 HB+ + OH−
HB+ + OH−
Χρησιμοποιώντας παρόμοιο συλλογισμό με τον προηγούμενο
Το Kb σχετίζεται με το Ka για το συζυγές οξύ. Στο νερό, η συγκέντρωση του ιόντος υδροξειδίου, [OH−], σχετίζεται με τη συγκέντρωση του υδρογονοϊόντος με την Kw = [H+] [OH−], συνεπώς
Η αντικατάσταση της παράστασης για τη [OH−] στην παράσταση για το Kb δίνει
Όταν το Ka, Kb και το Kw προσδιορίζονται κάτω από τις ίδιες συνθήκες θερμοκρασίας και ιοντικής ισχύος, συμπεραίνεται, λαμβάνοντας τους συλλογάριθμους, ότι το pKb ή «βασικότητα»= pKw − pKa. Σε υδατικά διαλύματα στους 25 °C, η pKw είναι 13,9965,[22] έτσι
με αρκετή ακρίβεια για τους περισσότερους πρακτικούς σκοπούς. Στην πραγματικότητα, δεν χρειάζεται ο ορισμός του pKb ξεχωριστά από το pKa, αλλά γίνεται εδώ επειδή συχνά μόνο οι τιμές pKb μπορούν να βρεθούν στην πιο παλιά βιβλιογραφία.
Εξάρτηση από τη θερμοκρασία
Όλες οι σταθερές ισορροπίας ποικίλουν με την θερμοκρασία σύμφωνα με την εξίσωση Βαν'τ Χοφ (van 't Hoff)[23]
Το R είναι η σταθερά των αερίων και T είναι η απόλυτη θερμοκρασία σε Κ . Συνεπώς, για εξώθερμες αντιδράσεις, (η πρότυπη μεταβολή της ενθαλπίας, ΔH![]() , είναι αρνητική) το K μειώνεται με τη θερμοκρασία, αλλά για ενδόθερμες αντιδράσεις (ΔH
, είναι αρνητική) το K μειώνεται με τη θερμοκρασία, αλλά για ενδόθερμες αντιδράσεις (ΔH![]() είναι θετική) το K αυξάνεται με τη θερμοκρασία.
είναι θετική) το K αυξάνεται με τη θερμοκρασία.
Ένας διαλύτης είναι πιο πιθανό να προάγει τον ιονισμό ενός διαλυμένου όξινου μορίου στις παρακάτω περιπτώσεις:[24]
- Είναι ένας πρωτικός διαλύτης, ικανός να σχηματίσει δεσμούς υδρογόνου.
- Έχει έναν υψηλό αριθμό δοτικότητας, καθιστώντας τον μια ισχυρή βάση Λιούις.
- Έχει μια υψηλή διηλεκτρική σταθερά (σχετική επιτρεπτότητα), κάνοντας τον καλό διαλύτη για ιοντικά είδη.
Οι τιμές pKa των οργανικών ενώσεων λαμβάνονται συχνά χρησιμοποιώντας τους απρωτικούς διαλύτες διμεθυλοσουλφοξείδιο (dimethyl sulfoxide) (DMSO)[24] και αιθανονιτρίλιο (ACN).[25]
Το DMSO χρησιμοποιείται πλατιά ως μια εναλλακτική λύση αντί για το νερό, επειδή έχει χαμηλότερη διηλεκτρική σταθερά από το νερό και είναι λιγότερο πολικό και έτσι διαλύει μη πολικές, υδρόφοβες ουσίες πιο εύκολα. Έχει μια μετρήσιμη περιοχή pKa από 1 έως 30, περίπου. Το αιθανονιτρίλιο είναι λιγότερο βασικό από το DMSO και συνεπώς, γενικά, τα οξέα είναι πιο ασθενή και οι βάσεις πιο ισχυρές σε αυτόν τον διαλύτη. Κάποιες τιμές pKa στους 25 °C για το αιθανονιτρίλιο (ACN)[26][27][28] και διμεθυλοσουλφοξείδιο (DMSO)[29] εμφανίζονται στους παρακάτω πίνακες. Οι τιμές για το νερό συμπεριλαμβάνονται για σύγκριση.
| HA | ACN | DMSO | νερό |
|---|---|---|---|
| p-Τολουολοσουλφονικό οξύ | 8,5 | 0,9 | ισχυρό |
| 2,4-δινιτροφαινόλη | 16,66 | 5,1 | 3,9 |
| Βενζοϊκό οξύ | 21,51 | 11,1 | 4,2 |
| Αιθανικό οξύ | 23,51 | 12,6 | 4,756 |
| Φαινόλη | 29,14 | 18,0 | 9,99 |
| BH+ | ACN | DMSO | νερό |
| Πυρρολιδίνη | 19,56 | 10,8 | 11,4 |
| Τριαιθυλαμίνη | 18,82 | 9,0 | 10,72 |
| 1,8-δις (διμεθυλαμινο) ναφθαλίνιο(Proton sponge) | 18,62 | 7,5 | 12,1 |
| Πυριδίνη | 12,53 | 3,4 | 5,2 |
| Ανιλίνη | 10,62 | 3,6 | 4,6 |
Ο ιονισμός των οξέων είναι μικρότερος σε έναν όξινο διαλύτη από ότι στο νερό. Παραδείγματος χάρη, το υδροχλώριο είναι ένα ασθενές οξύ διαλυμένο σε αιθανικό οξύ. Αυτό συμβαίνει, επειδή το αιθανικό οξύ είναι μια πολύ ασθενέστερη βάση από το νερό.
- HCl + CH3CO2Η
 Cl− + CH3C(OH)2+
Cl− + CH3C(OH)2+ - οξύ+ βάση
 συζυγής βάση + συζυγές οξύ
συζυγής βάση + συζυγές οξύ
Συγκρίνετε αυτήν την αντίδραση με τι συμβαίνει όταν το αιθανικό οξύ διαλύεται στο πιο όξινο διαλύτη καθαρού θειικού οξέος[30]
- H2SO4 + CH3CO2Η
 HSO4− + CH3C(OH)2+
HSO4− + CH3C(OH)2+
Το είδος της διόλης CH3C(OH)2+ είναι σταθερό σε αυτά τα περιβάλλοντα. Για τα υδατικά διαλύματα η κλίμακα του pH είναι η πιο βολική συνάρτηση οξύτητας.[31] Άλλες συναρτήσεις οξύτητας έχουν προταθεί για μη υδατικά μέσα, με πιο σημαντική τη συνάρτηση οξύτητας Hammett, H0, για μέσα υπεροξέων και η τροποποιημένη του έκδοση H− για τα μέσα υπερβάσεων.[32]

Σε απρωτικούς διαλύτες, ολιγομερή, όπως το πολύ γνωστό διμερές αιθανικό οξύ, μπορεί να σχηματιστεί με δεσμό υδρογόνου. Ένα οξύ μπορεί επίσης να σχηματίσει δεσμούς υδρογόνου με τη συζυγή του βάση. Αυτή η διεργασία, γνωστή ως ομοσύζευξη, έχει ως αποτέλεσμα την αύξηση της οξύτητας των οξέων, μειώνοντας τις ενεργές τους τιμές pKa, σταθεροποιώντας τη συζυγή βάση. Η ομοσύζευξη αυξάνει την δοτική ικανότητα του πρωτονίου του τολουολοσουλφονικού οξέος σε διάλυμα αιθανονιτριλίου κατά έναν συντελεστή σχεδόν 800.[33] Σε υδατικά διαλύματα, δεν συμβαίνει ομοσύζευξη, επειδή το νερό σχηματίζει ισχυρότερους δεσμούς υδρογόνου με τη συζυγή βάση από ότι κάνει με το οξύ.
Μικτοί διαλύτες

Όταν μια ένωση έχει περιορισμένη διαλυτότητα στο νερό στην κοινή πρακτική (στη φαρμακευτική βιομηχανία, παραδείγματος χάρη) οι τιμές pKa προσδιορίζονται σε ένα μείγμα διαλύτη όπως το νερό/διοξάνιο ή νερό/μεθανόλη, όπου η ένωση είναι πιο διαλυτή.[35] Στο παράδειγμα που εμφανίζεται στα δεξιά, η τιμή pKa αυξάνεται απότομα με την αύξηση του ποσοστού του διοξανίου επειδή η διηλεκτρική σταθερά του μείγματος μειώνεται.
Μια τιμή Ka που λαμβάνεται σε ένα μικτό διαλύτη δεν μπορεί να χρησιμοποιηθεί άμεσα για υδατικά διαλύματα. Ο λόγος είναι ότι όταν ο διαλύτης είναι στην τυπική του κατάσταση η ενεργότητά του «ορίζεται» ως 1. Παραδείγματος χάρη, η τυπική κατάσταση νερού:διοξάνιο 9:1 είναι ακριβώς αυτή του μείγματος του διαλύτη, χωρίς πρόσθετες διαλυμένες ουσίες. Για να ληφθεί η τιμή pKa προς χρήση με υδατικά διαλύματα πρέπει να προεκταθεί σε μηδενική συγκέντρωση συνδιαλύτη από τιμές που λαμβάνονται από διάφορα μείγματα συνδιαλύτη.
Αυτά τα γεγονότα επισκιάζονται από την παράλειψη του διαλύτη από την παράσταση που χρησιμοποιείται κανονικά για να ορίσει το pKa, αλλά οι τιμές pKa που λαμβάνονται σε ένα δεδομένο μικτό διαλύτη μπορούν να συγκριθούν μεταξύ τους, δίνοντας σχετική ισχύ οξέος. Το ίδιο συμβαίνει για τις τιμές pKa που λαμβάνονται σε έναν ειδικό μη υδατικό διαλύτη όπως το DMSO.
Μια παγκόσμια κλίμακα, ανεξάρτητη από τον διαλύτη, για τις σταθερές διάστασης οξέων δεν έχει αναπτυχθεί, επειδή δεν υπάρχει γνωστός τρόπος σύγκρισης των πρότυπων καταστάσεων δύο διαφορετικών διαλυτών.
Ο δεύτερος κανόνας του Πόλινγκ λέει ότι η τιμή του πρώτου pKa για τα οξέα του τύπου XOm(OH)n εξαρτάται κυρίως από τον αριθμό τον οξοομάδων m, είναι προσεγγιστικά ανεξάρτητη από τον αριθμό των υδροξυομάδων n καθώς και από το κεντρικό άτομο Χ. Οι προσεγγιστικές τιμές του pKa είναι 8 για m = 0, 2 για m = 1, −3 για m = 2 και < −10 για m = 3.[18] Εναλλακτικά, έχουν προταθεί διάφοροι αριθμητικοί τύποι που συμπεριλαμβάνουν την pKa = 8 − 5n (γνωστός ως κανόνας του Ρόνι Μπελ (Ronnie Bell),[19][36] pKa = 7 − 5n,[20][37] ή pKa = 9 − 7n.[19] Η εξάρτηση από το m σχετίζεται με την κατάσταση οξείδωσης του κεντρικού ατόμου, X: όσο υψηλότερη η οξειδωτική κατάσταση, τόσο πιο ισχυρό το οξυοξύ. Παραδείγματος χάρη, το pKa για το HClO είναι 7,2, για το HClO2 is 2,0, για το HClO3 είναι−1 και το HClO4 είναι ένα ισχυρό οξύ (pKa << 0).[3] Αυτός ο κανόνας μπορεί μπορεί να βοηθήσει στην απόδοση της μοριακής δομής: παραδείγματος χάρη, το φωσφορώδες οξύ (H3PO3) έχει ένα pKa κοντά στο 2 που υποδεικνύει ότι η δομή του είναι HPO(OH)2, όπως επιβεβαιώθηκε αργότερα από την φασματοσκοπία NMR και όχι P(OH)3 που θα αναμενόταν έχοντας μια pKa κοντά στο 8.[37]

Στα οργανικά οξέα επαγωγικά και μεσομερικά φαινόμενα επηρεάζουν τις τιμές pKa. Ένα απλό παράδειγμα δίνεται από την επίδραση της αντικατάστασης των υδρογονοατόμων στο αιθανικό οξύ από το περισσότερο ηλεκτραρνητικό άτομο του χλωρίου. The φαινόμενο αποδοχής ηλεκτρονίων του υποκαταστάτη κάνει τον ιονισμό πιο εύκολο, έτσι οι διαδοχικές τιμές pKa μειώνονται κατά σειρά 4,7, 2,8, 1,4 και 0,7 όταν υπάρχουν 0,1, 2 ή 3 άτομα χλωρίου.[38] Η εξίσωση Hammett equation, παρέχει μια γενική έκφραση για το φαινόμενο των υποκαταστατών.[39]
- log Ka = log Ka0 + ρσ.
Το Ka είναι η σταθερά διάστασης μιας υποκατεστημένης ένωσης, Ka0 είναι η σταθερά διάστασης όταν ο υποκαταστάτης είναι υδρογόνο, ρ είναι μια ιδιότητα της μη υποκατεστημένης ένωσης και το σ έχει μια ιδιαίτερη τιμή για κάθε υποκαταστάτη. Η γραφική παράσταση του log Ka ως προς το σ είναι μια ευθεία γραμμή με αποτέμνουσα y τον log Ka0 και κλίση συνάρτησης ρ. Αυτό είναι ένα παράδειγμα μιας γραμμικής σχέσης ελεύθερης ενέργειας, επειδή ο log Ka είναι ανάλογος την τυπική μεταβολή της ελεύθερης ενέργειας. Ο Hammett διατύπωσε[40] αρχικά τη σχέση με δεδομένα από το βενζοϊκό οξύ με διαφορετικούς υποκαταστάτες στις θέσεις όρθο- και πάρα- της υποκατάστασης αρενίου: μερικές αριθμητικές τιμές υπάρχουν στην εξίσωση Hammett. Αυτή και άλλες μελέτες επέτρεψαν τη διάταξη των υποκαταστατών σύμφωνα με την ισχύ του επαγωγικού φαινομένου (δεκτικότητα ή δοτικότητα ηλεκτρονίων) και τη διάκριση μεταξύ επαγωγικών και μεσομερικών φαινομένων.[41][42]
Οι αλκοόλες δεν συμπεριφέρονται κανονικά ως οξέα στο νερό, αλλά η παρουσία ενός διπλού δεσμού γειτονικά προς την ομάδα OH μπορεί να μειώσει σημαντικά το pKa μέσω του μηχανισμού του κετοενολικού ταυτομερισμού. Το ασκορβικό οξύ είναι ένα παράδειγμα αυτού του φαινομένου. Η δικετόνη 2,4-πεντανοδιόνη (2,4-pentanedione (ακετυλοακετόνη)) είναι επίσης ασθενές οξύ λόγω της κετοενολικής ισορροπίας. Σε αρωματικές ενώσεις, όπως η φαινόλη, που έχει έναν υποκαταστάτη OH, η σύζευξη με τον αρωματικό δακτύλιο ως ένα σύνολο αυξάνει πολύ τη σταθερότητα της αποπρωτονιωμένης μορφής.
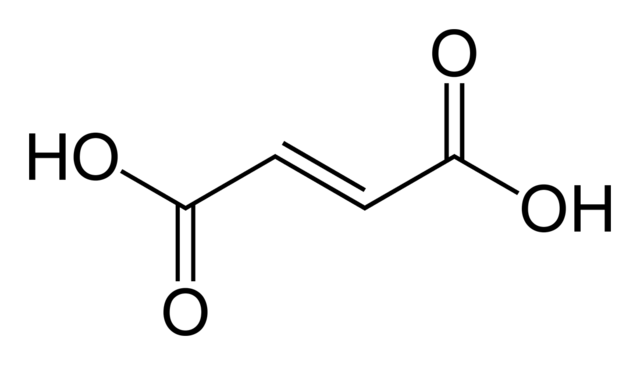
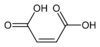
Τα δομικά φαινόμενα μπορεί επίσης να είναι σημαντικά. Η διαφορά μεταξύ φουμαρικού οξέος και μηλεϊνικού οξέος είναι ένα κλασικό παράδειγμα. Το φουμαρικό οξυ είναι (E)-1,4-βουτ-2-ενεδιοϊκό οξύ, ένα trans ισομερές, ενώ το μηλεϊνικό οξύ είναι το αντίστοιχο cis ισομερές, δηλαδή (Z)-1,4-βουτ-2-ενεδιοϊκό οξύ. Το φουμαρικό οξύ έχει τιμές pKa περίπου 3,0 και 4,5. Αντίθετα το μηλεϊνικό οξύ , έχει τιμές pKa περίπου 1,5 και 6,5. Η αιτία για αυτή τη μεγάλη διαφορά είναι ότι όταν ένα πρωτόνιο αφαιρείται από το cis- ισομερές (μηλεϊνικό οξύ) σχηματίζεται ένας ισχυρός διαμοριακός δεσμός υδρογόνου με την κοντινή εναπομένουσα καρβοξυλομάδα. Αυτό ευνοεί τον σχηματισμό του μηλεϊνικού H+ και αντιτίθεται στην αφαίρεση του δεύτερου πρωτονίου από αυτό. Στο trans ισομερές, οι δύο καρβοξυλομάδες είναι πάντα αρκετά μακριά, έτσι δεν παρατηρείται δεσμός υδρογόνου.[43]
Το 1,8-δις(διμεθυλαμινο)ναφθαλίνιο (Proton sponge), έχει μια τιμή pKa 12,1. Είναι μία από τις ισχυρότερες γνωστές αμινοβάσεις. Η υψηλή βασικότητα αποδίδεται στην βοήθεια της τάσης στην πρωτονίωση και στον ισχυρό εσωτερικό δεσμό υδρογόνου.[44][45]
Οι επιδράσεις του διαλύτη και της διάλυσης πρέπει επίσης να αναφερθούν σε αυτήν την ενότητα. Αποδεικνύεται ότι αυτές οι επιρροές είναι πιο μικρές από ότι αυτές του διηλεκτρικού μέσου, που αναφέρθηκε παραπάνω. Παραδείγματος χάρη, η αναμενόμενη (από τις ηλεκτρονικές επιδράσεις των μεθυλο υποκαταστατών) και η παρατηρούμενη σειρά στην αέρια φάση της βασικότητας των μεθυλαμινών, Me3N > Me2NH > MeNH2 > NH3, μεταβάλλεται από το νερό σε Me2NH > MeNH2 > Me3N > NH3. Τα ουδέτερα μόρια μεθυλαμίνης είναι ενωμένα με δεσμούς υδρογόνου στα μόρια του νερού κυρίως μέσα από μια αλληλεπίδραση δέκτη, N-HOH και μόνο ευκαιριακά απλώς με έναν περισσότερο δεσμό δότη, NH-OH2. Συνεπώς, οι μεθυλαμίνες σταθεροποιούνται περίπου στην ίδια έκταση με εφυδάτωση, ανεξάρτητα από τον αριθμό των μεθυλομάδων. Εντελώς αντίθετα, τα αντίστοιχα κατιόντα μεθυλαμμωνίου χρησιμοποιούν πάντα όλα τα διαθέσιμα πρωτόνια ως δότες δεσμού NH-OH2. Η σχετική σταθεροποίηση των ιόντων μεθυλαμμωνίου συνεπώς μειώνεται με τον αριθμό των μεθυλομάδων εξηγώντας τη σειρά βασικότητας των μεθυλαμινών στο νερό.[46]
Θερμοδυναμική
Μια σταθερά ισορροπίας σχετίζεται με την μεταβολή της πρότυπης ελεύθερης ενέργειας Gibbs για την αντίδραση, συνεπώς για νια σταθερά διάστασης οξέος
Το R είναι η σταθερά των αερίων και T είναι η θερμοκρασία στη κλίμακα Κέλβιν. Σημειώστε ότι η pKa= −log Ka και 2,303 ≈ ο φυσικός λογάριθμος του 10. Στους 25 °C ΔG![]() in kJ·mol−1 = 5.708 pKa (1 kJ·mol−1 = 1000 Τζάουλ (μονάδα μέτρησης) ανά mole). Η ελεύθερη ενέργεια αποτελείται από έναν όρο ενθαλπίας και έναν όρο εντροπίας.[7]
in kJ·mol−1 = 5.708 pKa (1 kJ·mol−1 = 1000 Τζάουλ (μονάδα μέτρησης) ανά mole). Η ελεύθερη ενέργεια αποτελείται από έναν όρο ενθαλπίας και έναν όρο εντροπίας.[7]
Η μεταβολή της πρότυπης ενθαλπίας μπορεί να προσδιοριστεί θερμιδομετρικά ή χρησιμοποιώντας την εξίσωση Βαν'τ Χοφ, αν και η θερμιδομετρική μέθοδος προτιμάται. Όταν και η μεταβολή της πρότυπης ενθαλπίας και η σταθερά διάστασης οξέος έχουν προσδιοριστεί, η μεταβολή της πρότυπης εντροπίας υπολογίζεται εύκολα από την παραπάνω εξίσωση. Στον παρακάτω πίνακα, οι όροι της εντροπίας υπολογίζονται από τις πειραματικές τιμές της pKa και της ΔH![]() . Τα δεδομένα αναφέρονται στους 25 °C και μηδενική ιοντική ισχύ, στο νερό.[7]
. Τα δεδομένα αναφέρονται στους 25 °C και μηδενική ιοντική ισχύ, στο νερό.[7]
| Ένωση | Ισορροπία | pKa | ΔG | ΔH | —TΔS |
|---|---|---|---|---|---|
| HA = Αιθανικό οξύ | HA | 4,756 | 27,147† | −0,41 | 27,56‡ |
| H2A+ = ΓλυκίνηH+ | H2A+ | 2,351 | 13,420 | 4,00 | 9,419 |
| HA | 9,78 | 55,825 | 44,20 | 11,6 | |
| H2A = Μηλεϊνικό οξύ | H2A | 1,92 | 10,76 | 1,10 | 9,85 |
| HA− | 6,27 | 35,79 | −3,60 | 39,4 | |
| H3A = Κιτρικό οξύ | H3A | 3,128 | 17,855 | 4,07 | 13,78 |
| H2A− | 4,76 | 27,176 | 2,23 | 24,9 | |
| HA2− | 6,40 | 36,509 | −3,38 | 39,9 | |
| H3A = Βορικό οξύ | H3A | 9,237 | 52,725 | 13,80 | 38,92 |
| H3A = Φωσφορικό οξύ | H3A | 2,148 | 12,261 | −8,00 | 20,26 |
| H2A− | 7,20 | 41,087 | 3,60 | 37,5 | |
| HA2− | 12,35 | 80,49 | 16,00 | 54,49 | |
| HA− = Όξινο θειώδες | HA− | 1,99 | 11,36 | −22,40 | 33,74 |
| H2A = Αιθανοδιικό οξύ | H2A | 1,27 | 7,27 | −3,90 | 11,15 |
| HA− | 4,266 | 24,351 | 7,00 | 31,35 |
- † ΔG
 = 2,303RT pKa
= 2,303RT pKa - ‡ Εδώ υπολογισμένο, από τις τιμές ΔH και ΔG που παρέχονται στην παραπομπή, χρησιμοποιώντας —TΔS
 = ΔG
= ΔG — ΔH
— ΔH
| Ένωση | Ισορροπία | pKa | ΔH | —TΔS |
|---|---|---|---|---|
| B = Αμμωνία | HB+ | 9,245 | 51,95 | 0,8205 |
| B = Μεθυλαμίνη | HB+ | 10,645 | 55,34 | 5,422 |
| B = Τριαιθυλαμίνη | HB+ | 10,72 | 43,13 | 18,06 |
Σημειώσεις: Πρώτη, όταν pKa είναι θετικό, η μεταβολή της πρότυπης ελεύθερης ενέργειας για την αντίδραση διάστασης είναι επίσης θετική. Δεύτερη, μερικές αντιδράσεις είναι εξώθερμες και μερικές ενδόθερμες , αλλά, όταν ΔH![]() είναι αρνητικό −TΔS
είναι αρνητικό −TΔS![]() είναι ο κυρίαρχος παράγοντας, που καθορίζει ότι ΔG
είναι ο κυρίαρχος παράγοντας, που καθορίζει ότι ΔG![]() είναι θετικό. Τελευταία, η συμβολή της εντροπίας είναι πάντα δυσμενής (ΔS
είναι θετικό. Τελευταία, η συμβολή της εντροπίας είναι πάντα δυσμενής (ΔS![]() < 0) σε αυτές τις αντιδράσεις. Τα ιόντα στα υδατικά διαλύματα τείνουν να προσανατολίζουν τα περιβάλλοντα μόρια νερού, που διατάσσουν το διάλυμα και μειώνουν την εντροπία. Η συνεισφορά ενός ιόντος στην εντροπία είναι η μερική μοριακή εντροπία που είναι συχνά αρνητική, ειδικά για μικρά ή υψηλά φορτισμένα ιόντα.[47] Ο ιονισμός ενός ουδέτερου οξέος περιλαμβάνει τη δημιουργία δύο ιόντων έτσι ώστε η εντροπία να μειώνεται (ΔS
< 0) σε αυτές τις αντιδράσεις. Τα ιόντα στα υδατικά διαλύματα τείνουν να προσανατολίζουν τα περιβάλλοντα μόρια νερού, που διατάσσουν το διάλυμα και μειώνουν την εντροπία. Η συνεισφορά ενός ιόντος στην εντροπία είναι η μερική μοριακή εντροπία που είναι συχνά αρνητική, ειδικά για μικρά ή υψηλά φορτισμένα ιόντα.[47] Ο ιονισμός ενός ουδέτερου οξέος περιλαμβάνει τη δημιουργία δύο ιόντων έτσι ώστε η εντροπία να μειώνεται (ΔS![]() < 0). Στον δεύτερο ιονισμό του ίδιου οξέος, υπάρχουν τώρα τρία ιόντα και το ανιόν έχει ένα φορτίο, συνεπώς η εντροπία πάλι μειώνεται.
< 0). Στον δεύτερο ιονισμό του ίδιου οξέος, υπάρχουν τώρα τρία ιόντα και το ανιόν έχει ένα φορτίο, συνεπώς η εντροπία πάλι μειώνεται.
Σημειώστε ότι η μεταβολή της πρότυπης ελεύθερης ενέργειας για την αντίδραση είναι για τις μεταβολές από τα αντιδρώντα στις πρότυπες τους καταστάσεις προς τα προϊόντα στις πρότυπες τους καταστάσεις. Η μεταβολή της ελεύθερης ενέργειας στην ισορροπία είναι μηδέν, επειδή τα χημικά δυναμικά των αντιδρώντων και των προϊόντων είναι ίσα στην ισορροπία.

.
Ο πειραματικός προσδιορισμός των τιμών της pKa εκτελείται συνήθως μέσω τιτλοδοτήσεων, σε ένα μέσο υψηλής ιοντικής ισχύος και σε σταθερή θερμοκρασία.[48] Μια τυπική διεργασία μπορεί να έχει ως ακολούθως. Ένα διάλυμα της ένωσης στο μέσο οξειδώνεται με ένα ισχυρό οξύ στο σημείο όπου η ένωση είναι πλήρως πρωτονιωμένη. Το διάλυμα τιτλοδοτείται έπειτα με μια ισχυρή βάση μέχρι να αφαιρεθούν όλα τα πρωτόνια. Σε κάθε σημείο της τιτλοδότησης μετριέται το pH χρησιμοποιώντας ένα ηλεκτρόδιο υάλου και ένα πεχάμετρο. Οι σταθερές ισορροπίας βρίσκονται ταιριάζοντας τις υπολογισμένες τιμές pH στις παρατηρούμενες τιμές, χρησιμοποιώντας τη μέθοδο των ελαχίστων τετραγώνων.[49]
Ο συνολικός όγκος της προστιθέμενης ισχυρής βάσης πρέπει να είναι μικρός συγκρινόμενος με τον αρχικό όγκο του ογκομετρούμενου διαλύματος για να διατηρηθεί η ιοντική ισχύς σχεδόν σταθερή. Αυτό θα εξασφαλίσει ότι η pKa παραμένει αμετάβλητη κατά τη διάρκεια της τιτλοδότησης.
Μια υπολογισμένη καμπύλη τιτλοδότησης για το αιθανοδιικό οξύ παρουσιάζεται στα δεξιά. Το αιθανοδιικό οξύ έχει τιμές pKa 1,27 και 4,27. Συνεπώς οι περιοχές ρύθμισης θα επικεντρωθούν περίπου σε pH 1,3 και pH 4,3. Οι περιοχές ρύθμισης μεταφέρουν τις απαραίτητες πληροφορίες για τη λήψη τιμών pKa καθώς οι συγκεντρώσεις του οξέος και της συζυγούς βάσης αλλάζουν μαζί με την περιοχή ρύθμισης.
Μεταξύ των δύο περιοχών ρύθμισης υπάρχει ένα τελικό σημείο, ή ισοδύναμο σημείο, όπου το pH αυξάνεται κατά περίπου δύο μονάδες. Αυτό το τελικό σημείο δεν είναι απότομο και είναι τυπικό ενός διπρωτικού οξέος του οποίου οι περιοχές ρύθμισης επικαλύπτονται κατά μικρή ποσότητα: το pKa2 − pKa1 είναι περίπου τρία σε αυτό το παράδειγμα. (Αν η διαφορά στις τιμές pK ήταν περίπου δύο ή λιγότερο, το τελικό σημείο το τελικό σημείο δεν ήταν εμφανές.) Το δεύτερο τελικό σημείο ξεκινά περίπου στο pH 6,3 και είναι απότομο. Αυτό δείχνει ότι όλα τα πρωτόνια έχουν αφαιρεθεί. Όταν συμβαίνει αυτό, το διάλυμα δεν ρυθμίζεται και το pH αυξάνεται απότομα με την προσθήκη μιας μικρής ποσότητας ισχυρής βάσης. Όμως, το pH δεν συνεχίζει να αυξάνεται απεριόριστα. Μια νέα περιοχή ρύθμισης ξεκινά σε pH περίπου 11 (pKw − 3), που είναι εκεί όπου ο αυτοϊονισμός του νερού γίνεται σημαντικός.
Είναι πολύ δύσκολο να μετρηθούν οι τιμές pH που είναι μικρότερες από δύο σε υδατικό διάλυμα με ένα ηλεκτρόδιο υάλου, επειδή ο νόμος του Nernst έχει πρόβλημα σε τέτοιες χαμηλές τιμές pH. Για να προσδιοριστούν οι τιμές pK που είναι μικρότερες από περίπου 2 ή μεγαλύτερες από περίπου 11 μπορεί να χρησιμοποιηθούν μετρήσεις φασματοφωτομετρίας[50] [51] ή NMR,[12][52] ή σε συνδυασμό με μετρήσεις pH.
Όταν το ηλεκτρόδιο υάλου δεν μπορεί να χρησιμοποιηθεί, όπως με τα μη υδατικά διαλύματα, χρησιμοποιούνται συχνά φασματοφωτομετρικές μέθοδοι.[27] Αυτές μπορεί να περιλαμβάνουν μετρήσεις απορρόφησης ή φθορισμού. Και στις δυο περιπτώσεις η μετρούμενη ποσότητα θεωρείται ότι είναι ανάλογη προς το άθροισμα των συνεισφορών από κάθε φωτοενεργό είδος· με τις μετρήσεις απορρόφησης θεωρείται ότι εφαρμόζεται ο νόμος Beer-Lambert.
Τα υδατικά διαλύματα με κανονικό νερό δεν μπορούν να χρησιμοποιηθούν για μετρήσεις NMR του 1H, αλλά πρέπει να χρησιμοποιηθεί το βαρύ ύδωρ, D2O. Τα δεδομένα NMR του 13C, όμως, μπορούν να χρησιμοποιηθούν με κανονικό νερό και φάσματα NMR 1Η με μη υδατικά μέσα. Οι μετρούμενες ποσότητες με NMR είναι χημικές μετατοπίσεις μέσου χρόνου, επειδή η ανταλλαγή πρωτονίων είναι γρήγορη στην κλίμακα χρόνου του NMR. Άλλες χημικές μετατοπίσεις, όπως αυτές του 31P μπορούν επίσης να μετρηθούν.
Μικροσταθερές

Μια βάση όπως η σπερμίνη έχει λίγες διαφορετικές θέσεις όπου μπορεί να συμβεί πρωτονίωση. Σε αυτό το παράδειγμα, το πρώτο πρωτόνιο μπορεί να πάει στην τελική ομάδα -NH2, ή στις εσωτερικές ομάδες -NH-. Οι τιμές pKa για τη διάσταση της πρωτονιωμένης σπερμίνης στη μία ή την άλλη θέση είναι παραδείγματα μικροσταθερών ισορροπίας. Δεν μπορούν να προσδιοριστούν άμεσα μέσω μετρήσεων του pH, της απορρόφησης, του φθορισμού, ή NMR. Παρόλα αυτά, η θέση της πρωτονίωσης είναι πολύ σημαντική για βιολογική λειτουργία, έτσι έχουν αναπτυχθεί μαθηματικές μέθοδοι για τον προσδιορισμό των μικροσταθερών.[53]
Η γνώση των τιμών pKa είναι σημαντική για την ποσοτική επεξεργασία των συστημάτων που περιλαμβάνουν ισορροπίες οξέος-βάσης σε διάλυμα. Πολλές εφαρμογές υπάρχουν στη βιοχημεία· παραδείγματος χάρη, οι τιμές pKa των πρωτεϊνών και των πλευρικών αλυσίδων των αμινοξέων είναι μεγάλης σημασίας για τη δραστικότητα των ενζύμων και τη σταθερότητα των πρωτεϊνών.[54] Οι τιμές pKa των πρωτεϊνών δεν μπορούν πάντα να μετρηθούν άμεσα, αλλά μπορούν να υπολογιστούν χρησιμοποιώντας θεωρητικές μεθόδους. Τα ρυθμιστικά διαλύματα χρησιμοποιούνται εκτεταμένα για να παράσχουν διαλύματα στο ή κοντά στο φυσιολογικό pH για τη μελέτη των βιοχημικών αντιδράσεων·[55] ο σχεδιασμός αυτών των διαλυμάτων εξαρτάται από τη γνώση των τιμών pKa των συστατικών τους. Σημαντικά ρυθμιστικά διαλύματα περιλαμβάνουν MOPS, που δίνουν ένα διάλυμα με pH 7,2 και την τρικίνη, που χρησιμοποιείται στην ηλεκτροφόρηση πηκτής.[56][57] Η ρύθμιση είναι ένα βασικό τμήμα της φυσιολογίας οξέος-βάσης που περιλαμβάνει την οξεοβασική ισορροπία,[58] και είναι βασική στην κατανόηση διαταραχών όπως η ανισορροπία οξέων-βάσεων.[59][60][61] Το ισοηλεκτρικό σημείο ενός δεδομένου μορίου είναι μια συνάρτηση των τιμών του pK, έτσι διαφορετικά μόρια έχουν διαφορετικά ισοηλεκτρικά σημεία. Αυτό επιτρέπει μια τεχνική που λέγεται ισοηλεκτρική εστίαση,[62] που χρησιμοποιείται στον διαχωρισμό των πρωτεϊνών με δισδιάστατη ηλεκτροφόρηση πηκτής.
Τα ρυθμιστικά διαλύματα παίζουν επίσης βασικό ρόλο στην αναλυτική χημεία. Χρησιμοποιούνται όποτε υπάρχει ανάγκη για τη ρύθμιση του pH ενός διαλύματος σε μια συγκεκριμένη τιμή. Συγκρινόμενο με ένα υδατικό διάλυμα, το pH ενός ρυθμιστικού διαλύματος είναι σχετικά ανθεκτικό στην προσθήκη μικρής ποσότητας ισχυρού οξέος ή ισχυρής βάσης. Η ικανότητα ρύθμισης[63] ενός απλού ρυθμιστικού διαλύματος είναι μέγιστη όταν pH = pKa. Στην εκχύλιση οξέος-βάσης, η αποτελεσματικότητα της εκχύλισης μιας ένωσης σε μια οργανική φάση, όπως ένας αιθέρας, μπορεί να βελτιστοποιηθεί ρυθμίζοντας το pH της υδατικής φάσης χρησιμοποιώντας ένα κατάλληλο ρυθμιστικό. Στο βέλτιστο pH, η συγκέντρωση του ηλεκτρικά ουδέτερου είδους μεγιστοποιείται· ένα τέτοιο είδος είναι πιο διαλυτό σε οργανικούς διαλύτες που έχουν μικρή διηλεκτρική σταθερά από ότι είναι στο νερό. Αυτή η τεχνική χρησιμοποιείται για τον καθαρισμό των ασθενών οξέων και βάσεων.[64]
Ένας πεχαμετρικός δείκτης είναι ένα ασθενές οξύ ή μια ασθενής βάση που αλλάζει χρώμα στη μετάβαση της περιοχής pH, που είναι περίπου pKa ± 1. Ο σχεδιασμός ενός γενικού δείκτη απαιτεί ένα μείγμα δεικτών των οποίων οι γειτονικές τιμές pKa διαφέρουν περίπου κατά δύο, έτσι ώστε οι περιοχές μετάβασης του pH τους μόλις να επικαλύπτονται.
Στη φαρμακολογία ο ιονισμός μιας ένωσης αλλάζει τη φυσική της συμπεριφορά και οι μακροϊδιότητες όπως η διαλυτότητα και ο συντελεστής κατανομής/λιποφιλία (log p). Παραδείγματος χάρη, ο ιονισμός οποιασδήποτε ένωσης θα αυξήσει τη διαλυτότητα στο νερό, αλλά θα μειώσει τη λιποφιλία. Αυτό χρησιμοποιείται στην ανάπτυξη των φαρμάκων για να αυξήσει τη συγκέντρωση μιας ένωσης στο αίμα ρυθμίζοντας το pKa μιας ιονίσιμης ομάδας.[65]
Η γνώση των τιμών pKa είναι σημαντική στην κατανόηση των συμπλόκων συναρμογής, που σχηματίζονται από την αλληλεπίδραση ενός μεταλλικού ιόντος, Mm+, που δρα ως οξύ Λιούις, με έναν υποκαταστάτη, L, που δρα ως βάση Λιούις. Όμως, ο υποκαταστάτης μπορεί επίσης να υποστεί αντιδράσεις πρωτονίωσης, έτσι ο σχηματισμός ενός συμπλόκου σε υδατικό διάλυμα μπορεί να αναπαρασταθεί συμβολικά με την αντίδραση
- [M(H2O)n]m+ +LH
 [M(H2O)n−1L](m−1)+ + H3O+
[M(H2O)n−1L](m−1)+ + H3O+
- [M(H2O)n]m+ +LH
Για τον προσδιορισμό της σταθεράς ισορροπίας αυτής της αντίδρασης, στην οποία ο υποκαταστάτης χάνει ένα πρωτόνιο, το pKa του πρωτονιωμένου υποκαταστάτη πρέπει να είναι γνωστό. Στην πράξη, ο υποκαταστάτης μπορεί να είναι πολυπρωτικός· παραδείγματος χάρη το EDTA4− μπορεί να δεχθεί τέσσερα πρωτόνια· σε αυτήν την περίπτωση, όλες οι τιμές pKa πρέπει να είναι γνωστές. Επιπλέον, το μεταλλικό ιόν υπόκειται σε υδρόλυση, δηλαδή, συμπεριφέρεται ως ασθενές οξύ, έτσι οι τιμές pK για τις αντιδράσεις υδρόλυσης πρέπει να είναι γνωστές.[66] Η αξιολόγηση του κινδύνου που σχετίζεται με ένα οξύ ή μια βάση μπορεί να απαιτήσει τη γνώση των τιμών pKa.[67] Παραδείγματος χάρη, το υδροκυάνιο είναι ένα πολύ τοξικό αέριο, επειδή το ιόν κυανίου αναστέλλει το ένζυμο οξειδάση του κυτοχρώματος c που περιέχει σίδηρο. Το υδροκυάνιο είναι ένα ασθενές οξύ σε υδατικά διαλύματα με pKa περίπου 9. Σε ισχυρά αλκαλικά διαλύματα, πάνω από pH 11, το κυανιούχο νάτριο είναι «πλήρως διιστάμενο», έτσι ο κίνδυνος λόγω του αερίου υδροκυανίου μειώνεται κατά πολύ. Ένα όξινο διάλυμα, αφ' ετέρου, είναι πολύ επικίνδυνο επειδή όλο το κυανίδιο είναι στην μορφή του οξέος. Η κατάποση του κυανιδίου από το στόμα είναι δυνητικά μοιραία, ανεξάρτητα από το pH, λόγω της αντίδρασης με την οξειδάση του κυτοχρώματος c.
Στην περιβαντολογία οι ισορροπίες οξέος-βάσης είναι σημαντικές για τις λίμνες[68] και τους ποταμούς·[69][70] παραδείγματος χάρη, τα χουμικά οξέα είναι σημαντικά συστατικά των φυσικών υδάτων. Ένα άλλο παράδειγμα εμφανίζεται στην χημική ωκεανογραφία:[71] για τον ποσοτικό προσδιορισμό της διαλυτότητας του σιδήρου(III) στο θαλασσινό νερό σε διαφορετικές αλμυρότητες, οι τιμές pKa για τον σχηματισμό των προϊόντων υδρόλυσης του σιδήρου(III) Fe(OH)2+, Fe(OH)2+ και Fe(OH)3 προσδιορίζονται, μαζί με το γινόμενο διαλυτότητας του υδροξειδίου του σιδήρου.[72]
Υπάρχουν πολλές τεχνικές για τον προσδιορισμό του pKa μιας χημικής ουσίας, που οδηγεί σε κάποιες διαφορές μεταξύ των διαφορετικών πηγών. Οι καλά μετρημένες τιμές μπορεί να διαφέρουν μεταξύ τους μέχρι 0,1 μονάδα, συνήθως. Τα δεδομένα που παρουσιάζονται εδώ ελήφθησαν στους 25 °C σε νερό.[3][73] Περισσότερες τιμές μπορούν να βρεθούν παραπάνω στη #Θερμοδυναμική.
| Χημικό όνομα | Ισορροπία | pKa |
|---|---|---|
| BH = Αδενίνη | BH |
4,17 |
| BH2+ |
9,65 | |
| H3A = Αρσενικικό οξύ | H3A |
2,22 |
| H2A− |
6,98 | |
| HA2− |
11,53 | |
| HA = Βενζοϊκό οξύ | HA |
4,204 |
| HA = Βουτανικό οξύ | HA |
4,82 |
| H2A = Χρωμικό οξύ | H2A |
0,98 |
| HA− |
6,5 | |
| B = Κωδεΐνη | BH+ |
8,17 |
| HA = Κρεζόλη | HA |
10,29 |
| HA = Μεθανικό οξύ | HA |
3,751 |
| HA = Υδροφθορικό οξύ | HA |
3,17 |
| HA = Υδροκυανικό οξύ | HA |
9,21 |
| HA = Υδροσελήνιο | HA |
3,89 |
| HA = Υπεροξείδιο του υδρογόνου (90%) | HA |
11,7 |
| HA = 2-υδροξυπροπανικό οξύ | HA |
3,86 |
| HA = Προπανικό οξύ | HA |
4,87 |
| HA = Φαινόλη | HA |
9,99 |
| H2A = L-(+)-Ασκορβικό οξύ | H2A |
4,17 |
| HA− |
11,57 |
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.

![{\displaystyle K_{\mathrm {a} }=\mathrm {\frac {[A^{-}][H^{+}]}{[HA]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/4df1424aa532585fc7ad6dd660a596705ee31a2b)


![{\displaystyle K^{\ominus }=\mathrm {{\frac {[A^{-}][H_{3}O^{+}]}{[HA][H_{2}O]}}\times {\frac {\gamma _{A^{-}}\ \gamma _{H_{3}O^{+}}}{\gamma _{HA}\ \gamma _{H_{2}O}}}=\mathrm {\frac {[A^{-}][H_{3}O^{+}]}{[HA][H_{2}O]}} \times \Gamma } }](http://wikimedia.org/api/rest_v1/media/math/render/svg/ef7fc9fca5864aabf89fb0ea85782fe1b6f30b68)

![{\displaystyle \mathrm {pH} =\mathrm {p} K_{\mathrm {a} }+\log \mathrm {\frac {[A^{-}]}{[HA]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/1e741bfd0c07772fa2abd205e79cd865a398268e)

![{\displaystyle K_{\mathrm {a} }=\mathrm {\frac {[H_{3}O^{+}][OH^{-}]}{[H_{2}O]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/64d435a42d84f7442530c948268614ed1b03685a)
![{\displaystyle K_{\mathrm {w} }=[\mathrm {H_{3}O} ^{+}][\mathrm {OH} ^{-}]\,}](http://wikimedia.org/api/rest_v1/media/math/render/svg/b28e22a7001351bdc196d0c1d2e7ea94f3b2842f)
![{\displaystyle K_{\mathrm {b} }=\mathrm {\frac {[HB^{+}][OH^{-}]}{[B]}} }](http://wikimedia.org/api/rest_v1/media/math/render/svg/5e8602a5fa0751164332991a802fe0f0a9226ba2)
![{\displaystyle \mathrm {[OH^{-}]} ={\frac {K_{\mathrm {w} }}{\mathrm {[H^{+}]} }}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/ab7f583da9f8b50145990ffa4342919930edfa16)
![{\displaystyle K_{\mathrm {b} }={\frac {[\mathrm {HB^{+}} ]K_{\mathrm {w} }}{\mathrm {[B][H^{+}]} }}={\frac {K_{\mathrm {w} }}{K_{\mathrm {a} }}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/55e99b9289faff1c69f7cc5b289e461e363515a5)

