Sauerstoffdifluorid
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Sauerstoffdifluorid ist ein Fluorid des Sauerstoffs mit der Summenformel OF2. Es gehört zu den Sauerstofffluoriden und ist einer von sehr wenigen Stoffen, in dem Sauerstoff mit einer positiven Oxidationszahl auftritt. Der manchmal verwendete Name Difluoroxid für diese Verbindung ist falsch, weil Sauerstoff in Oxiden eine negative Oxidationszahl besitzt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
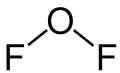 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Sauerstoffdifluorid | |||||||||||||||
| Andere Namen |
Difluoroxid | |||||||||||||||
| Summenformel | OF2 | |||||||||||||||
| Kurzbeschreibung |
farbloses Gas mit widerlichem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 54,00 g·mol−1 | |||||||||||||||
| Aggregatzustand |
gasförmig | |||||||||||||||
| Dichte |
2,42 g·l−1 (0 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (68 cm3/l bei 0 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
Schweiz: 0,05 ml·m−3 bzw. 0,1 mg·m−3[4] | |||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Gewinnung und Darstellung
Über Sauerstoffdifluorid wurde 1929 das erste Mal berichtet, dargestellt wurde es bei der Elektrolyse von geschmolzenem Kaliumfluorid und Fluorwasserstoff in Wasser. Heutzutage wird Sauerstoffdifluorid durch Einleiten von Fluor in Natronlauge oder Kalilauge gewonnen:[5]
Eigenschaften
Zusammenfassung
Kontext
Sauerstoffdifluorid ist eines der stärksten bekannten Oxidationsmittel, das sogar mit dem Edelgas Xenon zu Xenontetrafluorid (XeF4) reagieren kann:
Grund für diese Reaktion ist die starke Elektronegativität von Fluor und Sauerstoff, welcher in Sauerstoffdifluorid eine positive Partialladung hat.
In Wasser ist es wenig löslich,[3] gelöst reagiert Sauerstoffdifluorid mit Wasser zu Fluorwasserstoff und Sauerstoff (Komproportionierung)[2]:
Es kondensiert bei −144,8 °C zu einer orangefarbenen Flüssigkeit, die von der Struktur her an Wasser erinnert. Der Bindungswinkel, den die beiden O-F-Bindungen einschließen, beträgt 103°, die Bindungslänge der O-F-Bindungen jeweils 140,5 pm.

Verwendung
Sauerstoffdifluorid wurde als Oxidationsmittel für Raketentreibstoffe[6] untersucht, da es einen hohen spezifischen Impuls liefert (z. B. zusammen mit Lithiumhydrid 4112 m/s.[7]).
Sicherheitshinweise
Aufgrund seiner extrem starken oxidierenden Wirkung ist Sauerstoffdifluorid ein für Mensch und Tier gefährlicher Stoff. Es erzeugt nach Einatmung heftige Atembeschwerden, die oft erst nach mehreren Stunden einsetzen und stundenlang anhalten.[8]
Weblinks
Commons: Sauerstoffdifluorid – Sammlung von Bildern, Videos und Audiodateien
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.






