Lokalanästhetikum
Wirkstoff zur örtlich begrenzten Narkose Aus Wikipedia, der freien Enzyklopädie
Als Lokalanästhetikum (Plural Lokalanästhetika) wird ein Anästhetikum zur örtlichen Betäubung (Lokalanästhesie) bezeichnet. Man unterscheidet injizierbare Lokalanästhetika und externe (äußerliche) Lokalanästhetika („Kontaktanästhetika“, Oberflächenanästhetika), die direkt auf Haut- oder Schleimhaut aufgetragen werden. Es gibt Wirkstoffe, die in beiden Formen zur Verfügung stehen. Obwohl deren Ursprung meist auf das Kokain zurückzuführen ist, besitzen die modernen Wirkstoffe keine euphorisierende oder suchterzeugende Wirkung. Sie dürfen nicht mit Betäubungsmitteln im Sinne des Betäubungsmittelgesetzes, wie Morphin oder Heroin, verwechselt werden.
Geschichte
Zusammenfassung
Kontext
Obwohl bereits die Inkas Kokablätter zur Lokalanästhesie nutzten, dauerte es bis in die Mitte des 19. Jahrhunderts, bis sich eine naturwissenschaftlich begründete Nutzung durchsetzte. 1859 isolierte der Goslarer Chemiker Alfred Niemann erstmals Kokain an der chemischen Fakultät in Göttingen und beschrieb dessen lokalanästhetische Wirkung. 1884 führte der Wiener Ophthalmologe Carl Koller erstmals eine schmerzfreie Augenoperation mit Kokain durch. Die erste Leitungsanästhesie unternahm der Chirurg William Halsted 1884, indem er den Nervus alveolaris inferior am Foramen mandibulae mit Kokain betäubte. Die Infiltrationsanästhesie führte Carl Ludwig Schleich 1892 ein. 1899 injizierte August Bier Kokain in den Wirbelkanal und erfand damit die Spinalanästhesie oder sogar (versehentlich) die Periduralanästhesie. 1905 entwickelte Bier auch das Verfahren der intravenösen Regionalanästhesie. Die Periduralanästhesie wurde 1920 durch Fidel Pagés etabliert.[1]
Zunächst wurde vor allem Kokain eingesetzt. 1903 (vorgeschlagen 1897) verlängerte der Leipziger Chirurg Heinrich Braun durch Beigabe von Adrenalin die Wirkdauer von Kokain in der Anästhesie.[2] Die ersten als Ersatz für Kokain dienenden synthetischen Lokalanästhetika, die sich in der medizinischen Praxis (Chirurgie) durchsetzten, waren Stovain von Ernest Fourneau 1903, in der klinischen Praxis vom französischen Chirurgen Paul Reclus erprobt, und Novocain von Alfred Einhorn 1904, in der klinischen Praxis von Heinrich Braun 1906 erprobt. Andere Vorläufer wie Benzocain (Anästhesin, 1890, Eduard Ritsert[3]), Nirvanin (1898, Einhorn), Eukain (Georg Merling 1897), konnten sich nicht durchsetzen. 1948 kam mit Lidocain, das durch die schwedischen Chemiker Nils Löfgren und Bengt Lundqvist im Jahre 1943 synthetisiert worden war[4], erstmals ein Lokalanästhetikum vom Amidtyp auf den Markt.[1] Es wurden seither immer wieder weitere Lokalanästhetika entwickelt, so wurde 1955 Chlorprocain eingeführt.[5]
In der zweiten Hälfte des 19. Jahrhunderts wurde in Zahnheilkunde auch Chlorethan als Lokalanästhetikum verwendet, so 1888 durch den Schweizer Camille Redard (1841–1910) zur Kälteanästhesie.[6]
Chemische Struktur
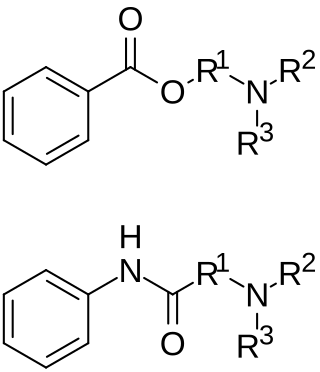
Die chemische Struktur vieler Lokalanästhetika ist ähnlich. Sie bestehen aus einer lipophilen aromatischen Ringstruktur, einer Zwischenkette und einer hydrophilen Aminogruppe. Nach der Zwischenkette unterscheidet man Aminoester (Lokalanästhetika vom „Ester-Typ“ mit Esterbindung wie sie zuerst beim Procain vorlag) und Aminoamide (Lokalanästhetika vom „Amid-Typ“ mit Säureamidbindung). Die Aminoester werden im Gewebe durch eine Cholinesterase metabolisiert. Der Abbau der Aminoamide erfolgt in der Leber durch N-Dealkylierung oder Hydrolyse.
Wirkungsmechanismus
Zusammenfassung
Kontext
Lokalanästhetika entfalten ihre Wirkung an der Zellmembran von Nervenzellen. Hier blockieren sie Natriumkanäle und verhindern dadurch den Einstrom von Natriumionen in die Zelle und somit die Bildung von Aktionspotentialen. In höheren Konzentrationen wird zusätzlich der Kaliumkanal blockiert und Kaliumionen gehindert, aus dem Zellinneren auszuströmen. Damit wird die Bildung und Fortleitung von Empfindungen wie Temperatur, Druck oder Schmerz und die Überleitung motorischer Impulse an dieser Stelle abgeschwächt oder ganz unterbrochen.
Die meisten Lokalanästhetika sind schwach basische Amine und liegen bei physiologischem pH-Wert in geladener und ungeladener Form vor. Der Wirkort liegt an der Innenseite der Natriumkanäle in der Zellmembran, daher ist eine Diffusion der Substanzen in das Zellplasma notwendig. Nur die ungeladene Base kann durch die Zellmembran ins Innere gelangen, wird hier zur geladenen Ammonium-Form protoniert, welche auch die aktive Form des Lokalanästhetikums darstellt, gelangt an die Bindungsstelle des Natriumkanals und entfaltet dort ihre Wirkung.
Die Lokalanästhetika haben einen pKS-Wert zwischen 7 und 9. Wasserlöslich sind sie nur in der ionisierten (protonierten) Form, d. h. bei pH-Werten unter dem jeweiligen pKS-Wert. Daher werden sie in Injektionslösungen mit einem pH von 4–6 verabreicht. Im Gewebe mit einem pH-Wert von 7,4 wird die Injektionslösung abgepuffert und es liegen je nach pKS-Wert des Lokalanästhetikums 2–30 % des Lokalanästhetikums in der nichtionisierten, lipidlöslichen Form vor. Wirksam ist das Anästhetikum jedoch nur in der ionisierten Form, so dass ab einem pH-Wert von 9 alle Lokalanästhetika unwirksam werden. Umgekehrt kann auch ein niedriger pH-Wert, wie er beispielsweise im entzündeten Gewebe (pH ≤ 6) herrscht, dazu führen, dass das Lokalanästhetikum nicht in die Nervenfasern eindringen kann und ebenfalls unwirksam bleibt.
Anwendung
Zusammenfassung
Kontext
Präparate dieser Art werden fast ausschließlich zur Schmerzausschaltung bei medizinischen Prozeduren wie z. B. Operationen und zur Schmerztherapie eingesetzt. In der Chirurgie und vor allem in der Anästhesie haben sich im Laufe der Zeit vielfältige Methoden zur Lokalanästhesie entwickelt. Diese reichen von einfachen Infiltrationsanästhesien bis hin zur Anlage von rückenmarksnahen Schmerzkathetern (Periduralanästhesie).
Bei der Spinalanästhesien wird das Lokalanästhetikum in den Subarachnoidalraum des Spinalkanals gespritzt; dort liegt das Rückenmark (bis etwa zum 12. Brustwirbelkörper, darunter Nervenstränge, die weiter nach unten ziehen) in einer Flüssigkeit, dem Liquor cerebrospinalis. Für diese Art der Betäubung gibt es spezielle Zubereitungen, denen Glukoselösung beigemischt wurde. Diese sogenannten hyperbaren Lokalanästhetika sinken nach Einspritzen in den Subarachnoidalraum der Schwerkraft gehorchend nach unten, da sie wegen der Beimischung ein höheres spezifisches Gewicht als der Liquor cerebrospinalis haben. Dadurch lässt sich, abhängig von der Lagerung des Patienten, eine gezielte Ausbreitung des betäubten Bereiches erreichen.
Diverse Techniken der Lokalanästhesie in der Zahnmedizin wurden zur Schmerzausschaltung im Mund-, Kiefer- und Gesichtsbereich entwickelt.
Die Kombination von lokalanästhetisch wirksamen Stoffen mit Vasokonstriktoren wie Adrenalin, Noradrenalin oder Phenylephrin (im veterinärmedizinischen Sprachgebrauch auch als Sperrkörper bezeichnet) bewirkt eine Verengung der Blutgefäße im Wirkbereich und senkt so die Durchblutung. Dadurch wird der Abtransport eines Lokalanästhetikums verlangsamt und seine Wirkdauer verlängert. Außerdem führen Vasokonstriktoren zu weniger Blut im OP-Gebiet und somit besseren Übersicht für den Operateur. Dieses Vorgehen ist (Stand 2024) bei der operativen Anwendung an Akren (Hände, Finger, Füße und Zehen), Nase, Ohr und Penis ein Off-Label-Use, also eine zulassungsüberschreitende Anwendung: Wegen der potentiellen Gefahr des Endarterienverschlusses könnte eine Gewebenekrosen (Absterben von Geweben) durch Minderdurchblutung resultieren. In der Fachwelt hat sich aber mittlerweile die Erkenntnis verfestigt, dass die Kombination unbedenklich sei. Die gleichzeitige Gabe von Vasokonstriktoren mit Lokalanästhetika auch in diesen Körperbereichen ist gängige Praxis.[7][8] Als WALANT-Anästhesie (Akronym von englisch wide awake local anesthesia no tourniquet) fand sie Einzug in die Hand-Chirurgie.[9]
Externe Lokalanästhetika dienen der Therapie schmerzhafter Läsionen von Haut und Schleimhaut sowie zur Bekämpfung des Juckreizes. Außerdem werden sie zur Anästhesie der Hornhaut und der Bindehaut bei diagnostischen und operativen Eingriffen am Auge verwandt.[10] Angeboten werden sie je nach Anwendungsbereich als Salbe, Creme, Gel, Lotio, Lösung, Spray oder Pflaster.[11]
Unerwünschte Wirkungen
Zusammenfassung
Kontext
Bei den unerwünschten Wirkungen ist zu unterscheiden, worauf diese zurückzuführen sind, demnach
- auf die anästhetische Substanz
- einen zugesetzten Vasokonstriktor
- ein zugesetztes Konservierungsmittel
- auf die Konzentration und Dosierung
- auf Wechselwirkungen mit anderen Arzneimitteln
- auf die vorliegende Erkrankung
- auf eine Begleiterkrankung
- auf eine Allergie
- bei einer Schwangerschaft/Stillzeit
- auf die Applikationstechnik.
Lokalanästhetika können nicht nur die Bildung von Aktionspotentialen in peripheren Nerven blockieren, sondern auch in anderen Bereichen wie Gehirn oder Herz. Da sie im Allgemeinen (mit Ausnahme bei der intravenösen Regionalanästhesie) in die Nähe von peripheren Nerven bzw. Rückenmark appliziert werden, kommt es nicht zu solchen systemischen Wirkungen. Gelangt jedoch eine zu große Menge der verwendeten Substanz in das Kreislaufsystem, beispielsweise bei unbemerkter intravenöser Injektion, kann es zu unerwünschten Wirkungen kommen.
Wirkungsweise
Die Ursache der unerwünschten Wirkungen ist neben der Blockade der Natriumkanäle im Nervensystem und im Herzen auch die Störung von Kalziumkanälen sowie eine Entkopplung der Atmungskette in den Mitochondrien. Die durch die Symptome gestörte Atmung führt zu einer Azidose des Blutes, welche durch eine verringerte Plasmaeiweißbindung die Menge an freiem Lokalanästhethikum erhöht und das Eindringen in die Nerven und Herzzellen begünstigt. Erschwerend kommt hinzu, dass durch die Azidose der Blutfluss zum Gehirn erhöht wird und damit mehr Lokalanästhetikum dorthin gelangt. Schließlich entsteht auch eine intrazelluläre Azidose, welche das Lokalanästhetikum protoniert und an dem Herausdiffundieren aus der Zelle hindert. Dieser Mechanismus wird als Ion trapping (Ionenfalle) bezeichnet.[12]
Die Intoxikation kann in vier Stadien eingeteilt werden:
- Prodromalstadium (periorale Taubheit, metallischer Geschmack)
- Präkonvulsives Stadium (Tremor, Tinnitus, Nystagmus, Somnolenz)
- Konvulsives Stadium (generalisierte tonisch-klonische Anfälle)
- Stadium der ZNS Depression (Koma, Apnoe, Kreislaufkollaps)
ZNS-Nebenwirkungen
Bei zu hohen Plasmaspiegeln von Lokalanästhetika kommt es primär zu Funktionsstörungen des zentralen Nervensystems (ZNS). Diese können von Unruhe, Schwindelgefühl, oralem Kribbeln, metallischem Geschmack im Mund bzw. Taubheit bis hin zu generalisierten Krampfanfällen und Koma reichen. Da die zentralnervösen Symptome meist reversible sind, bemüht man sich, Medikamente zu verabreichen, deren ZNS-Nebenwirkungen lange vor den kardialen auftreten (hohe CC/CNS-Ratio, z. B. Ropivacain).
Kardiotoxizität
Am Herzen kann es bei einem zu hohen Plasmaspiegel eines Lokalanästhetikums zu Nebenwirkungen kommen. Es kann zur Abnahme der Herzkraft (Inotropie), Verlangsamung der Erregungsweiterleitung im Herzen bis hin zu lebensgefährlichen Herzrhythmusstörungen kommen.
Allergien
Allergien treten vor allem bei Lokalanästhetika vom Ester-Typ (Procain) auf, da beim Abbau dieser Substanzen Paraaminobenzoesäure entsteht, die für die allergische Reaktion verantwortlich gemacht wird (Kreuzallergie). Lokalanästhetika vom Ester-Typ werden in Deutschland meist äußerlich und nur noch sehr selten als Injektion angewendet. Injektionssfläschchen für die Mehrfachentnahme müssen zum Schutz vor mikrobiellem Verderb konserviert werden, etwa mit 4-Hydroxybenzoesäuremethylester und 4-Hydroxybenzoesäurepropylester (Parabene), die ein Allergisierungspotential haben.
Therapie der Intoxikation
Zusammenfassung
Kontext
Die Therapie konzentriert sich auf die Sicherung der Vitalfunktionen. Sauerstoffgabe erfolgt mit 15 l/min über Maske. Die Übergänge zwischen den Stadien sind zügig fließend und erfolgen nicht in strenger Reihenfolge. Bei Krampfäquivalenten sollten die Atemwege sofort durch Intubation gesichert werden. Vor allem bei Bupivacain, aber auch bei Ropivacain sind durch die hohe Lipophilie der Substanzen Blockierungen des Reizleitungssystems des Myokards zu erwarten. Diese Lipophilie liegt auch der Notfalltherapie mit endovenösen Lipiden (lipid-sink) zugrunde.
Nach den Empfehlungen der Deutschen Gesellschaft für Anästhesiologie und Intensivmedizin (DGAI) soll bei einer Lokalanästhetikaintoxikation neben der Sicherung der Vitalfunktion nach den aktuellen Reanimationsleitlinien auch frühzeitig der Einsatz von intravenöser Fettinfusion (Lipidemulsion, Lipid Rescue) erfolgen. In Tierexperimenten und klinischen Fallstudien am Menschen zeigt sich eine höhere Überlebensrate, wenn mit Fettinfusion behandelt wurde. Man vermutet, dass das verabreichte Fett im Blut das (lipophile) Lokalanästhetikum teilweise bindet und/oder am Herzen die schädliche Wirkung der Lokalanästhetika verringert. Zum Einsatz kommen übliche 20%ige Fettemulsionen, wie sie auch auf Intensivstationen zur intravenösen Ernährung genutzt werden. Der Einsatz dieser Fettinfusionen bei Lokalanästhetikaintoxikation ist jedoch ein sogenannter Off-Label Use außerhalb der vom Hersteller zugelassenen Verwendungszwecke. Die von der DGAI empfohlene Therapie ist der Tabelle zu entnehmen:
| Vorgehen bei Lokalanästhetika-Intoxikation.[13] |
|---|
| 1. Lokalanästhetikazufuhr stoppen |
| 2. Adäquate Oxygenierung, ggfs. Beatmung |
| 3. Kardiopulmonale Reanimation bei Herz-Kreislaufstillstand |
| 4. i.v.-Gabe von Lipidemulsion (Bolus 1,5 ml/kg; Infusion 0,1 ml/kg/min über 30 Minuten oder 0,5 ml/kg/min über 10 Minuten) |
| 5. Antikonvulsiva bei Krampfanfällen |
Unerwünschte Wirkungen bei äußerlicher Anwendung
Grundsätzlich sind die meisten Nebenwirkungen, die bei Injektion von Lokalanästhetika auftreten, auch bei lokaler Applikation denkbar, aber viel seltener, da weniger Wirkstoff in den Blutkreislauf gelangt. Probleme können entstehen bei größeren oder tieferen Läsionen sowie bei großflächiger oder häufiger Anwendung (Oberflächenanästhetika dürfen nicht in offene Wunden gebracht werden). Lokale allergische (selten auch systemische) Reaktionen teils gegen den Wirkstoff selbst, teils gegen die Trägersubstanz dürften noch am häufigsten sein.
Wirkstoffe
| Substanz | Struktur | Anwendungsart | Wirkeintritt | PKs | Wirkdauer | Proteinbindung | Einführung |
|---|---|---|---|---|---|---|---|
| Aminoamide | |||||||
| Lidocain |  | Injektion, extern | schnell | 7,9 | 60–120 min | 65 % | 1943 |
| Mepivacain |  | Injektion | schnell | 7,6 | 90–180 min | 75 % | 1957 |
| Prilocain | 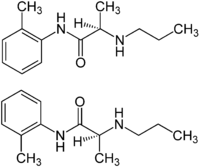 | Injektion, extern | schnell | 7,7 | 60–120 min | 55 % | 1960 |
| Articain (bis 1984 Carticain) |  | Injektion | schnell | 7,8 | 0,5–5 h | 95 % | 1970 |
| Bupivacain |  | Injektion | langsam | 8,1 | 4–5 h | 95 % | 1963 |
| Ropivacain | 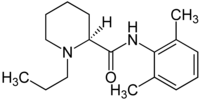 | Injektion | langsam | 8,1 | 4–6 h | 94 % | 1996 |
| Cinchocain (=Dibucain) |  | extern | langsam | 1,5–2 h | 1930 | ||
| Etidocain# |  | Injektion | schnell | 7,7 | 4–6 h | 95 % | 1972 |
| Aminoester | |||||||
| Procain |  | Injektion | langsam | 8,9 | 45–60 min | 5 % | 1905 |
| Benzocain | 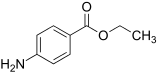 | extern | schnell | 3,5 | 30–60 min | 6 % | 1900 |
| Chloroprocain oder Chlorprocain |  | Injektion | schnell | 9,1 | 30–45 min | 1952 | |
| Oxybuprocain |  | extern | |||||
| Tetracain |  | extern | langsam | 8,6 | 60–180 min | 80 % | 1931 |
| Proxymetacain | 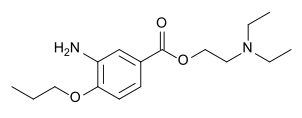 | extern | |||||
| Fomocaine | |||||||
| Fomocain# | 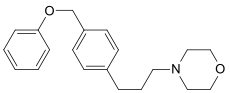 | extern | |||||
| andere | |||||||
| Quinisocain |  | extern | 1952 | ||||
| Dyclonin# |  | extern | |||||
| Lauromacrogol 400 (Polidocanol) | Strukturbeispiel | extern | |||||
| # In Deutschland keine Präparate zugelassen (Rote Liste Online, Oktober 2018). Referenzen:[14][15][16][17] | |||||||
Literatur
- Heinrich Braun: Über einige örtliche Anästhetika. In: Deutsche medizinische Wochenschrift. Band 31, 1905, S. 1665 ff.
- Leonard S. Jacob: Intensivkurs: Pharmakologie. Urban & Schwarzenberg, München / Wien / Baltimore 1995, ISBN 3-541-12831-3.
- H. A. McLure, A. P. Rubin: Review of local anaesthetic agents. In: Minerva Anestesiol. 2005 Mar; 71(3), S. 59–74. Review. PMID 15714182 (PDF, 113 kB)
- Christoph Klaus Müller, Die Lokalanästhesie. Welche Risiken bestehen aus allgemeinmedizinischer Sicht?, Zahnärzteblatt Baden-Württemberg, Ausgabe 03/2011. Abgerufen am 9. März 2015.
- H. Orth, I. Kis: Schmerzbekämpfung und Narkose. In: Franz Xaver Sailer, Friedrich Wilhelm Gierhake (Hrsg.): Chirurgie historisch gesehen. Anfang – Entwicklung – Differenzierung. Dustri-Verlag, Deisenhofen bei München 1973, ISBN 3-87185-021-7, S. 1–32, hier: S. 19 f.
- W. Zink, B. M. Graf: Toxikologie der Lokalanästhetika. Pathomechanismen – Klinik – Therapie. In: Anaesthesist. 2003 Dec; 52(12), S. 1102–1123. Review. PMID 14691623 (PDF, 462 kB).
Weblinks
Wiktionary: Lokalanästhetikum – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.