Lanthanchlorid
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Lanthanchlorid ist eine chemische Verbindung aus der Gruppe der Chloride.
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
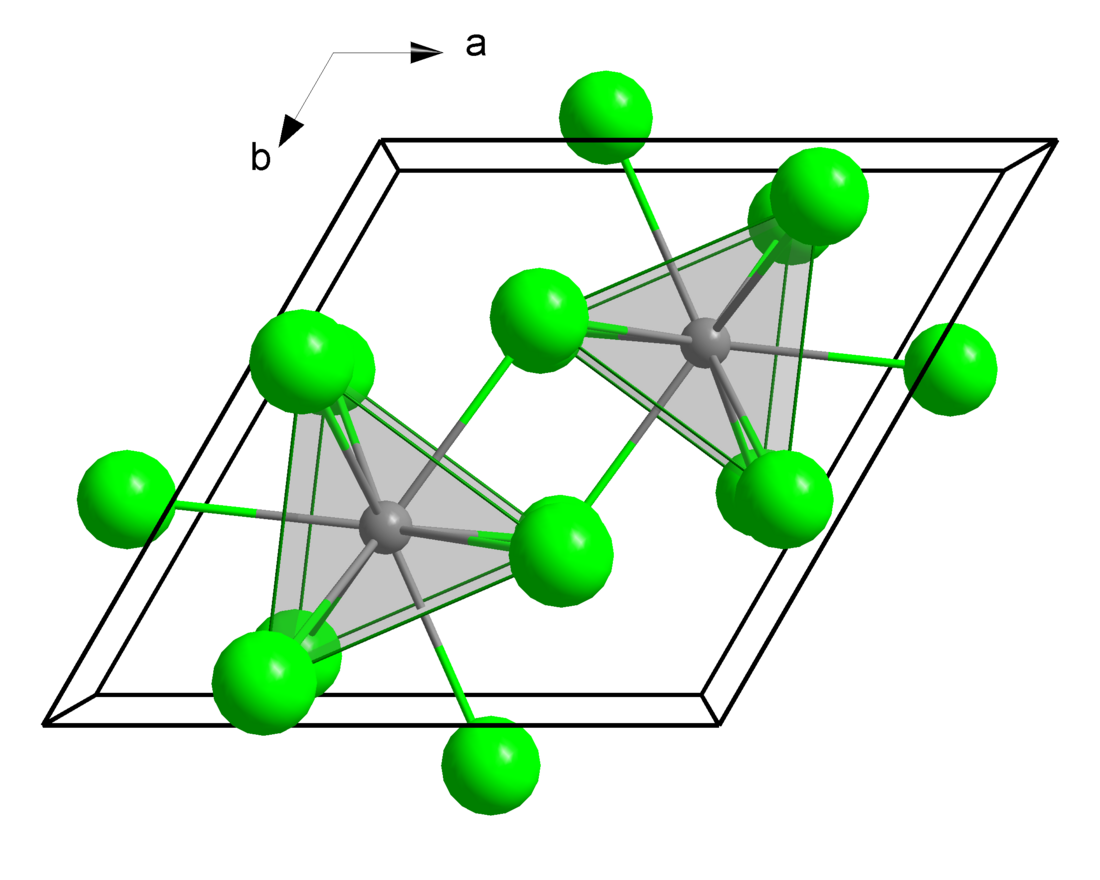
 | ||||||||||
| _ La3+ _ Cl− | ||||||||||
| Kristallsystem | ||||||||||
| Raumgruppe |
P63/m (Nr. 176) | |||||||||
| Gitterparameter |
a = 748 pm | |||||||||
| Koordinationszahlen |
La[9], Cl[3] | |||||||||
| Allgemeines | ||||||||||
| Name | Lanthanchlorid | |||||||||
| Andere Namen | ||||||||||
| Verhältnisformel | LaCl3 | |||||||||
| Kurzbeschreibung |
weißes Pulver[2] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 245,26 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Dichte | ||||||||||
| Schmelzpunkt | ||||||||||
| Siedepunkt |
1812 °C[4] | |||||||||
| Löslichkeit | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Toxikologische Daten | ||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Gewinnung und Darstellung
Lanthanchlorid kann durch Reaktion von Lanthanoxid mit Chlorwasserstoff gewonnen werden.
Lanthanchlorid kann ebenfalls über Reaktion mit Aluminiumchlorid bei 175 °C in einer ionischen Flüssigkeit erhalten werden.[8]
Eigenschaften
Lanthanchlorid bildet weiße hexagonale Kristalle, die hygroskopisch sind. Es kristallisiert in der Raumgruppe P63/m (Raumgruppen-Nr. 176) mit den Gitterparametern a = 748 pm, c = 436 pm und zwei Formeleinheiten pro Elementarzelle. Das Heptahydrat kristallisiert monoklin mit den Gitterparametern a = 1237 pm, b = 1068 pm, c = 923 pm und einem Winkel von 114,3°.[3] Das Heptahydrat wandelt sich oberhalb von 90 °C in das Anhydrat um.[9]
Verwendung
Lanthanchlorid wird als milde Lewis-Säure für chemische Reaktionen verwendet, die normalerweise saure Bedingungen erfordern, wie zum Beispiel der Umbau von Aldehyden zu Acetalen unter nahezu neutralen Bedingungen. Es dient auch als Katalysator beim Fluid catalytic cracking.[10] Das Heptyhydrat wird in der Medizin als Kalziumkanalblocker eingesetzt[9] und dient weiterhin in der Wasserwirtschaft zur Eindämmung von Algenwachstum durch Bindung von Phosphaten.[11]
Literatur
- Xiao He, Zhiyong Zhang, Haifeng Zhang, Yuliang Zhao, Zhifang Chai: Neurotoxicological Evaluation of Long-Term Lanthanum Chloride Exposure in Rats. In: Toxicological Sciences, 103 (2), 2008, S. 354–361; doi:10.1093/toxsci/kfn046.
Weblinks
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.