Diethylamin
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Diethylamin ist eine chemische Verbindung aus der Gruppe der aliphatischen sekundären Amine.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
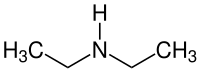 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Diethylamin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C4H11N | |||||||||||||||
| Kurzbeschreibung |
farblose, leichtentzündliche Flüssigkeit mit aminartigem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 73,14 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,71 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
56 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| pKS-Wert | ||||||||||||||||
| Löslichkeit |
vollständig mischbar mit Wasser[1] | |||||||||||||||
| Brechungsindex |
1,3864[4] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Diethylamin kann durch Reaktion von Ethanol mit Ammoniak gewonnen werden, wobei auch Ethylamin und Triethylamin entstehen.
Eigenschaften
Die wässrige Lösung von Diethylamin reagiert stark alkalisch. Ab etwa 500 °C zersetzt sich Diethylamin.[1] Es hat eine dynamische Viskosität von 0,34 mPa·s bei 25 °C.[4]
Sicherheitstechnische Kenndaten
Diethylamin bildet mit Luft leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt unterhalb von −20 °C.[1] Der Explosionsbereich liegt zwischen 1,7 Vol.‑% (50 g/m3) als untere Explosionsgrenze (UEG) und 10,1 Vol.‑% (305 g/m3) als obere Explosionsgrenze (OEG).[1][7] Die Grenzspaltweite wurde mit 1,15 mm (50 °C) bestimmt.[1] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIA.[1][7] Die Zündtemperatur beträgt 305 °C.[1][7] Der Stoff fällt somit in die Temperaturklasse T2.
Verwendung
Diethylamin wird zur Herstellung von Kautschuk-, Textil-, Flotationschemikalien, von Kunstharzen, Farb- und Arzneistoffen, Insektiziden, galvanischen Bädern und Polymerisationsverzögerern sowie als pH-Wert-Regler und Puffersubstanz verwendet. Es kann auch zur Herstellung des Nervengiftes Tabun verwendet werden[8]. Weiterhin wird es in der Herstellung von Elektrolytkondensatoren eingesetzt.[9]
Supramolekulare Struktur

Diethylamin ist das kleinste und einfachste Molekül das eine supramolekulare Helix als Aggregat mit niedrigster Energie aufweist. Andere ähnlich kleine wasserstoffverbrückte Moleküle bevorzugen zyklische Strukturen.[10]
Salze
Diethylamin bildet Hydrohalogenide wie das Diethylaminhydrochlorid und das Diethylaminhydrobromid[11]
Einzelnachweise
Wikiwand - on
Seamless Wikipedia browsing. On steroids.



