Loading AI tools
chemische Verbindung Aus Wikipedia, der freien Enzyklopädie
Aluminiumhydrid (Alan) ist eine chemische Verbindung aus den Elementen Aluminium und Wasserstoff mit der Verhältnisformel (AlH3)x. Es ist ein farbloses Pulver, welches oberhalb von 100 °C in seine Bestandteile zerfällt. Aluminiumhydrid ist außerordentlich feuchtigkeits- und oxidationsempfindlich. Es verbrennt explosionsartig an Luft und kann zur Speicherung von Wasserstoff in wasserstoffbetriebenen Fahrzeugen eingesetzt werden.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
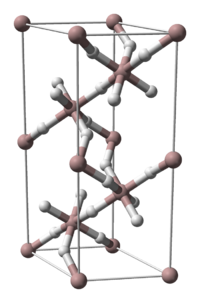 | |||||||||||||||||||
| _ Al3+ _ H− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Aluminiumhydrid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Verhältnisformel | (AlH3)x | ||||||||||||||||||
| Kurzbeschreibung |
farbloses Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 30,01 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,48 g·cm−3 [2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−46,0 kJ/mol[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Von Aluminiumhydrid kennt man fünf kristalline Phasen (α, γ, δ, ζ), von denen bislang nur die Struktur der α-Phase erforscht wurde. Durch Einbau von Magnesium mit einem Massenanteil (veraltet Gewichtsprozent) von 0,01 bis 3 % kann die Vakuumstabilität von α-Aluminiumhydrid signifikant erhöht werden.[5] Auch kann die Beständigkeit gegenüber Hydrolyse durch Tempern erhöht werden.[6] So behandeltes α-Aluminiumhydrid wurde intensiv als energetischer Zusatz für Raketentreibstoffe und Sprengstoffe untersucht.[7]
Die Darstellung von Aluminiumhydrid erfolgt zweckmäßig durch die Umsetzung von Aluminiumchlorid mit Lithiumaluminiumhydrid in Diethylether:[1]
Hierbei wird zunächst eine als Monomer anfallende Verbindung, das Etherat
gebildet, welche sich allmählich in das hochpolymere Aluminiumhydrid umwandelt.
Aluminiumhydrid reagiert mit Wasser sehr stark unter Wasserstoff-Freisetzung gemäß:
Zusammen mit anderen Metallhydriden bildet Aluminiumhydrid Alanate. Wichtigster Vertreter ist das Lithiumaluminiumhydrid (Lithiumalanat):
Wegen seiner Unlöslichkeit hat es als Reduktionsmittel kaum Bedeutung.[8]
Das Dimer Al2H6 ist isostrukturell zu Diboran (B2H6) und Digallan (Ga2H6).
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.